名校
解题方法
1 . 下列各组离子或分子在给定条件的溶液中可能大量共存的是
A.加入铝片有大量氢气产生的溶液中: 、 、 、 、 、 、 |
B.在0.1mol/L的盐酸中: 、 、 、 、 、 、 |
C.在强碱性溶液中: 、 、 、 、 、 、 |
D.碱性无色溶液中: 、 、 、 、 、 、 |
您最近半年使用:0次
2 . 下列选项描述与对应图像相符的是:

| A.图①为新制氯水在阳光直射时,溶液中Cl-浓度随着时间变化的曲线 |
| B.图②为等物质的量的NaOH和Na2CO3混合液中逐滴加入盐酸产生CO2的图像 |
| C.图③为NaOH溶液中滴加MgSO4溶液的导电性变化图像 |
| D.图④为AlCl3溶液中滴加NaOH溶液的沉淀变化图像 |
您最近半年使用:0次
3 . 在给定条件下,下列选项所示的物质间转化均能实现的是
A.Br2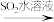 HBr HBr Br2 Br2 |
B.Fe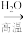 Fe2O3 Fe2O3 Fe Fe |
C.Al2O3 Al Al Al(OH)3 Al(OH)3 |
D. |
您最近半年使用:0次
4 . 某无色溶液中只可能含有K+、Al3+、Ba2+、Mg2+、Cl-、NO 、CO
、CO 、SO
、SO 中的一种或几种,对其进行如下实验操作:①取少量溶液,滴加足量稀硫酸,产生白色沉淀;②另取少量溶液,加入AgNO3溶液,也有白色沉淀生成;③再取少量溶液,加入少量NaOH溶液,同样有白色沉淀生成;④向③所得混合物中继续加入NaOH溶液至过量,沉淀全部溶解。试回答下列问题:
中的一种或几种,对其进行如下实验操作:①取少量溶液,滴加足量稀硫酸,产生白色沉淀;②另取少量溶液,加入AgNO3溶液,也有白色沉淀生成;③再取少量溶液,加入少量NaOH溶液,同样有白色沉淀生成;④向③所得混合物中继续加入NaOH溶液至过量,沉淀全部溶解。试回答下列问题:
(1)该溶液中肯定存在的离子为___________ ;
(2)该溶液中肯定不存在的离子为___________ ;
(3)该溶液中无法确定的离子为___________ ;
(4)第①步实验中发生的离子反应方程式为___________ ;
(5)第③步实验中产生的白色沉淀为___________ (填化学式);
(6)第④步实验中沉淀溶解的化学方程式为___________ 。
 、CO
、CO 、SO
、SO 中的一种或几种,对其进行如下实验操作:①取少量溶液,滴加足量稀硫酸,产生白色沉淀;②另取少量溶液,加入AgNO3溶液,也有白色沉淀生成;③再取少量溶液,加入少量NaOH溶液,同样有白色沉淀生成;④向③所得混合物中继续加入NaOH溶液至过量,沉淀全部溶解。试回答下列问题:
中的一种或几种,对其进行如下实验操作:①取少量溶液,滴加足量稀硫酸,产生白色沉淀;②另取少量溶液,加入AgNO3溶液,也有白色沉淀生成;③再取少量溶液,加入少量NaOH溶液,同样有白色沉淀生成;④向③所得混合物中继续加入NaOH溶液至过量,沉淀全部溶解。试回答下列问题:(1)该溶液中肯定存在的离子为
(2)该溶液中肯定不存在的离子为
(3)该溶液中无法确定的离子为
(4)第①步实验中发生的离子反应方程式为
(5)第③步实验中产生的白色沉淀为
(6)第④步实验中沉淀溶解的化学方程式为
您最近半年使用:0次
名校
5 . 下列转化不能通过一步反应实现的是
A. | B. |
C. | D.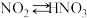 |
您最近半年使用:0次
名校
解题方法
6 . 下列指定反应的离子方程式书写正确的是
| A.AlCl3溶液中加入过量氨水:Al3++3OH-=A1(OH)3↓ |
B.K3[Fe(CN)6]溶液滴入FeCl2溶液中: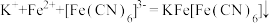 |
C.Cu与浓HNO3反应: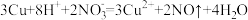 |
D.酸性KMnO4溶液滴定H2C2O4溶液: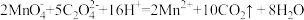 |
您最近半年使用:0次
昨日更新
|
180次组卷
|
2卷引用:安徽省合肥市第一中学2024届高三第一次教学质量检测化学试题
解题方法
7 . 在 的溶液中能大量共存的离子组是
的溶液中能大量共存的离子组是
 的溶液中能大量共存的离子组是
的溶液中能大量共存的离子组是A.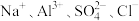 | B.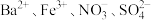 |
C.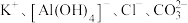 | D.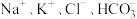 |
您最近半年使用:0次
解题方法
8 . 氧化铝粉体材料广泛应用于生物陶瓷、电子、催化剂、航空航天等领域。下图为利用钾明矾石精矿[主要成分为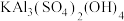 及少量
及少量 ]制备超细
]制备超细 的工艺流程。
的工艺流程。
(1)“粉碎”的目的是_____ 。
(2)“碱浸”过程中相关数据如图 ,则应选择的合适条件为
,则应选择的合适条件为_____ ,在该条件下, 转化为
转化为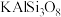 沉淀。
沉淀。_____ (写出一条即可)。
(4)“酸溶”时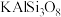 溶解反应的离子方程式为
溶解反应的离子方程式为_____ 。
(5)“沉铝”反应生成难溶物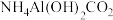 及无色气体,反应的离子方程式为
及无色气体,反应的离子方程式为_____ 。检验沉淀是否洗涤干净的方法为_____ 。
(6)流程中部分副产物稍加处理便能循环利用,写出其中一种的化学式_____ 。
(7)工业生产中常用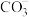 和
和 来沉淀
来沉淀 ,已知常温下,在
,已知常温下,在 和
和 共存的悬浊液中,
共存的悬浊液中, 。则
。则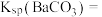
_____ 。[已知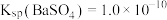 ]
]
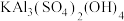 及少量
及少量 ]制备超细
]制备超细 的工艺流程。
的工艺流程。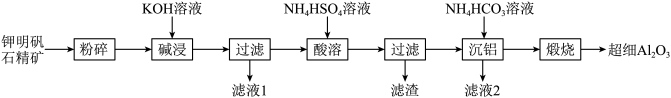
(1)“粉碎”的目的是
(2)“碱浸”过程中相关数据如图
 ,则应选择的合适条件为
,则应选择的合适条件为 转化为
转化为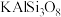 沉淀。
沉淀。
(4)“酸溶”时
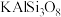 溶解反应的离子方程式为
溶解反应的离子方程式为(5)“沉铝”反应生成难溶物
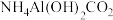 及无色气体,反应的离子方程式为
及无色气体,反应的离子方程式为(6)流程中部分副产物稍加处理便能循环利用,写出其中一种的化学式
(7)工业生产中常用
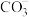 和
和 来沉淀
来沉淀 ,已知常温下,在
,已知常温下,在 和
和 共存的悬浊液中,
共存的悬浊液中, 。则
。则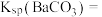
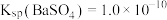 ]
]
您最近半年使用:0次
名校
解题方法
9 . 取一定体积且物质量浓度相同的两种试剂进行反应.改变两种试剂的滴加顺序,反应现象明显不同的是
选项 | 试剂① | 试剂② |
A | 硫酸 | 氢氧化钡溶液 |
B |
|
|
C |
|
|
D |
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 下列物质之间的转化都一步能实现的是
A.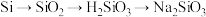 |
B. →Na[Al(OH)4] →Na[Al(OH)4] |
C.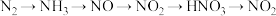 |
D. |
您最近半年使用:0次

 溶液
溶液 溶液
溶液 溶液
溶液 溶液
溶液 溶液
溶液 溶液
溶液

