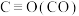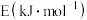名校
1 . 从海水中提取澳的工业流程如图,下列说法正确的是

| A.海水晒盐利用的是蒸发结晶法 |
| B.获取Cl2的同时可以得到金属钠,通常采用热分解法 |
| C.步骤Ⅱ中溴与碳酸钠反应中氧化剂与还原剂物质的量之比为1:1 |
| D.实验室分离溴还可以用溶剂萃取法,乙醇可以用作溴的萃取剂 |
您最近一年使用:0次
名校
2 . 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
(1)工业合成氨反应: 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知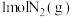 完全反应生成
完全反应生成 可放出
可放出 热量。如果将
热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量_______ (填“大于”、“小于”或“等于”)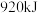 。
。
(2)实验室模拟工业合成氨时,在容积为 的密闭容器内,反应经过
的密闭容器内,反应经过 后,生成
后,生成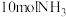 ,用
,用 表示的化学反应速率为
表示的化学反应速率为_______ 。
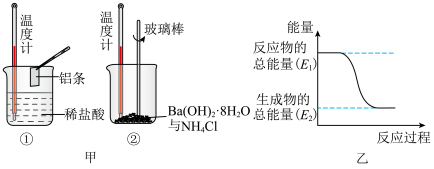
(3)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度_______ (填“升高”或“降低”),反应过程_______ (填“①”或“②”)的能量变化可用图乙表示。_______ (填字母)。
A.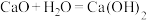
B.
C.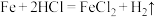
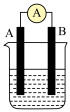
(5)如图为原电池装置示意图。 为
为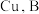 为石墨,电解质为
为石墨,电解质为 溶液,工作时的总反应为
溶液,工作时的总反应为 。
。_______ 极(填“正”或“负”)。
②该电池在工作时,溶液中 向
向_______ (填“A”或“B”)移动, 电极的质量将
电极的质量将_______ (填“增加”、“减小”或“不变”)。
(6)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。_______ 。
②有关反应一段时间后的实验现象,下列说法正确的是_______ (填字母)。
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(1)工业合成氨反应:
 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知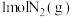 完全反应生成
完全反应生成 可放出
可放出 热量。如果将
热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量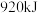 。
。(2)实验室模拟工业合成氨时,在容积为
 的密闭容器内,反应经过
的密闭容器内,反应经过 后,生成
后,生成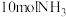 ,用
,用 表示的化学反应速率为
表示的化学反应速率为(3)某实验小组同学进行如图甲所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度
A.
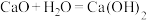
B.

C.
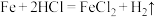
(5)如图为原电池装置示意图。
 为
为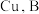 为石墨,电解质为
为石墨,电解质为 溶液,工作时的总反应为
溶液,工作时的总反应为 。
。
②该电池在工作时,溶液中
 向
向 电极的质量将
电极的质量将(6)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。
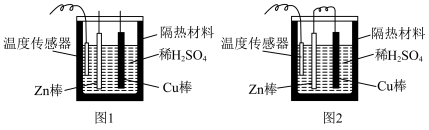
②有关反应一段时间后的实验现象,下列说法正确的是
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
您最近一年使用:0次
名校
3 . 回答下列问题。
(1)已知反应 中相关的化学键键能数据如表:
中相关的化学键键能数据如表:
若有 生成,该反应
生成,该反应_______ (填“吸收”或“放出”)_______  能量。
能量。
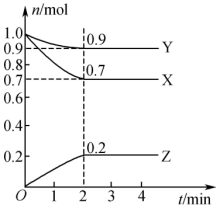
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:_______ 。
(3)反应从开始至2min,用Z的浓度变化表示的平均反应速率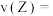
_______ 。
(4)2min后反应达到平衡,容器内混合气体的平均相对分子质量比起始时_______ (填“增大”“减小”或“不变”下同);混合气体的密度_______ 。
(5)将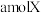 与
与 的混合气体通入
的混合气体通入 的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足:
的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足: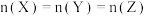 ,则原混合气体中
,则原混合气体中
_______ 。
(6)下列措施能加快反应速率的是_______ (填序号,下同)。
A.恒压时充入 B.恒容时充入He
B.恒容时充入He
C.恒容时充入X D.及时分离出
E.升高温度 F.选择高效的催化剂
(7)下列说法正确的是_______ 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
(1)已知反应
 中相关的化学键键能数据如表:
中相关的化学键键能数据如表:化学键 |
|
|
|
|
|
| 436 | 343 | 1076 | 465 | 413 |
 生成,该反应
生成,该反应 能量。
能量。某温度时,在2L的密闭容器中,X、Y、Z(均为气体)的物质的量随时间的变化曲线如图所示。请回答下列问题:
(3)反应从开始至2min,用Z的浓度变化表示的平均反应速率
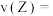
(4)2min后反应达到平衡,容器内混合气体的平均相对分子质量比起始时
(5)将
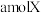 与
与 的混合气体通入
的混合气体通入 的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足:
的密闭容器中并发生上述反应,反应到某时刻各物质的物质的量恰好满足: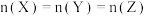 ,则原混合气体中
,则原混合气体中
(6)下列措施能加快反应速率的是
A.恒压时充入
 B.恒容时充入He
B.恒容时充入HeC.恒容时充入X D.及时分离出

E.升高温度 F.选择高效的催化剂
(7)下列说法正确的是
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关
D.化学反应的限度是不可能改变的
E.增大Y的浓度,正反应速率加快,逆反应速率减慢
您最近一年使用:0次
4 . 下列各组物质均由一种干燥气体和一种液体组成,其中可以进行喷泉实验,且液体几乎充满烧瓶的组合是
A. ,稀盐酸 ,稀盐酸 | B. ,稀硫酸 ,稀硫酸 | C. ,饱和食盐水 ,饱和食盐水 | D. ,水 ,水 |
您最近一年使用:0次
名校
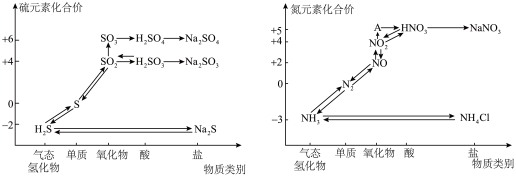
5 . 硫、氮的氧化物都会引起环境问题,越来越引起人们的重视.如图是硫、氮元素的各种价态与物质类别的对应关系:
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为________ (填化学式);
(2)若将 通入紫色石蕊溶液中可观察到的现象为
通入紫色石蕊溶液中可观察到的现象为________________ ;
(3)根据A对应的化合价和物质类别,A为________ (写分子式);
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择________ ,反
应的离子方程式为________________ ;
(5)工业生产中利用氨水吸收 和
和 ,流程如图所示:
,流程如图所示: 被吸收过程的离子方程式是
被吸收过程的离子方程式是________________ ;
(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下: ;
; ;若用某
;若用某 溶液恰好完全吸收含
溶液恰好完全吸收含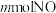 和
和 的大气污染物,则
的大气污染物,则 的物质的量为
的物质的量为________  .若所得溶液中
.若所得溶液中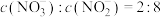 ,则原混合气体中
,则原混合气体中 和
和 物质的量之比
物质的量之比
________ 。
(1)从硫元素的化合价变化的角度判断,图中只有还原性的含硫化合物为
(2)若将
 通入紫色石蕊溶液中可观察到的现象为
通入紫色石蕊溶液中可观察到的现象为(3)根据A对应的化合价和物质类别,A为
(4)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
应的离子方程式为
(5)工业生产中利用氨水吸收
 和
和 ,流程如图所示:
,流程如图所示: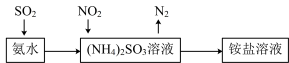
 被吸收过程的离子方程式是
被吸收过程的离子方程式是(6)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
 ;
; ;若用某
;若用某 溶液恰好完全吸收含
溶液恰好完全吸收含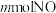 和
和 的大气污染物,则
的大气污染物,则 的物质的量为
的物质的量为 .若所得溶液中
.若所得溶液中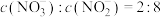 ,则原混合气体中
,则原混合气体中 和
和 物质的量之比
物质的量之比
您最近一年使用:0次
名校
解题方法
6 . 下列实验装置正确且能够达到目的的是

A.甲装置除去 中的 中的 杂质 杂质 | B.乙装置证明 和浓 和浓 反应放热 反应放热 |
C.丙装置制取并收集 | D.丁装置制取 并控制气体产生或停止 并控制气体产生或停止 |
您最近一年使用:0次
7 . 二氧化硅是玻璃的主要成分之一。下列说法错误的是
| A.二氧化硅高温下可与碳酸钙反应 |
| B.二氧化硅为酸性氧化物,能与水反应生成硅酸 |
| C.实验室不能用磨口玻璃塞试剂瓶盛放氢氧化钠溶液 |
| D.氢氟酸能雕刻玻璃,不能用玻璃瓶盛放氢氟酸 |
您最近一年使用:0次
名校
8 . 在恒容密闭容器中,由 合成甲醇
合成甲醇 的反应为
的反应为 ,在其他条件不变的情况下,测得温度对反应的影响结果如图所示.下列有关说法错误的是
,在其他条件不变的情况下,测得温度对反应的影响结果如图所示.下列有关说法错误的是
 合成甲醇
合成甲醇 的反应为
的反应为 ,在其他条件不变的情况下,测得温度对反应的影响结果如图所示.下列有关说法错误的是
,在其他条件不变的情况下,测得温度对反应的影响结果如图所示.下列有关说法错误的是
A.平衡常数表达式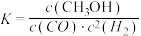 |
B.平衡常数: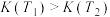 |
C. 合成 合成 反应的 反应的 |
D.处于A点的反应体系从 变到 变到 ,达到平衡状态时 ,达到平衡状态时 减小 减小 |
您最近一年使用:0次
名校
9 . 向恒容密闭容器中充入一定体积的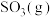 ,发生反应
,发生反应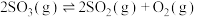 ,
, 后达到平衡.若保持温度不变,再充入相同体积的
后达到平衡.若保持温度不变,再充入相同体积的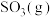 ,达到新平衡后,与原平衡相比,下列值增大的是
,达到新平衡后,与原平衡相比,下列值增大的是
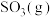 ,发生反应
,发生反应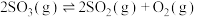 ,
, 后达到平衡.若保持温度不变,再充入相同体积的
后达到平衡.若保持温度不变,再充入相同体积的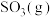 ,达到新平衡后,与原平衡相比,下列值增大的是
,达到新平衡后,与原平衡相比,下列值增大的是A.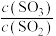 | B. 的转化率 的转化率 | C.平衡常数K | D.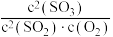 |
您最近一年使用:0次
名校
10 . 硫、氮及其化合物在生活中被广泛使用.下列有关离子方程式书写错误的是
A. 溶于足量稀硝酸: 溶于足量稀硝酸: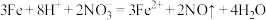 |
B.用足量 溶液吸收 溶液吸收 尾气: 尾气: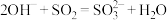 |
C. 使溴水褪色: 使溴水褪色: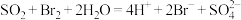 |
D.向 溶液中滴加 溶液中滴加 溶液并加热: 溶液并加热: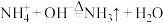 |
您最近一年使用:0次