解题方法
1 . 设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.标准状况,2.24LO2中含有分子的数目为0.1NA |
| B.2.3g Na与Cl2反应,转移电子的数目为 0.2NA |
| C.0.1mo1/LNa2CO3溶液中,合有Na+的数目为0.2NA |
| D.常温常压下,1.8gH2O中含有原子的数目为0.1NA |
您最近一年使用:0次
名校
2 . 如图为 和
和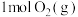 反应生成
反应生成 过程中的能量变化,下列说法正确的是
过程中的能量变化,下列说法正确的是
 和
和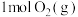 反应生成
反应生成 过程中的能量变化,下列说法正确的是
过程中的能量变化,下列说法正确的是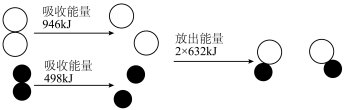
| A.该反应为放热反应 |
B.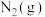 和 和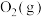 反应生成 反应生成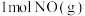 吸收能量为180kJ 吸收能量为180kJ |
| C.断开氮分子内两个氮原子间的化学键需要较多的能量,所以氮气的化学性质很稳定 |
D.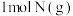 和 和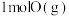 总能量比 总能量比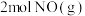 能量高 能量高 |
您最近一年使用:0次
7日内更新
|
272次组卷
|
3卷引用:浙江省9+1高中联盟2023-2024学年高一下学期4月期中考试化学试题
浙江省9+1高中联盟2023-2024学年高一下学期4月期中考试化学试题(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)名校期末好题汇编-化学反应与能量(选择题)
名校
3 . 锌-空气电池(原理如图)适宜用作城市电动车的动力电源。该电池放电时 转化为
转化为 。该电池工作时,下列说法不正确的是
。该电池工作时,下列说法不正确的是
 转化为
转化为 。该电池工作时,下列说法不正确的是
。该电池工作时,下列说法不正确的是
A. 是该电池的负极 是该电池的负极 |
B.石墨电极的电极反应: |
C. 向石墨电极移动 向石墨电极移动 |
D.电子由 极流出到石墨电极,再经溶液回到 极流出到石墨电极,再经溶液回到 极,形成回路 极,形成回路 |
您最近一年使用:0次
名校
4 . 部分含氮物质的分类与相应氮元素的化合价关系如图所示。下列说法正确的是
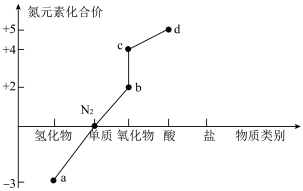
A.实验室可以通过加热固体 来制备a 来制备a |
B.C能使湿润的淀粉— 试纸变蓝 试纸变蓝 |
C.b和c都能与 溶液反应 溶液反应 |
D. 与d的浓溶液常温下不反应,故可以用铝槽车运输d的浓溶液 与d的浓溶液常温下不反应,故可以用铝槽车运输d的浓溶液 |
您最近一年使用:0次
2024-06-06更新
|
149次组卷
|
2卷引用:浙江省浙南名校2023-2024学年高一下学期4月期中联考化学试题
名校
5 . 氮化镁( )是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用
)是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用 与
与 的反应制备氮化镁,并设计了如下装置。
的反应制备氮化镁,并设计了如下装置。
(1)仪器a的名称为_______ 。
(2) 可通过饱和
可通过饱和 溶液与固体
溶液与固体 共热制得,则A处应选用装置
共热制得,则A处应选用装置_______ (填“①”或“②”或“③”),该反应的化学方程式为_______ 。_______ 。
(4)下列说法正确的是_______。
(5)取18g镁粉进行实验,将反应后的固体产物与水充分反应,经过滤、洗涤、干燥得到38.4g固体,则镁粉与氮气反应时 的转化率为
的转化率为_______ 。
 )是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用
)是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用 与
与 的反应制备氮化镁,并设计了如下装置。
的反应制备氮化镁,并设计了如下装置。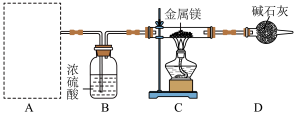
(1)仪器a的名称为
(2)
 可通过饱和
可通过饱和 溶液与固体
溶液与固体 共热制得,则A处应选用装置
共热制得,则A处应选用装置
(4)下列说法正确的是_______。
| A.导管b的作用为平衡气压,使液体顺利滴下 |
| B.实验时应先点燃C处酒精灯预热后,再开始装置A的反应 |
C.装置D中碱石灰可以换成无水 |
D.可用稀盐酸检验反应后的固体产物中是否存在尚未反应完的 |
(5)取18g镁粉进行实验,将反应后的固体产物与水充分反应,经过滤、洗涤、干燥得到38.4g固体,则镁粉与氮气反应时
 的转化率为
的转化率为
您最近一年使用:0次
名校
解题方法
6 . 下列表示正确的是
A.甲基的电子式: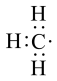 | B.乙醛的结构简式: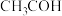 |
C. 的结构示意图: 的结构示意图: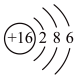 | D.次氯酸的结构式: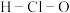 |
您最近一年使用:0次
名校
7 . 在2L密闭容器中,800℃时,反应 体系中,
体系中,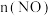 )随时间的变化如下表所示。下列有关说法正确的是
)随时间的变化如下表所示。下列有关说法正确的是
 体系中,
体系中,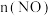 )随时间的变化如下表所示。下列有关说法正确的是
)随时间的变化如下表所示。下列有关说法正确的是| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
 | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
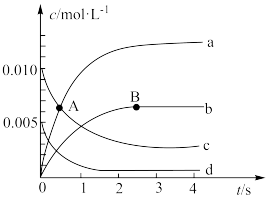
A.图中表示 变化的曲线是a 变化的曲线是a |
| B.A点处于化学平衡状态 |
C.0~2s内 平均速率 平均速率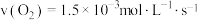 |
D.恒容条件下,充入 化学反应速率增大 化学反应速率增大 |
您最近一年使用:0次
名校
8 .  受热分解常用于实验室制备
受热分解常用于实验室制备 。工业制备
。工业制备 中,首先以软锰矿(主要成分为
中,首先以软锰矿(主要成分为 )为原料生成
)为原料生成 ,进而利用
,进而利用 “酸性歧化法”生成
“酸性歧化法”生成 ,流程如下图所示。
,流程如下图所示。 。下列说法正确的是
。下列说法正确的是
 受热分解常用于实验室制备
受热分解常用于实验室制备 。工业制备
。工业制备 中,首先以软锰矿(主要成分为
中,首先以软锰矿(主要成分为 )为原料生成
)为原料生成 ,进而利用
,进而利用 “酸性歧化法”生成
“酸性歧化法”生成 ,流程如下图所示。
,流程如下图所示。
 。下列说法正确的是
。下列说法正确的是A.软锰矿熔融时发生的化学反应为: |
| B.熔融过程温度较高,可以选用氧化铝坩埚作反应容器 |
| C.“酸化”时可以用盐酸代替硫酸 |
D.“结晶”获取 晶体时采用蒸发结晶 晶体时采用蒸发结晶 |
您最近一年使用:0次
名校
9 . 下列装置或操作一定能达到实验目的是
|
|
| A.用于制备并收集少量干燥氨气 | B.排水法收集 |
|
|
C.验证反应是否有 生成 生成 | D.验证非金属性: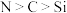 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-04更新
|
147次组卷
|
2卷引用:浙江省9+1高中联盟2023-2024学年高一下学期4月期中考试化学试题
名校
10 . 一些元素在周期表中的分布情况如图:___________ 。
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序___________ (用离子符号表示)。
(3)Sn的价电子数为___________ 。
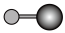
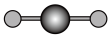
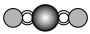
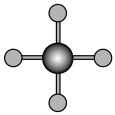
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
(6)用电子式表示 的形成过程
的形成过程___________ 。
(7)在下列物质中:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是___________ ;既存在离子键又存在极性键的是___________ 。
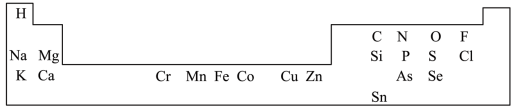
(2)Na、Cl、K元素对应的简单离子半径由小到大的顺序
(3)Sn的价电子数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确是___________(填字母)。
| A | B | C | D |
 |  |  |  |
|
|
|
|
| 直线形 | 直线形 | 直线形 | 平面正方形 |
| A.A | B.B | C.C | D.D |
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是___________。
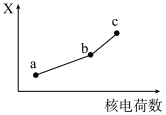
| A.若a、b、c表示ⅠA族金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示ⅦA族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示ⅥA族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第ⅡA族元素,则X表示最高价氧化物对应水化物的碱性 |
(6)用电子式表示
 的形成过程
的形成过程(7)在下列物质中:①
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦Ar⑧
⑦Ar⑧ (用物质前序号填空)。其中既存在极性键又存在非极性键的是
(用物质前序号填空)。其中既存在极性键又存在非极性键的是
您最近一年使用:0次