1 . KI可用作制有机化合物及制药原料,医疗上用于防治甲状腺肿和甲状腺功能亢进的手术前准备所需药物,也可用作祛痰药。某实验小组设计制备一定量KI的实验(加热及夹持装置已省略)如下:
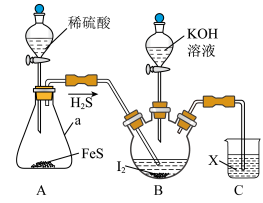
(1)实验开始前,先进行的操作为_______ 。
(2)仪器a的名称是_______ 。
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是_______ 。
(4)久置KI溶液易被氧化而导致变质,实验小组取久置KI溶液进行实验,如图所示。
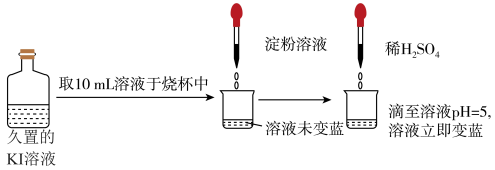
关于溶液立即变蓝的原因,该实验小组进行了如下探究,请将空格补充完整:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ.KI溶液久置过程中产生了 ;
; 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。
②实验与结论
(5)测定KI的纯度:称取0.5000g样品溶于水,加入稍过量硫酸酸化的H2O2充分反应后,加热除去过量H2O2,加入几滴淀粉溶液,用0.2000mol·L-1的Na2S2O3标准溶液滴定( )。
)。
①滴定前装有标准液的滴定管排气泡时,应选择图中的_______ (填标号,下同)。
a.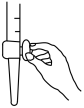 b.
b.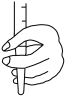 c.
c.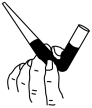 d.
d.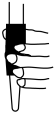
②若用25.00ml的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积_______ 。
a.=10.00mL b.=15.00mL c.<10.00mL d.>15.00mL
③滴定终点时消耗14.50mL标准溶液,则样品的纯度为_______ (计算结果保留两位有效数字)。

(1)实验开始前,先进行的操作为
(2)仪器a的名称是
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是
(4)久置KI溶液易被氧化而导致变质,实验小组取久置KI溶液进行实验,如图所示。

关于溶液立即变蓝的原因,该实验小组进行了如下探究,请将空格补充完整:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ.KI溶液久置过程中产生了
 ;
; 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。②实验与结论
| 实验编号 | 实验方案 | 实验现象 | 结论与解释 |
| ⅰ | 往试管中加入10mL0.1mol·L-1新制KI溶液并加入几滴淀粉溶液, | 50min后溶液变蓝 | 猜想Ⅰ不成立 |
| ⅱ | 取少量KIO3溶液与少量KI溶液混合,加入淀粉溶液,再滴加稀H2SO4调节pH至5 | 溶液立即变蓝 | 猜想Ⅱ成立。写出相关反应的离子方程式 |
 )。
)。①滴定前装有标准液的滴定管排气泡时,应选择图中的
a.
 b.
b. c.
c. d.
d.
②若用25.00ml的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
a.=10.00mL b.=15.00mL c.<10.00mL d.>15.00mL
③滴定终点时消耗14.50mL标准溶液,则样品的纯度为
您最近一年使用:0次
2023-09-09更新
|
148次组卷
|
4卷引用:青海省海东市名校2023-2024学年高三上学期9月联考化学试题
名校
2 . 食品安全关系国计民生,影响食品安全的因素很多.下面是以食品为主题的相关问题,请根据要求回答.
(1)聚偏二氯乙烯(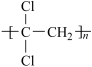 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由___________ (写结构简式) 单体发生加聚反应生成的.若以乙炔为原料,通过加成反应生成1,1,2三氯乙烷,再和氢氧化钠醇溶液反应可合成这种单体,则在加成反应中宜选择的试剂是_________ .(选填编号字母)
a.HCl b.Cl2 c.HClO d.NaCl
(2)人们从食用植物油中摄取的亚油酸[ ]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是___________ (选填编号字母).
a.分子式为C18H34O2
b.在食用油中亚油酸通常是以甘油酯的形式存在
c.亚油酸属于一种不饱和低级脂肪酸,所以能和NaOH溶液反应
d.亚油酸含量高的植物油在空气中易氧化变质
(3)食用酱油中的“氯丙醇”是多种氯代丙醇的总称,它们是在酱油配制过程中植物蛋白水解发生一系列化学变化而产生的,氯丙醇中部分异构体对人体有不同程度的致癌效应.则氯丙醇中三氯丙醇异构体共有_________ 种(已知卤原子和羟基一般不会连在同一碳原子上).
(4)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖,请设计实验证明淀粉已经全部水解,写出操作方法、现象和结论______________ .
(5)木糖醇[CH2OH(CHOH)3CH2OH]作为一种甜味剂,食用后不会引起血糖升高,比较适合于糖尿病人食用.预测木糖醇能和新制备的Cu(OH)2浊液发生化学反应的依据是___________ .
(6)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60.
②对A的水溶液进行测定发现该溶液pH<7.
③核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值,根据峰值可以确定分子中氢原子的种类和数目.例如乙醇有三种氢原子(图1).经测定有机物A的核磁共振氢谱示意图如图2
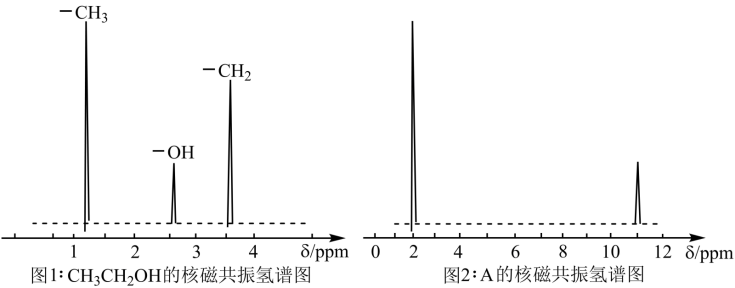
根据以上分析,写出A的结构简式__________ .
(1)聚偏二氯乙烯(
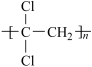 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由a.HCl b.Cl2 c.HClO d.NaCl
(2)人们从食用植物油中摄取的亚油酸[
 ]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是a.分子式为C18H34O2
b.在食用油中亚油酸通常是以甘油酯的形式存在
c.亚油酸属于一种不饱和低级脂肪酸,所以能和NaOH溶液反应
d.亚油酸含量高的植物油在空气中易氧化变质
(3)食用酱油中的“氯丙醇”是多种氯代丙醇的总称,它们是在酱油配制过程中植物蛋白水解发生一系列化学变化而产生的,氯丙醇中部分异构体对人体有不同程度的致癌效应.则氯丙醇中三氯丙醇异构体共有
(4)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖,请设计实验证明淀粉已经全部水解,写出操作方法、现象和结论
(5)木糖醇[CH2OH(CHOH)3CH2OH]作为一种甜味剂,食用后不会引起血糖升高,比较适合于糖尿病人食用.预测木糖醇能和新制备的Cu(OH)2浊液发生化学反应的依据是
(6)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60.
②对A的水溶液进行测定发现该溶液pH<7.
③核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值,根据峰值可以确定分子中氢原子的种类和数目.例如乙醇有三种氢原子(图1).经测定有机物A的核磁共振氢谱示意图如图2

根据以上分析,写出A的结构简式
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.实验室有一瓶失去标签的某白色固体X,已知其成分可能是碳酸或亚硫酸的钠盐或钾盐,且成分单一。现某化学小组通过如下步骤来确定其成分:
(1)阳离子的确定
实验方法及现象:__ 。
结论:此白色固体是钠盐。
(2)阴离子的确定
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需继续进行如下实验:取适量白色固体配成溶液,取少许该溶液于试管中,加入BaCl2溶液,出现白色沉淀。
结论:__ 。
Ⅱ.确认其成分后,由于某些原因,该白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤①:称取样品1.000g。
步骤②:将样品溶解后完全转移到250mL容量瓶中,定容,充分摇匀。
步骤③:移取25.00mL样品溶液于250mL锥形瓶中,用0.01mol·L-1KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤③所发生反应的离子方程式:__ 。
(2)判断滴定终点的现象是__ 。
(3)在配制0.01mol·L-1KMnO4溶液定容时若仰视,则最终测得变质固体中X的含量__ (填“偏大”、“偏小”或“无影响”)。
(4)滴定结果如表所示:
则该变质固体中X的质量分数为___ 。
(1)阳离子的确定
实验方法及现象:
结论:此白色固体是钠盐。
(2)阴离子的确定
①取少量白色固体于试管中,然后向试管中加入稀盐酸,白色固体全部溶解,产生无色气体,此气体能使溴水褪色。
②要进一步确定其成分需继续进行如下实验:取适量白色固体配成溶液,取少许该溶液于试管中,加入BaCl2溶液,出现白色沉淀。
结论:
Ⅱ.确认其成分后,由于某些原因,该白色固体部分被空气氧化,该化学小组想用已知浓度的酸性KMnO4溶液来确定变质固体中X的含量,具体步骤如下:
步骤①:称取样品1.000g。
步骤②:将样品溶解后完全转移到250mL容量瓶中,定容,充分摇匀。
步骤③:移取25.00mL样品溶液于250mL锥形瓶中,用0.01mol·L-1KMnO4标准溶液滴定至终点。
按上述操作方法再重复2次。
(1)写出步骤③所发生反应的离子方程式:
(2)判断滴定终点的现象是
(3)在配制0.01mol·L-1KMnO4溶液定容时若仰视,则最终测得变质固体中X的含量
(4)滴定结果如表所示:
| 滴定次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 2.20 | 20.20 |
您最近一年使用:0次
4 . 下列实验操作及现象,能推出相应结论的是
| 选项 | 实验操作及现象 | 结论 |
| A | 常温下,用pH计测得0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH,前者大 | 酸性:CH3COOH>HClO |
| B | 向淀粉溶液中加入稀硫酸并加热,再加入银氨溶液,水浴加热,未见有银镜产生 | 淀粉没有水解 |
| C | 向MgCl2溶液中滴加足量NaOH溶液,有白色沉淀生成;再滴加CuCl2溶液,有蓝色沉淀生成 | Ksp[Cu(OH)2]<Ksp[Mg(OH)2] |
| D | 向Fe(NO3)2样品,溶于稀硫酸,滴加KSCN溶液,溶液变红 | Fe(NO3)2样品溶于稀硫酸前已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-03-15更新
|
404次组卷
|
3卷引用:青海省西宁市2018届高三下学期复习检测一(一模)理综化学试题
解题方法
5 . 钠、铝、铁是三种重要的金属。
(1)将一小块金属钠投入水中,反应的离子方程式为___________ ;钠能与冷水剧烈反应而铁不能,证明金属活动性:钠___________ 铁(填“>”或“<”)。
(2)实验室常用Al2(SO4)3与氨水反应制备氢氧化铝,反应的离子方程式为___________
(3)某补铁剂(有效成分为FeSO4)因长期放置被氧化而失效,为检验其氧化产物(Fe3+),同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入___________ ,出现血红色溶液,证明氧化产物为Fe3+。
②乙同学另取少许溶液,加入淀粉-KI溶液,溶液变为___________ 色,证明氧化产物为Fe3+,该反应的离子方程式为___________ (已知:淀粉遇I2变蓝)。
(1)将一小块金属钠投入水中,反应的离子方程式为
(2)实验室常用Al2(SO4)3与氨水反应制备氢氧化铝,反应的离子方程式为
(3)某补铁剂(有效成分为FeSO4)因长期放置被氧化而失效,为检验其氧化产物(Fe3+),同学们取上述样品制成溶液进行如下实验。
①甲同学取少许溶液,加入
②乙同学另取少许溶液,加入淀粉-KI溶液,溶液变为
您最近一年使用:0次
名校
6 . 高锰酸钾是一种常见的氧化剂,工业上碱熔法利用软锰矿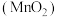 制备高锰酸钾的流程如下。某化学活动小组在实验室中模拟该流程制备高锰酸钾,并对产物中
制备高锰酸钾的流程如下。某化学活动小组在实验室中模拟该流程制备高锰酸钾,并对产物中 的质量分数进行测定。
的质量分数进行测定。
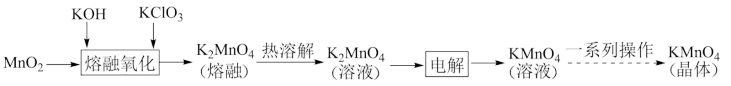
(1)“熔融氧化”步骤在坩埚中进行,则选用坩埚的材料为___________(填序号)。
(2)工业上电解制取 溶液时,生成的
溶液时,生成的___________ (填化学式)经回收可以返名回“熔融氧化”步骤循环利用。
(3)由 溶液获得
溶液获得 晶体的一系列操作为
晶体的一系列操作为___________ 、___________ 、过滤、洗涤、干燥。
(4)按下述步骤测定产物中 的质量分数:
的质量分数:
a.用分析天平准确称取 样品1.0000g,配制成250mL溶液;
样品1.0000g,配制成250mL溶液;
b.用分析天平准确称取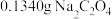 ,加入500mL的锥形瓶中,用100mL蒸馏水溶解,再加入
,加入500mL的锥形瓶中,用100mL蒸馏水溶解,再加入 硫酸10mL,加热到70~80℃;
硫酸10mL,加热到70~80℃;
c.趁热用高锰酸钾溶液进行滴定;
d.重复步骤b、c三次测定数据如下表,并进行数据处理。
①配制 样品溶液时,下列玻璃仪器中不需要的有
样品溶液时,下列玻璃仪器中不需要的有___________ (填序号)。
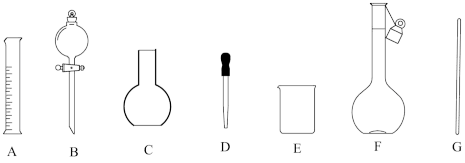
②步骤b适宜选用的加热方式为___________ ,需趁热滴定是因为反应在常温下进行较慢,一般要求滴定结束时不低于60℃,但也不能温度过高,防止 部分分解导致测定结果
部分分解导致测定结果___________ (填“偏高”或“偏低”)。
③滴定终点现象为___________ ;产物中 的质量分数为
的质量分数为___________ 。
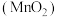 制备高锰酸钾的流程如下。某化学活动小组在实验室中模拟该流程制备高锰酸钾,并对产物中
制备高锰酸钾的流程如下。某化学活动小组在实验室中模拟该流程制备高锰酸钾,并对产物中 的质量分数进行测定。
的质量分数进行测定。
(1)“熔融氧化”步骤在坩埚中进行,则选用坩埚的材料为___________(填序号)。
| A.陶瓷 | B.石英 | C.铁 | D.刚玉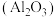 |
 溶液时,生成的
溶液时,生成的(3)由
 溶液获得
溶液获得 晶体的一系列操作为
晶体的一系列操作为(4)按下述步骤测定产物中
 的质量分数:
的质量分数:a.用分析天平准确称取
 样品1.0000g,配制成250mL溶液;
样品1.0000g,配制成250mL溶液;b.用分析天平准确称取
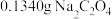 ,加入500mL的锥形瓶中,用100mL蒸馏水溶解,再加入
,加入500mL的锥形瓶中,用100mL蒸馏水溶解,再加入 硫酸10mL,加热到70~80℃;
硫酸10mL,加热到70~80℃;c.趁热用高锰酸钾溶液进行滴定;
d.重复步骤b、c三次测定数据如下表,并进行数据处理。
| 实验序号 | 1 | 2 | 3 |
消耗 样品溶液体积/mL 样品溶液体积/mL | 25.10 | 24.80 | 25.10 |
①配制
 样品溶液时,下列玻璃仪器中不需要的有
样品溶液时,下列玻璃仪器中不需要的有
②步骤b适宜选用的加热方式为
 部分分解导致测定结果
部分分解导致测定结果③滴定终点现象为
 的质量分数为
的质量分数为
您最近一年使用:0次
2022-01-09更新
|
128次组卷
|
2卷引用:青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题
7 . 电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置.
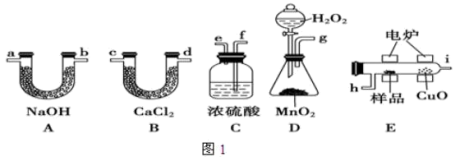
(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是__________________
(2)C装置中浓硫酸的作用是________________ .
(3)D装置中MnO2的作用是________________________ .
(4)燃烧管中CuO的作用是________________ .
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为______ .
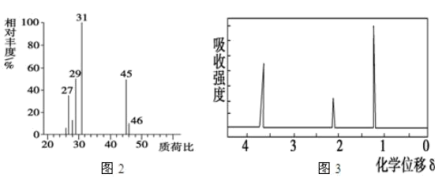
(6)用质谱仪测定其相对分子质量,得如图二所示的质谱图,则该有机物的相对分子质量为____ .
(7)能否根据A的实验式确定A的分子式________ (填“能”或“不能”),若能,则A的分子式是______ (若不能,则此空不填).
(8)该物质的核磁共振氢谱如图三所示,则其结构简式为________ .


(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是
(2)C装置中浓硫酸的作用是
(3)D装置中MnO2的作用是
(4)燃烧管中CuO的作用是
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为
(6)用质谱仪测定其相对分子质量,得如图二所示的质谱图,则该有机物的相对分子质量为
(7)能否根据A的实验式确定A的分子式
(8)该物质的核磁共振氢谱如图三所示,则其结构简式为
您最近一年使用:0次
2016-12-09更新
|
176次组卷
|
2卷引用:2015-2016学年青海西宁第四高级中学高二下期末化学卷



