KI可用作制有机化合物及制药原料,医疗上用于防治甲状腺肿和甲状腺功能亢进的手术前准备所需药物,也可用作祛痰药。某实验小组设计制备一定量KI的实验(加热及夹持装置已省略)如下:
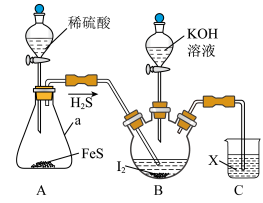
(1)实验开始前,先进行的操作为_______ 。
(2)仪器a的名称是_______ 。
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是_______ 。
(4)久置KI溶液易被氧化而导致变质,实验小组取久置KI溶液进行实验,如图所示。
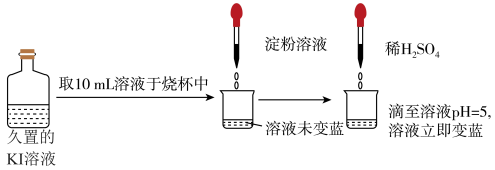
关于溶液立即变蓝的原因,该实验小组进行了如下探究,请将空格补充完整:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ.KI溶液久置过程中产生了 ;
; 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。
②实验与结论
(5)测定KI的纯度:称取0.5000g样品溶于水,加入稍过量硫酸酸化的H2O2充分反应后,加热除去过量H2O2,加入几滴淀粉溶液,用0.2000mol·L-1的Na2S2O3标准溶液滴定( )。
)。
①滴定前装有标准液的滴定管排气泡时,应选择图中的_______ (填标号,下同)。
a.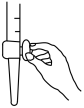 b.
b.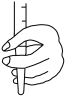 c.
c.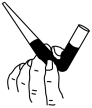 d.
d.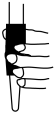
②若用25.00ml的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积_______ 。
a.=10.00mL b.=15.00mL c.<10.00mL d.>15.00mL
③滴定终点时消耗14.50mL标准溶液,则样品的纯度为_______ (计算结果保留两位有效数字)。

(1)实验开始前,先进行的操作为
(2)仪器a的名称是
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是
(4)久置KI溶液易被氧化而导致变质,实验小组取久置KI溶液进行实验,如图所示。

关于溶液立即变蓝的原因,该实验小组进行了如下探究,请将空格补充完整:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ.KI溶液久置过程中产生了
 ;
; 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。②实验与结论
| 实验编号 | 实验方案 | 实验现象 | 结论与解释 |
| ⅰ | 往试管中加入10mL0.1mol·L-1新制KI溶液并加入几滴淀粉溶液, | 50min后溶液变蓝 | 猜想Ⅰ不成立 |
| ⅱ | 取少量KIO3溶液与少量KI溶液混合,加入淀粉溶液,再滴加稀H2SO4调节pH至5 | 溶液立即变蓝 | 猜想Ⅱ成立。写出相关反应的离子方程式 |
 )。
)。①滴定前装有标准液的滴定管排气泡时,应选择图中的
a.
 b.
b. c.
c. d.
d.
②若用25.00ml的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
a.=10.00mL b.=15.00mL c.<10.00mL d.>15.00mL
③滴定终点时消耗14.50mL标准溶液,则样品的纯度为
更新时间:2023-09-09 22:05:19
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究小组用如图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8 ℃,沸点是44.8 ℃。
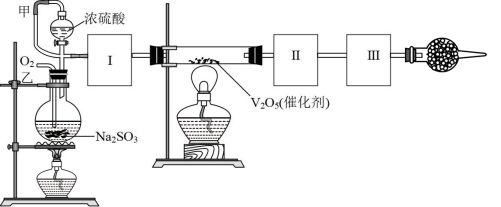
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ 处连接合适的装置。请从如图A~E装置中选择最适合装置并将其序号填入下面的空格中。Ⅰ、Ⅱ、Ⅲ 处连接的装置分别是_______ 、_________ 、___________ 。
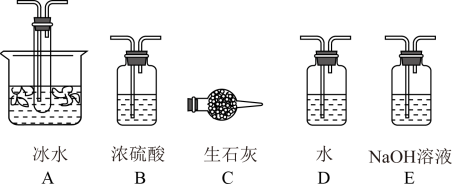
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是________ 。
(3)实验中发现SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,分析可能的原因并说明相应的验证方法(写2点)。
①原因______ ,验证方法________ 。
②原因______ ,验证方法________ 。
(4)尾端球形干燥管的作用是________ 。
(5)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了b g,则实验中SO2的转化率为______ %(用含a、b的代数式表示)。

(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ 处连接合适的装置。请从如图A~E装置中选择最适合装置并将其序号填入下面的空格中。Ⅰ、Ⅱ、Ⅲ 处连接的装置分别是

(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是
(3)实验中发现SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,分析可能的原因并说明相应的验证方法(写2点)。
①原因
②原因
(4)尾端球形干燥管的作用是
(5)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了b g,则实验中SO2的转化率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】焦亚硫酸钠(Na2S2O5)可用作食品的抗氧化剂。查阅资料知:焦亚硫酸钠露置空气中易氧化成硫酸钠,与强酸接触放出二氧化硫而生成相应的盐类。请回答下列问题:
(1)Na2S2O5中S的化合价为_______ 。
(2)配制Na2S2O5溶液所需要的蒸馏水必须经过煮沸、冷却后才能使用,目的是______ 。
(3)葡萄酒常用Na2S2O5作抗氧化剂,可用碘标准液测定其残留量。在测定某葡萄酒中Na2S2O5残留量时,取20.00 mL样品于锥形瓶,滴加几滴淀粉溶液,用0.01000 mol/L碘标准液滴定至终点,数据如表:
①滴定过程中Na2S2O5与碘标准液反应的离子方程式_________ 。
②判断到达滴定终点的标准是_______ 。
③计算该葡萄酒样品中Na2S2O5残留量_________ g/L(以SO2计)。
(4)试设计检验Na2S2O5晶体在空气中已被氧化的实验方案_________ 。
(1)Na2S2O5中S的化合价为
(2)配制Na2S2O5溶液所需要的蒸馏水必须经过煮沸、冷却后才能使用,目的是
(3)葡萄酒常用Na2S2O5作抗氧化剂,可用碘标准液测定其残留量。在测定某葡萄酒中Na2S2O5残留量时,取20.00 mL样品于锥形瓶,滴加几滴淀粉溶液,用0.01000 mol/L碘标准液滴定至终点,数据如表:
| 滴定次数 | 第一次 | 第二次 | 第三次 | |
| 待测液体积/mL | 20.00 | 20.00 | 20.00 | |
| 碘标准液读数/mL | 滴定前 | 0.40 | 2.00 | 3.10 |
| 滴定后 | 10.30 | 13.10 | 13.20 | |
①滴定过程中Na2S2O5与碘标准液反应的离子方程式
②判断到达滴定终点的标准是
③计算该葡萄酒样品中Na2S2O5残留量
(4)试设计检验Na2S2O5晶体在空气中已被氧化的实验方案
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】水合肼 的制备方法有多种,实验室以
的制备方法有多种,实验室以 、NaOH和尿素
、NaOH和尿素 为原料制备,也可以利用电解法制备。再用水合肼处理铜氨溶液并制得铜粉,其实验过程可表示为:
为原料制备,也可以利用电解法制备。再用水合肼处理铜氨溶液并制得铜粉,其实验过程可表示为:
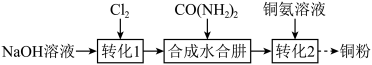
已知: 沸点约118℃,具有强还原性。
沸点约118℃,具有强还原性。
(1)“合成水合肼”用如图所示装置。仪器A的名称是_______ ,仪器A中反应的离子方程式是_______ 。
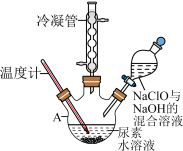
(2)若滴加NaClO与NaOH的混合溶液的速度较快,水合肼的产率会下降,原因是_______ 。
(3)某实验室设计了如图所示装置制备 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
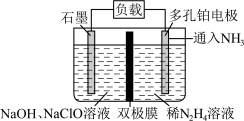
①双极膜中产生的_______ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②石墨电极反应方程式为_______ 。
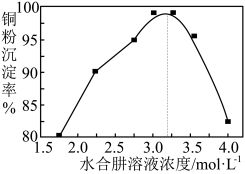
(4)已知: 。铜粉沉淀率与水合肼溶液初始浓度的关系如图所示。请设计由铜氨溶液[主要含有
。铜粉沉淀率与水合肼溶液初始浓度的关系如图所示。请设计由铜氨溶液[主要含有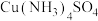 ]回收铜粉的实验方案:取一定体积
]回收铜粉的实验方案:取一定体积 水合肼溶液,
水合肼溶液,_______ ,静置、过滤、洗涤、干燥。(须使用的试剂: 硫酸、NaOH固体、铜氨溶液、蒸馏水)
硫酸、NaOH固体、铜氨溶液、蒸馏水)
 的制备方法有多种,实验室以
的制备方法有多种,实验室以 、NaOH和尿素
、NaOH和尿素 为原料制备,也可以利用电解法制备。再用水合肼处理铜氨溶液并制得铜粉,其实验过程可表示为:
为原料制备,也可以利用电解法制备。再用水合肼处理铜氨溶液并制得铜粉,其实验过程可表示为:
已知:
 沸点约118℃,具有强还原性。
沸点约118℃,具有强还原性。(1)“合成水合肼”用如图所示装置。仪器A的名称是

(2)若滴加NaClO与NaOH的混合溶液的速度较快,水合肼的产率会下降,原因是
(3)某实验室设计了如图所示装置制备
 。双极膜是阴、阳复合膜,层间的
。双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②石墨电极反应方程式为
(4)已知:
 。铜粉沉淀率与水合肼溶液初始浓度的关系如图所示。请设计由铜氨溶液[主要含有
。铜粉沉淀率与水合肼溶液初始浓度的关系如图所示。请设计由铜氨溶液[主要含有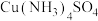 ]回收铜粉的实验方案:取一定体积
]回收铜粉的实验方案:取一定体积 水合肼溶液,
水合肼溶液, 硫酸、NaOH固体、铜氨溶液、蒸馏水)
硫酸、NaOH固体、铜氨溶液、蒸馏水)
您最近一年使用:0次



