名校
解题方法
1 . 碘化亚铜(CuI)是重要的有机催化剂。某学习小组用如图装置制备CuI,并设计实验探究其性质.已知:碘化亚铜(CuI)是白色固体,难溶于水,易与浓度较大的KI溶液形成 ,实验装置如图1所示。
,实验装置如图1所示。

(1)仪器D的名称是__________________ 。
(2)实验完毕后,用图2所示装置分离CuI的突出优点是__________________ 。
(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是__________________ 。
(4)装置B中发生反应的离子方程式是___________________________ 。
(5)小组同学设计下表方案对CuI的性质进行探究:
①在实验I中“加水,又生成白色沉淀”的原理是___________________________ 。
②根据实验Ⅱ,CuI与NaOH溶液反应的化学方程式是___________________________ 。
(6)测定 CuI样品纯度:取ag CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用bmol∙L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为VmL[已知:滴定反应为 。该样品纯度为
。该样品纯度为_________ (用含a、b、V的代数式表示)。如果其他操作均正确,若选用的Na2S2O3标准液部分被氧化变质,测得结果_________ (填“偏高”“偏低”或“无影响”)。
 ,实验装置如图1所示。
,实验装置如图1所示。
图1 图2
(1)仪器D的名称是
(2)实验完毕后,用图2所示装置分离CuI的突出优点是
(3)某同学向装置C的烧杯中倾倒NaOH溶液时,不慎将少量溶液溅到皮肤上,处理的方法是
(4)装置B中发生反应的离子方程式是
(5)小组同学设计下表方案对CuI的性质进行探究:
实验 | 实验操作及现象 |
I | 取少量CuI放入试管中,加入KI浓溶液,白色固体溶解得到无色溶液;加水,又生成白色沉淀 |
Ⅱ | 取少量CuI放入试管中,加入NaOH溶液,振荡,产生砖红色沉淀,过滤,向所得上层清液中滴加淀粉溶液,无明显变化:将砖红色沉淀溶于稀硫酸,产生红色固体和蓝色溶液 |
②根据实验Ⅱ,CuI与NaOH溶液反应的化学方程式是
(6)测定 CuI样品纯度:取ag CuI样品与适量NaOH溶液充分反应后,过滤;在滤液中加入足量的酸化的双氧水,滴几滴淀粉溶液,用bmol∙L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3溶液体积为VmL[已知:滴定反应为
 。该样品纯度为
。该样品纯度为
您最近一年使用:0次
解题方法
2 . 下列实验方案、现象和结论均正确的是
| 选项 | 实验方案 | 现象 | 结论 |
| A | 取两份新制氯水,分别滴加AgNO3溶液和淀粉KI溶液 | 前者有白色沉淀,后者溶液变蓝 | 氯气与水反应存在限度 |
| B | 向稀硫酸中加入铜粉,再加入少量KNO3固体 | 开始无明显现象,加入KNO3后,溶液变蓝 | KNO3起催化作用 |
| C | 取少量Na2SO3样品溶于蒸馏水,滴加足量稀盐酸,再加入足量BaCl2溶液 | 有白色沉淀生成 | 样品已经变质 |
| D | 向浓度均为0.1mol·L-1的NaCl和Na2CO3溶液中分别滴加酚酞 | 前者不变色,后者变红 | 非金属性:C<Cl |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-16更新
|
105次组卷
|
2卷引用:重庆市康德2024年普通高中学业水平选择性考试高三下学期高考模拟调研卷(三)化学试题
3 . 下列方案设计、现象和结论均正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 鉴定某涂改液中是否存在含氯化合物 | 涂改液与KOH溶液混合加热,充分反应,取上层清液,加入足量稀硝酸,最后滴加硝酸银溶液 | 出现白色沉淀,说明涂改液中存在含氯化合物 |
| B | 证明非金属性 | 向装有FeS固体的试管中滴加稀盐酸 | 固体溶解,生成臭鸡蛋气味气体,证明非金属性 |
| C | 检验乙醇中是否混有乙醛 | 取待测液,滴加酸性高锰酸钾溶液 | 高锰酸钾溶液褪色,证明乙醇中混有乙醛 |
| D | 检验 样品是否变质 样品是否变质 | 将 样品溶于稀 样品溶于稀 ,滴加KSCN溶液 ,滴加KSCN溶液 | 观察到溶液变红,证明样品已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . KI可用作制有机化合物及制药原料,医疗上用于防治甲状腺肿和甲状腺功能亢进的手术前准备所需药物,也可用作祛痰药。某实验小组设计制备一定量KI的实验(加热及夹持装置已省略)如下:
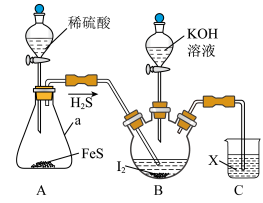
(1)实验开始前,先进行的操作为_______ 。
(2)仪器a的名称是_______ 。
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是_______ 。
(4)久置KI溶液易被氧化而导致变质,实验小组取久置KI溶液进行实验,如图所示。
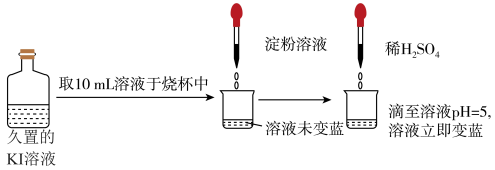
关于溶液立即变蓝的原因,该实验小组进行了如下探究,请将空格补充完整:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ.KI溶液久置过程中产生了 ;
; 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。
②实验与结论
(5)测定KI的纯度:称取0.5000g样品溶于水,加入稍过量硫酸酸化的H2O2充分反应后,加热除去过量H2O2,加入几滴淀粉溶液,用0.2000mol·L-1的Na2S2O3标准溶液滴定( )。
)。
①滴定前装有标准液的滴定管排气泡时,应选择图中的_______ (填标号,下同)。
a.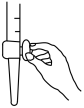 b.
b.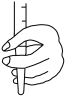 c.
c.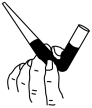 d.
d.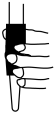
②若用25.00ml的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积_______ 。
a.=10.00mL b.=15.00mL c.<10.00mL d.>15.00mL
③滴定终点时消耗14.50mL标准溶液,则样品的纯度为_______ (计算结果保留两位有效数字)。

(1)实验开始前,先进行的操作为
(2)仪器a的名称是
(3)实验中不能用稀硝酸代替稀硫酸的根本原因是
(4)久置KI溶液易被氧化而导致变质,实验小组取久置KI溶液进行实验,如图所示。

关于溶液立即变蓝的原因,该实验小组进行了如下探究,请将空格补充完整:
①提出猜想
猜想Ⅰ.酸性条件下,空气中的O2将I-迅速氧化成I2;
猜想Ⅱ.KI溶液久置过程中产生了
 ;
; 在酸性条件下与I-反应生成I2。
在酸性条件下与I-反应生成I2。②实验与结论
| 实验编号 | 实验方案 | 实验现象 | 结论与解释 |
| ⅰ | 往试管中加入10mL0.1mol·L-1新制KI溶液并加入几滴淀粉溶液, | 50min后溶液变蓝 | 猜想Ⅰ不成立 |
| ⅱ | 取少量KIO3溶液与少量KI溶液混合,加入淀粉溶液,再滴加稀H2SO4调节pH至5 | 溶液立即变蓝 | 猜想Ⅱ成立。写出相关反应的离子方程式 |
 )。
)。①滴定前装有标准液的滴定管排气泡时,应选择图中的
a.
 b.
b. c.
c. d.
d.
②若用25.00ml的滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积
a.=10.00mL b.=15.00mL c.<10.00mL d.>15.00mL
③滴定终点时消耗14.50mL标准溶液,则样品的纯度为
您最近一年使用:0次
2023-09-09更新
|
148次组卷
|
4卷引用:重庆市2023-2024学年高三上学期9月联考化学试题
名校
解题方法
5 . 下列实验方案设计、现象与结论均正确的是
选项 | 目的 | 方案设计 | 现象与结论 |
A | 比较B元素和C元素的非金属性强弱 | 向 硼酸溶液中加入 硼酸溶液中加入 碳酸氢钠溶液 碳酸氢钠溶液 | 若无明显变化,说明非金属性: |
B | 检验 固体是否变质 固体是否变质 | 取少量固体溶于水,滴加少量 ,再滴入KSCN溶液,振荡,观察溶液颜色变化 ,再滴入KSCN溶液,振荡,观察溶液颜色变化 | 若溶液变红,说明样品已变质 |
C | 证明蔗糖是否水解 | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 悬浊液 悬浊液 | 若无砖红色沉淀,说明蔗糖未发生水解 |
D | 探究不同价态硫元素之间的转化 | 向 和 和 混合溶液中,加入大量浓硫酸 混合溶液中,加入大量浓硫酸 | 若溶液中出现淡黄色沉淀,则说明 价和 价和 价硫可归中 价硫可归中 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列实验方案能达到实验目的的是
选项 | 实验目的 | 实验方案 |
| A | 证明 沉淀可以转化为 沉淀可以转化为 | 向 溶液中先加入2滴 溶液中先加入2滴 溶液,再加入2滴 溶液,再加入2滴 溶液 溶液 |
| B | 证明 溶液中存在水解平衡 溶液中存在水解平衡 | 向滴有酚酞的 溶液中加入少量 溶液中加入少量 固体,溶液红色稍微变浅 固体,溶液红色稍微变浅 |
| C | 检验 晶体是否已氧化变质 晶体是否已氧化变质 | 将 样品溶于稀盐酸后,滴加 样品溶于稀盐酸后,滴加 溶液,观察溶液是否变红 溶液,观察溶液是否变红 |
| D | 比较 和 和 的酸性强弱 的酸性强弱 | 常温下,用pH试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的pH 溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 某课外活动小组探究某食品包装袋中还原性铁粉是否变质,分别取少量样品溶于盐酸,然后进行下列实验。下列说法正确的是
A.若滴加 溶液,无红褐色沉淀产生,说明铁粉未变质 溶液,无红褐色沉淀产生,说明铁粉未变质 |
B.若滴加 溶液,溶液变红,说明铁粉变质 溶液,溶液变红,说明铁粉变质 |
C.若先滴加氯水,再滴加 溶液,溶液变红,说明铁粉全部变质 溶液,溶液变红,说明铁粉全部变质 |
D.若滴加 溶液,无白色沉淀产生,说明铁粉全部变质 溶液,无白色沉淀产生,说明铁粉全部变质 |
您最近一年使用:0次
2023-02-11更新
|
356次组卷
|
3卷引用:重庆市南开中学校2022-2023学年高一上学期期末联合检测化学试题
重庆市南开中学校2022-2023学年高一上学期期末联合检测化学试题(已下线)第14讲 铁的氢氧化物和铁盐、亚铁盐-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)云南省普洱市西盟佤族自治县第一中学2022-2023学年高一下学期4月月考化学试题
8 . 下图的实验装置可用于研究SO2转化为SO3的转化率。
已知:SO3的熔点是16.8℃,沸点是44.8℃。

完成下列填空:
(1)A装置中发生的化学反应方程式为_______ 。
(2)根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:_______ ,E:_______ 。
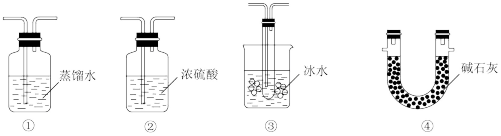
装置F的作用为_______ 。
(3)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重b g,则此时SO2的转化率为_______ (用含a、b的代数式表示)。
(4)现欲检验Na2SO3样品在空气中是否变质,其方法是_______ 。(简述实验操作及现象)
(5)实验结束后,不慎将收集了SO3的装置露置于空气中,可观察到装置出口处产生大量白雾,简述其原因_______ 。
已知:SO3的熔点是16.8℃,沸点是44.8℃。

完成下列填空:
(1)A装置中发生的化学反应方程式为
(2)根据实验需要,应该在D、E处连接合适的装置。请从下图中选择,将所选装置的序号填入相应的空格,D:

装置F的作用为
(3)用a mol Na2SO3粉末与足量浓硫酸进行此实验,当A处反应结束时,再继续通入一段时间O2,最后测得E处装置增重b g,则此时SO2的转化率为
(4)现欲检验Na2SO3样品在空气中是否变质,其方法是
(5)实验结束后,不慎将收集了SO3的装置露置于空气中,可观察到装置出口处产生大量白雾,简述其原因
您最近一年使用:0次
解题方法
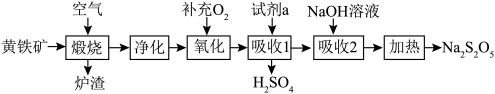
9 . 硫酸的消耗量是衡量一个国家化学工业发展水平的标志。以黄铁矿(主要成分为 )为原料生产
)为原料生产 和
和 。
。
(1) 中铁元素的化合价为
中铁元素的化合价为___________ ;试剂a为___________ 。
(2)若要增大煅烧过程的反应速率,应采取的措施是___________ (写两条即可)。
(3)煅烧时主要反应的化学方程式为___________ 。
(4)“氧化”时,反应的化学方程式为___________ 。
(5) 可用于葡萄酒的抗氧化剂,用碘标准液可以测定葡萄酒中
可用于葡萄酒的抗氧化剂,用碘标准液可以测定葡萄酒中 的含量。请配平其反应的化学方程式:
的含量。请配平其反应的化学方程式:_________
______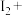 _______
_______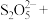 _______
_______ ________
________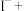 ______
______ ___________
___________
若要检验 是否变质生成了
是否变质生成了 ,所用的试剂是
,所用的试剂是___________ 。
(6)在测定某葡萄酒中 的含量时,取
的含量时,取 葡萄酒样品,消耗
葡萄酒样品,消耗 碘标准液
碘标准液 。样品中
。样品中 的含量为
的含量为___________  。
。
 )为原料生产
)为原料生产 和
和 。
。
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)若要增大煅烧过程的反应速率,应采取的措施是
(3)煅烧时主要反应的化学方程式为
(4)“氧化”时,反应的化学方程式为
(5)
 可用于葡萄酒的抗氧化剂,用碘标准液可以测定葡萄酒中
可用于葡萄酒的抗氧化剂,用碘标准液可以测定葡萄酒中 的含量。请配平其反应的化学方程式:
的含量。请配平其反应的化学方程式:______
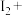 _______
_______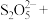 _______
_______ ________
________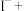 ______
______ ___________
___________
若要检验
 是否变质生成了
是否变质生成了 ,所用的试剂是
,所用的试剂是(6)在测定某葡萄酒中
 的含量时,取
的含量时,取 葡萄酒样品,消耗
葡萄酒样品,消耗 碘标准液
碘标准液 。样品中
。样品中 的含量为
的含量为 。
。
您最近一年使用:0次
10 . 由下列实验操作和现象所得结论均正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 将亚硫酸钠样品溶于水,加入盐酸酸化的Ba(NO3)2溶液有白色沉淀产生 | 样品已变质 |
| B | 将盐酸滴入某溶液,产生能使澄清石灰水变浑浊的气体 | 溶液中有 |
| C | 铁投入冷的浓硝酸中无明显现象,投入稀硝酸中有气泡冒出 | 氧化性:稀硝酸>浓硝酸 |
| D | 向Na2SO3溶液中滴入稀盐酸,产生刺激性气味的气体可使品红溶液褪色 | 酸性:HCl>H2SO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-09更新
|
212次组卷
|
3卷引用:重庆市两江中学校2021-2022学年高一下学期第一次月考化学试题



