名校
1 . X、Y、Z、W为原子半径依次增大的短周期p区元素,由四种元素形成的微粒Q可作为绿色催化剂和溶剂离子液体的阴离子,Q的结构如图所示下列说法正确的是

A.氢化物的沸点: |
B.电负性: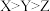 |
| C.W的氧化物对应的水化物属于强酸 |
| D.该阴离子中Y不满足8电子稳定结构 |
您最近一年使用:0次
名校
解题方法
2 . 某高分子化合物M常用于制作眼镜镜片,可由N和P两种物质合成,M、N、P的结构如图所示,下列说法正确的是
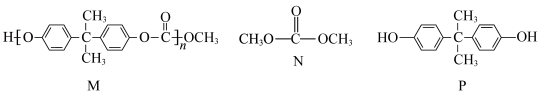
| A.N与P合成M的反应为加聚反应 | B.M的链节中在同一平面的碳原子最多有14个 |
| C.P在空气中很稳定,可以保存在广口瓶中 | D.常温下,M、N、P均易溶于水 |
您最近一年使用:0次
7日内更新
|
353次组卷
|
4卷引用:2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学
名校
3 . 已知 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法错误 的是
 为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL
为拟卤素,性质与卤素类似。老师将学生分为四组,做如下探究实验:甲组:分别配制500mL KSCN溶液、
KSCN溶液、 溶液;乙组:向
溶液;乙组:向 的KSCN溶液中滴加酸性
的KSCN溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丙组:向
溶液褪色;丙组:向 的
的 溶液中滴加酸性
溶液中滴加酸性 溶液,酸性
溶液,酸性 溶液褪色;丁组:分别取50mL
溶液褪色;丁组:分别取50mL KSCN溶液和50mL
KSCN溶液和50mL
 溶液,混合,向混合液中滴加酸性
溶液,混合,向混合液中滴加酸性 溶液,溶液先变红后褪色,下列说法
溶液,溶液先变红后褪色,下列说法| A.甲组同学用到500mL容量瓶、玻璃棒、烧杯、胶头滴管等玻璃仪器 |
B.乙组实验中 将 将 氧化为 氧化为 |
C.丙组实验发生反应的离子方程式: |
D.丁组实验说明还原性: |
您最近一年使用:0次
7日内更新
|
252次组卷
|
6卷引用:2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学
2024届山西省晋中市和诚高中高三下学期理综冲刺卷(二)-高中化学河北省2024届高三下学期普通高中学业水平选择性考试化学冲刺卷(二)河南省许昌高级中学2023-2024学年高三下学期5月月考化学试题2024届吉林省通化市梅河口市第五中学高三下学期三模化学试题(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)山东省烟台市龙口第一中学东校2023-2024学年高二下学期6月月考化学试题
解题方法
4 . 下列根据实验操作及现象不能达到相应实验目的的是
| 选项 | 实验操作及现象 | 实验目的 |
| A | 向滴有几滴 的 的 溶液中加入 溶液中加入 ,缓缓通入少量 ,缓缓通入少量 并振荡、静置,水层显红色,有机层显无色 并振荡、静置,水层显红色,有机层显无色 | 验证还原性: |
| B | 相同温度下,同时进行 与 与 和 和 的反应,观察产生 的反应,观察产生 的快慢 的快慢 | 探究 键的极性对反应速率的影响 键的极性对反应速率的影响 |
| C | 将胆矾晶体投入浓硫酸中,固体由蓝色变为白色 | 验证浓硫酸具有脱水性 |
| D | 分别测定 和 和 与盐酸反应的反应热 与盐酸反应的反应热 | 确定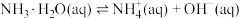 的 的 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 儿茶酸具有抗菌、抗氧化作用,常用于治疗烧伤、小儿肺炎等疾病,可采用如图所示路线合成。下列说法正确的是
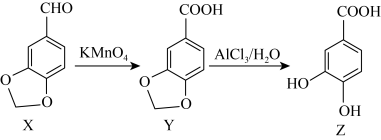
| A.Y存在二元芳香酸的同分异构体 | B.可用酸性 溶液鉴别X和Z 溶液鉴别X和Z |
| C.X分子中所有原子可能共平面 | D.Z与足量的溴水反应消耗 |
您最近一年使用:0次
7日内更新
|
259次组卷
|
7卷引用:2024届山西省晋城市第一中学校高三下学期模拟预测理综试题-高中化学
2024届山西省晋城市第一中学校高三下学期模拟预测理综试题-高中化学广东省茂名市高州市2024届高三下学期高考适应性考试(三模)化学试题(已下线)山东省青岛市2023-2024学年高三下学期第三次模拟考试化学试题2024届河南省南阳市第一中学校高三下学期高考冲刺押题卷(二)理科综合试题-高中化学2024届陕西省安康市高新中学、安康中学高新分校高三下学期5月模拟考试理综试题-高中化学河北省衡水市部分示范性高中2024届高三下学期三模化学试题(已下线)选择题6-10
名校
解题方法
6 . 近期我国科学家报道了一种低成本高储能液流电池,其工作原理如下图。下列说法中错误的是
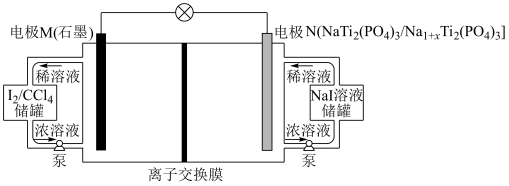
| A.电极M为正极 |
| B.离子交换膜应选用阳离子交换膜 |
C.电极N上发生反应的电极反应为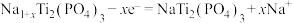 |
D.理论上N电极质量减少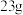 ,电路中转移的电子数目为 ,电路中转移的电子数目为 |
您最近一年使用:0次
2024-06-12更新
|
134次组卷
|
2卷引用:2024届山西省晋城市第一中学校高三下学期模拟预测理综试题-高中化学
名校
解题方法
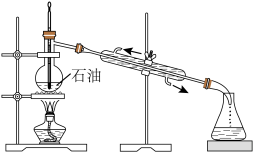
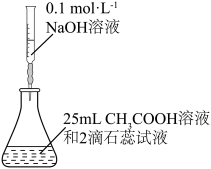
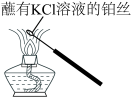
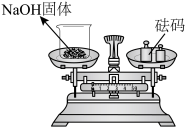
7 . 化学实验操作是进行科学实验的基础。下列操作合理的是
|
|
| A.石油分馏 | B.用NaOH标准溶液滴定未知浓度的 溶液 溶液 |
|
|
| C.观察K元素的焰色 | D.称量NaOH固体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-12更新
|
177次组卷
|
7卷引用:2024届山西省晋城市第一中学校高三下学期模拟预测理综试题-高中化学
解题方法
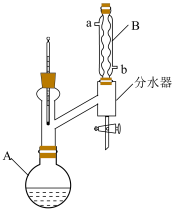
8 . 乙酸正丁酯是优良的有机溶剂,在石油加工、制药工程等领域均有广泛应用。在实验室中,乙酸正丁酯可通过正丁醇和冰醋酸在强酸催化及加热条件下合成,实验装置如图所示。反应中生成的水可以与正丁醇或乙酸正丁酯形成共沸混合物被蒸出。使用分水器可在反应进行的同时分离出生成的水,并使有机相流回反应瓶中。实验步骤如下:
②关闭分水器旋塞,并在分水器带旋塞的一侧预先加入适量的水,再向反应装置中依次加入5mL(55mmol)正丁醇、3.4mL(60mmol)冰醋酸和0.05mL浓硫酸,加入一粒沸石。
③将反应液温度控制在T1℃并保持15分钟,然后升温至回流状态。当___________,停止加热。将分水器中的液体导入分液漏斗中,将水层分出。
④依次用5mL水、5mL10%碳酸钠溶液、5mL水洗涤有机层。
⑤有机层用无水硫酸镁干燥。常压蒸馏,在T2℃时收集馏分。
已知各化合物及相关共沸物在常压下的沸点如下表所示:
回答下列问题:
(1)仪器A的名称为___________ ;仪器B中进水口为___________ (填“a”或“b”)。
(2)正丁醇的密度为___________ g·cm-3。
(3)步骤③中停止加热的标志是___________ 。
(4)T1和T2的范围分别是___________ (填标号)。
a.T1>90℃,T2>120℃ b.T1>90℃,T2<12℃
c.T1<90℃,T2>120℃ d.T1<90℃,T2<120℃
(5)冰醋酸略过量的原因是___________ ,若最终得到产品的质量为5.12g,测得纯度为98%,则反应的产率为___________ (结果保留一位小数)。
(6)步骤③中,有一处操作明显错误使得产率降低,正确做法是___________ 。
②关闭分水器旋塞,并在分水器带旋塞的一侧预先加入适量的水,再向反应装置中依次加入5mL(55mmol)正丁醇、3.4mL(60mmol)冰醋酸和0.05mL浓硫酸,加入一粒沸石。
③将反应液温度控制在T1℃并保持15分钟,然后升温至回流状态。当___________,停止加热。将分水器中的液体导入分液漏斗中,将水层分出。
④依次用5mL水、5mL10%碳酸钠溶液、5mL水洗涤有机层。
⑤有机层用无水硫酸镁干燥。常压蒸馏,在T2℃时收集馏分。
已知各化合物及相关共沸物在常压下的沸点如下表所示:
| 化合物 | 乙酸 | 正丁醇 | 乙酸丁酯醋 |
| 沸点 | 117.9℃ | 117.3℃ | 126.6℃ |
| 共沸物 | 正丁醇—水 | 乙酸正丁酯—水 | 乙酸正丁酯—正丁醇—水 |
| 沸点 | 92.7℃ | 90.7℃ | 90.7℃ |
(1)仪器A的名称为
(2)正丁醇的密度为
(3)步骤③中停止加热的标志是
(4)T1和T2的范围分别是
a.T1>90℃,T2>120℃ b.T1>90℃,T2<12℃
c.T1<90℃,T2>120℃ d.T1<90℃,T2<120℃
(5)冰醋酸略过量的原因是
(6)步骤③中,有一处操作明显错误使得产率降低,正确做法是
您最近一年使用:0次
解题方法
9 . 锂离子电池是新能源重要组成部分,废旧锂电池的回收利用意义重大。某研究小组对废弃的锂电池正极材料LiCoO2进行氯化处理以回收Li、Co等金属,工艺流程如下:
(1)已知Co的原子序数为27,则其在元素周期表中的位置是___________ 。
(2)已知“烧渣”是LiCl、CoCl2和SiO2的混合物,则“500℃焙烧”反应生成的氧化产物与还原产物的物质的量之比为___________ ;滤饼2成分的化学式为___________ 。
(3)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入Na2CO3,将温度升至90℃是为了提高沉淀反应速率和___________ 。得到碳酸锂沉淀的操作为___________ (填标号)。
b.加热后,趁热过滤
c.蒸发浓缩、冷却结晶
(4)取100mL滤液2,其中c(Li+)=0.10mol·L-1,为使锂元素的回收率不低于80%,则至少应加入Na2CO3固体的物质的量为___________ mol[已知Ksp(Li2CO3)=3.6×10-4,忽略溶液体积变化]。
(5)将碳酸锂(Li2CO3)与CoCO3按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为___________ 。
(6)钴的某种氧化物的晶胞结构如图所示,该立方晶胞参数为apm。___________ 。
②设阿伏加德罗常数的值为NA,则该晶胞的密度为___________ g·cm-3。

(1)已知Co的原子序数为27,则其在元素周期表中的位置是
(2)已知“烧渣”是LiCl、CoCl2和SiO2的混合物,则“500℃焙烧”反应生成的氧化产物与还原产物的物质的量之比为
(3)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入Na2CO3,将温度升至90℃是为了提高沉淀反应速率和
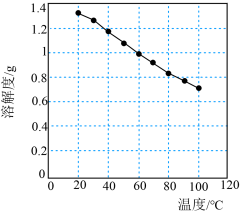
b.加热后,趁热过滤
c.蒸发浓缩、冷却结晶
(4)取100mL滤液2,其中c(Li+)=0.10mol·L-1,为使锂元素的回收率不低于80%,则至少应加入Na2CO3固体的物质的量为
(5)将碳酸锂(Li2CO3)与CoCO3按n(Li):n(Co)=1:1的比例配合,然后在空气中于700℃烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为
(6)钴的某种氧化物的晶胞结构如图所示,该立方晶胞参数为apm。
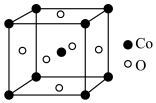
②设阿伏加德罗常数的值为NA,则该晶胞的密度为
您最近一年使用:0次
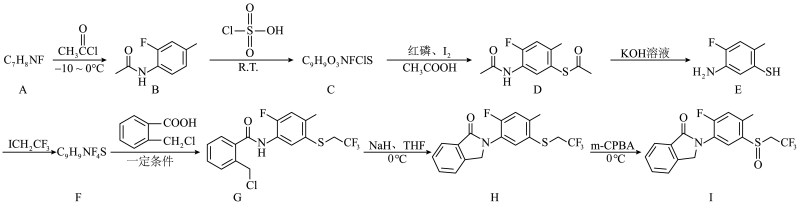
10 . 高活性杀螨剂(化合物Ⅰ)的合成路线如下:
(1)B的分子式为___________ ,H中含氧官能团的名称为___________ 。
(2)B→C反应的另一种产物为___________ ,E→F的反应类型为___________ 。
(3)A的结构简式是___________ 。
(4)F→G的化学方程式为___________ 。
(5)化合物B的同分异构体中满足下列条件的有___________ 种(不考虑立体异构);其中核磁共振氢谱有5组峰且峰面积之比为3:2:2:2:1的结构简式为___________ 。
①苯环上含有两个取代基且能发生银镜反应;
②分子中含有-NH2且-NH2与苯环直接相连。
(1)B的分子式为
(2)B→C反应的另一种产物为
(3)A的结构简式是
(4)F→G的化学方程式为
(5)化合物B的同分异构体中满足下列条件的有
①苯环上含有两个取代基且能发生银镜反应;
②分子中含有-NH2且-NH2与苯环直接相连。
您最近一年使用:0次