1 . 雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺技术是国内外研究的热点。研究表明,氮氧化物 和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。
和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。 溶液中的离子浓度由大到小顺序是
溶液中的离子浓度由大到小顺序是___________ 。
(2)①已知: 生成
生成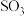 总反应的化学方程式是
总反应的化学方程式是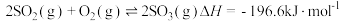 ,此反应可通过如下两步完成:
,此反应可通过如下两步完成: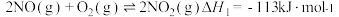 ;
;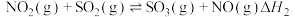 。则
。则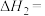
___________ 。
②一定温度下,向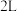 恒容密闭容器中充入
恒容密闭容器中充入 和
和 各
各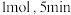 达到平衡,此时容器中
达到平衡,此时容器中 和
和 的浓度之比为
的浓度之比为 ,则
,则 的平衡转化率是
的平衡转化率是___________ 。
(3) 属于酸性氧化物,将其通入
属于酸性氧化物,将其通入 溶液中,得到
溶液中,得到 溶液。
溶液。
① 溶液呈酸性,其原因是
溶液呈酸性,其原因是___________ 。
②向 的
的 溶液中滴加一定浓度的
溶液中滴加一定浓度的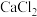 溶液,溶液中出现浑浊,
溶液,溶液中出现浑浊, 降为2,用化学平衡移动原理解释溶液
降为2,用化学平衡移动原理解释溶液 降低的原因:
降低的原因:___________ 。
(4)通过 传感器可监测
传感器可监测 的含量,其工作原理示意图如图。
的含量,其工作原理示意图如图。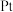 电极上发生的是
电极上发生的是___________ (填“氧化”或“还原”)反应。
②写出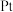 电极的电极反应式:
电极的电极反应式:___________ 。
③写出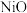 电极的电极反应式:
电极的电极反应式:___________ 。
 和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。
和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。
 溶液中的离子浓度由大到小顺序是
溶液中的离子浓度由大到小顺序是(2)①已知:
 生成
生成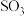 总反应的化学方程式是
总反应的化学方程式是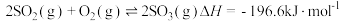 ,此反应可通过如下两步完成:
,此反应可通过如下两步完成: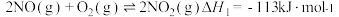 ;
;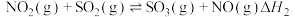 。则
。则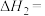
②一定温度下,向
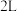 恒容密闭容器中充入
恒容密闭容器中充入 和
和 各
各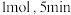 达到平衡,此时容器中
达到平衡,此时容器中 和
和 的浓度之比为
的浓度之比为 ,则
,则 的平衡转化率是
的平衡转化率是(3)
 属于酸性氧化物,将其通入
属于酸性氧化物,将其通入 溶液中,得到
溶液中,得到 溶液。
溶液。①
 溶液呈酸性,其原因是
溶液呈酸性,其原因是②向
 的
的 溶液中滴加一定浓度的
溶液中滴加一定浓度的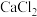 溶液,溶液中出现浑浊,
溶液,溶液中出现浑浊, 降为2,用化学平衡移动原理解释溶液
降为2,用化学平衡移动原理解释溶液 降低的原因:
降低的原因:(4)通过
 传感器可监测
传感器可监测 的含量,其工作原理示意图如图。
的含量,其工作原理示意图如图。
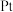 电极上发生的是
电极上发生的是②写出
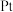 电极的电极反应式:
电极的电极反应式:③写出
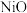 电极的电极反应式:
电极的电极反应式:
您最近一年使用:0次
2 . 某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣(已除去葡萄糖溶液过滤得到的),对甘蔗渣进行综合利用不仅可以提高经济效益,而且还能防止环境污染。生产流程如图所示。 的产量可以用来衡量一个国家石油化学工业的发展水平,
的产量可以用来衡量一个国家石油化学工业的发展水平, 的分子中含有醛基,
的分子中含有醛基, 是具有香味的液体。完成下列各题。
是具有香味的液体。完成下列各题。
(1)A的名称为___________ ; 的名称为
的名称为___________ 。
(2)B的结构简式为___________ ; 的结构简式为
的结构简式为___________ , 的官能团名称为
的官能团名称为___________ 。
(3)写出 的化学方程式:
的化学方程式:___________ 。
(4)写出 的化学方程式:
的化学方程式:___________ 。
(5)写出 的同分异构体中与
的同分异构体中与 互为同系物的结构简式:
互为同系物的结构简式:___________ 。

 的产量可以用来衡量一个国家石油化学工业的发展水平,
的产量可以用来衡量一个国家石油化学工业的发展水平, 的分子中含有醛基,
的分子中含有醛基, 是具有香味的液体。完成下列各题。
是具有香味的液体。完成下列各题。(1)A的名称为
 的名称为
的名称为(2)B的结构简式为
 的结构简式为
的结构简式为 的官能团名称为
的官能团名称为(3)写出
 的化学方程式:
的化学方程式:(4)写出
 的化学方程式:
的化学方程式:(5)写出
 的同分异构体中与
的同分异构体中与 互为同系物的结构简式:
互为同系物的结构简式:
您最近一年使用:0次
3 . 铁元素在细菌的作用下可发生如图所示的转化。下列说法中正确的是

| A.反硝化过程均属于氮的固定 |
| B.硝化过程中,含氮物质均发生还原反应 |
C. 将 将 转化为 转化为 的离子方程式为 的离子方程式为 |
D.在氨氧化细菌作用下,水体中的铵态氮和硝态氮可转移到大气中,该反应中每产生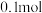 氮气时转移 氮气时转移 电子 电子 |
您最近一年使用:0次
4 . 下列有关化学反应速率的说法正确的是
A.用铁片与稀硫酸反应制取氢气时,改用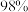 的浓硫酸可增大产生氢气的速率 的浓硫酸可增大产生氢气的速率 |
B. 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 |
C. 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 |
D.汽车尾气中的 与 与 可以缓慢反应生成 可以缓慢反应生成 和 和 ,增大压强,化学反应速率增大 ,增大压强,化学反应速率增大 |
您最近一年使用:0次
5 . 下列分离、提纯、鉴别物质的方法错误的是
A.用丁达尔效应鉴别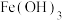 胶体和 胶体和 溶液 溶液 |
B.用溶解、过滤的方法除去 中的 中的 |
C.用加热方法除去 中的 中的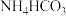 |
D.用加热、蒸发的方法除去粗盐中的 杂质 杂质 |
您最近一年使用:0次
6 . I.化学小组的同学用10mol/L的浓硫酸配制100mL物质的量浓度为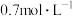 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。
(1)需要量取________ mL上述浓硫酸进行配制。
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是________ 。
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是________ (填序号)。
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为________ 。
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是________ ;产生该现象原因是________________ (用化学方程式解释)。
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是________ 。
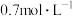 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。(1)需要量取
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是
您最近一年使用:0次
7 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是________ 。
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为________ 。
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为________ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是________ (填化学式,用“>”连接)。
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为________ 。
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是________ 。

(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是
您最近一年使用:0次
解题方法
8 . 表示下列反应的离子方程式正确的是
A.铁跟稀硫酸反应: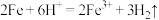 |
B.NaHCO3溶液和NaOH溶液反应: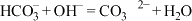 |
C.氢氧化钡溶液和稀硫酸反应: |
D.向澄清石灰水中通入少量CO2: |
您最近一年使用:0次
解题方法
9 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
| A.Fe2O3(Al2O3):加入足量NaOH溶液,过滤 |
| B.NaHCO3溶液(Na2CO3):通入足量的CO2 |
| C.FeCl3溶液(FeCl2):通入足量的氯气 |
| D.CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
10 . 回答下列问题
(1) 中氮元素的化合价为
中氮元素的化合价为___________ 价。
(2)已知 能发生反应:
能发生反应: 。用单线桥法表示该反应中电子转移情况
。用单线桥法表示该反应中电子转移情况___________ 。
(1)
 中氮元素的化合价为
中氮元素的化合价为(2)已知
 能发生反应:
能发生反应: 。用单线桥法表示该反应中电子转移情况
。用单线桥法表示该反应中电子转移情况
您最近一年使用:0次



