名校
1 . 碳酸钠是造纸、玻璃、纺织等行业的重要原料。工业碳酸钠(纯度约为98%)中含有少量 、
、 、
、 和
和 等杂质,提纯的工艺流程如下:
等杂质,提纯的工艺流程如下: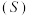 随温度变化的曲线如图所示。
随温度变化的曲线如图所示。
(1)设计实验方案,验证工业碳酸钠中含有杂质 ,写出该方案的操作和现象:
,写出该方案的操作和现象:_____ 。
(2)“滤渣”的主要成分为_______ (写化学式)。
(3)实验室进行“蒸发浓缩结晶”用到的主要仪器有蒸发皿、酒精灯、_______ 等。
(4)“趁热过滤”的目的是_______ 。
(5)若“母液”多次循环使用,可能导致的问题是_______ 。
(6)“加热脱水”属于_______ 变化(填“物理”或“化学”)。
(7)“检验”制备的试剂级碳酸钠纯度,设计如下实验方案:取 产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到
产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到 固体,则产品中
固体,则产品中 的质量分数为
的质量分数为_______ (用含 、
、 的式子表示)。
的式子表示)。
(8)实验室探究 和
和 的热稳定性,设计了如图装置。大试管中应盛放的固体是
的热稳定性,设计了如图装置。大试管中应盛放的固体是_______ ,理由是_______ 。
 、
、 、
、 和
和 等杂质,提纯的工艺流程如下:
等杂质,提纯的工艺流程如下:
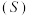 随温度变化的曲线如图所示。
随温度变化的曲线如图所示。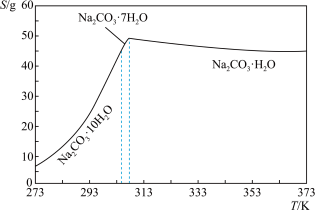
(1)设计实验方案,验证工业碳酸钠中含有杂质
 ,写出该方案的操作和现象:
,写出该方案的操作和现象:(2)“滤渣”的主要成分为
(3)实验室进行“蒸发浓缩结晶”用到的主要仪器有蒸发皿、酒精灯、
(4)“趁热过滤”的目的是
(5)若“母液”多次循环使用,可能导致的问题是
(6)“加热脱水”属于
(7)“检验”制备的试剂级碳酸钠纯度,设计如下实验方案:取
 产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到
产品,将其投入到过量的稀硫酸中,将产生的气体通入到足量的澄清石灰水中,经过滤、洗涤、干燥,得到 固体,则产品中
固体,则产品中 的质量分数为
的质量分数为 、
、 的式子表示)。
的式子表示)。(8)实验室探究
 和
和 的热稳定性,设计了如图装置。大试管中应盛放的固体是
的热稳定性,设计了如图装置。大试管中应盛放的固体是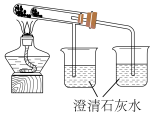
您最近一年使用:0次
名校
2 . Ⅰ.在10L的密闭容器中,进行如下化学反应: 。其化学平衡常数K和温度t的关系如下表:
。其化学平衡常数K和温度t的关系如下表:
请回答:
(1)该反应为_______ (填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为
_______ 。保持温度和体积不变,充入一定量的CO2,则平衡常数_______ (填“增大”“减小”“不变”)
(3)能说明该反应达到化学平衡状态的是_______ (填字母)。
A.一定温度下容器中压强不变
B.混合气体中c(CO)不变
C.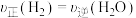
D.
E.氢气转化率不变
(4)下列措施可以提高H2的平衡转化率的是_______(填字母)
(5)某温度下,平衡浓度符合下式: ,试判断此时的温度为
,试判断此时的温度为_______ ℃。
(6)800℃,某时刻测得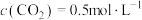 ,
,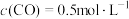 ,
,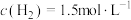 ,
,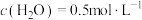 ,则此时反应是否达到平衡状态
,则此时反应是否达到平衡状态_______ (填“是”“否”)。此时,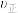
_______  (填“<”“>”“=”)。
(填“<”“>”“=”)。
Ⅱ.一定温度下,在容积固定的VL密闭容器里加入1molA、2molB、2molC,发生反应: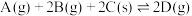
 。
。
(7)在保证A浓度不变的情况下,增大容器的体积,平衡_______ (填字母)
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(8)若该反应的逆反应速率与时间的关系如图所示:_______ ;t4时_______ ;
②t2时平衡向_______ (填“正反应”或“逆反应”)方向移动。
③反应过程中,转化率最大的时刻点为_______ (填“t1”或“t3”或“t5”)。
 。其化学平衡常数K和温度t的关系如下表:
。其化学平衡常数K和温度t的关系如下表: | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应为
(2)该反应的化学平衡常数表达式为

(3)能说明该反应达到化学平衡状态的是
A.一定温度下容器中压强不变
B.混合气体中c(CO)不变
C.
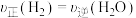
D.

E.氢气转化率不变
(4)下列措施可以提高H2的平衡转化率的是_______(填字母)
| A.选择适当的催化剂 | B.增大压强 | C.及时分离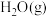 | D.升高温度 |
(5)某温度下,平衡浓度符合下式:
 ,试判断此时的温度为
,试判断此时的温度为(6)800℃,某时刻测得
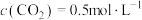 ,
,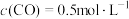 ,
,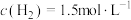 ,
,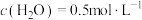 ,则此时反应是否达到平衡状态
,则此时反应是否达到平衡状态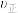
 (填“<”“>”“=”)。
(填“<”“>”“=”)。Ⅱ.一定温度下,在容积固定的VL密闭容器里加入1molA、2molB、2molC,发生反应:
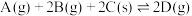
 。
。(7)在保证A浓度不变的情况下,增大容器的体积,平衡
A.向正反应方向移动 B.向逆反应方向移动 C.不移动
(8)若该反应的逆反应速率与时间的关系如图所示:
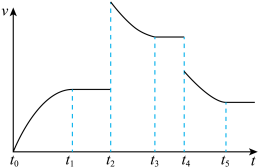
②t2时平衡向
③反应过程中,转化率最大的时刻点为
您最近一年使用:0次
名校
解题方法
3 . 回答下列问题:
(1)已知:CO分子结构为 。在一定条件下可实现反应:
。在一定条件下可实现反应:
 。已知部分化学键键能数据如下,则
。已知部分化学键键能数据如下,则
_______ 。
本反应的催化原理分为两步,第一步为吸热的慢反应,第二步为放热的快反应。能正确表示催化反应原理的能量变化示意图为_______ 。(选填字母)

已知下列反应:
已知:
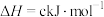 。则
。则
_______  。
。
(3) 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
(ⅰ)直接氯化:
 ,
,
(ⅱ)碳氯化: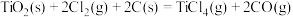
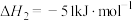 ,
,
①反应 的
的 为
为_______  ,
,
_______ (用含 和
和 的式子表示)。
的式子表示)。
②已知:C的燃烧热为 ,则CO的燃烧热为
,则CO的燃烧热为_______  。
。
(1)已知:CO分子结构为
 。在一定条件下可实现反应:
。在一定条件下可实现反应:
 。已知部分化学键键能数据如下,则
。已知部分化学键键能数据如下,则
| 化学键 |  |  |  |  |
键能 | 436 | 803 | 1076 | 465 |
A. 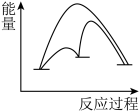 B.
B. 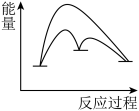 C.
C.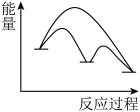 D.
D.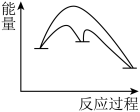


已知下列反应:
| 可燃物 |  |  |
燃烧热 | a | b |

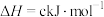 。则
。则
 。
。(3)
 转化为
转化为 有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:
有直接氯化法和碳氯化法。在1000℃时反应的热化学方程式及其平衡常数如下:(ⅰ)直接氯化:

 ,
,
(ⅱ)碳氯化:
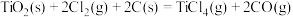
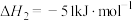 ,
,
①反应
 的
的 为
为 ,
,
 和
和 的式子表示)。
的式子表示)。②已知:C的燃烧热为
 ,则CO的燃烧热为
,则CO的燃烧热为 。
。
您最近一年使用:0次
名校
解题方法
4 . 按要求回答问题。
Ⅰ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。_______ 。
(2)取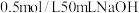 溶液和
溶液和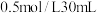 硫酸溶液进行实验,实验数据如表。已知:假设盐酸和氢氧化钠溶液的密度都是
硫酸溶液进行实验,实验数据如表。已知:假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容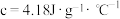
①请填写表中的空白:
②通过上述实验测得中和热数值为_______  (保留一位小数)。此结果与
(保留一位小数)。此结果与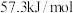 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是_______ (填字母)。
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时,俯视容量瓶刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时,倒出溶液后用少量水洗涤量筒,将洗涤液再倒入装置中
Ⅱ.某探究性学习实验小组做了如下实验:利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。
(3)通过实验A、B,可探究_______ 的改变对反应速度的影响,其中
_______ ,
_______ ;通过实验_______ 可探究出温度变化对化学反应速度的影响。
(4)对照实验A和B,时间t1的范围为:t1_______ 8(填“<”“>”“=”);利用实验B中数据计算,用KMnO4的浓度变化表示的反应速率为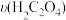 =
=_______  。
。
Ⅰ.中和热的测定:
测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。
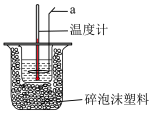
(2)取
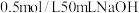 溶液和
溶液和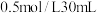 硫酸溶液进行实验,实验数据如表。已知:假设盐酸和氢氧化钠溶液的密度都是
硫酸溶液进行实验,实验数据如表。已知:假设盐酸和氢氧化钠溶液的密度都是 ,又知中和反应后生成溶液的比热容
,又知中和反应后生成溶液的比热容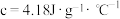
①请填写表中的空白:
| 温度实验次数 | 起始温度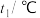 | 终止温度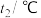 | 温度差平均值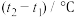 | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | ① |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 (保留一位小数)。此结果与
(保留一位小数)。此结果与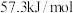 有偏差,产生偏差的原因可能是
有偏差,产生偏差的原因可能是a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液时,俯视容量瓶刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时,倒出溶液后用少量水洗涤量筒,将洗涤液再倒入装置中
Ⅱ.某探究性学习实验小组做了如下实验:利用H2C2O4溶液和酸性KMnO4溶液之间的反应来探究外界条件改变对化学反应速率的影响。
| 实验序号 | 实验温度/K | KMnO4溶液(硫酸酸化) | H2C2O4溶液 | H2O | 溶液颜色褪至无色时所需时间 | ||
 | 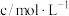 |  | 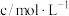 |  | |||
| A | 293 | 2 | 0.02 | 5 | 0.1 | 3 | t1 |
| B |  | 2 | 0.02 | 3 | 0.1 | 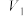 | 8 |
| C | 313 | 2 | 0.02 | 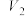 | 0.1 | 5 | t2 |
(3)通过实验A、B,可探究


(4)对照实验A和B,时间t1的范围为:t1
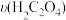 =
= 。
。
您最近一年使用:0次
名校
解题方法
5 . 某温度下,在2L密闭容器中投入一定量的A、B发生反应: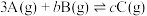
 。12s时反应达到平衡,反应初始与平衡时的压强比为13:9,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
。12s时反应达到平衡,反应初始与平衡时的压强比为13:9,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
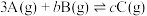
 。12s时反应达到平衡,反应初始与平衡时的压强比为13:9,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是
。12s时反应达到平衡,反应初始与平衡时的压强比为13:9,反应过程中A、B的物质的量浓度随时间的变化关系如图所示。下列说法正确的是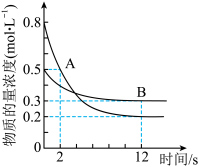
A.前12s内,A的平均反应速率为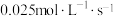 |
| B.12s后,A的消耗速率等于B的生成速率 |
C.化学计量数之比 |
D.12s内,A和B反应放出的热量为 |
您最近一年使用:0次
名校
6 . 向容积为1L的密闭容器中通入一定量N2O4和NO2的混合气体,发生反应
 。体系中各物质浓度随时间的变化如图所示。
。体系中各物质浓度随时间的变化如图所示。

 。体系中各物质浓度随时间的变化如图所示。
。体系中各物质浓度随时间的变化如图所示。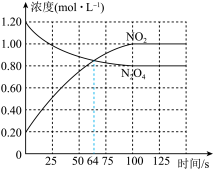
| A.64s时,反应达到化学平衡状态 |
| B.平衡后,压缩体积,增大压强,平衡逆移,混合气体的颜色逐渐变深 |
| C.平衡后,增大N2O4的浓度,平衡正向移动,K值增大 |
| D.若该容器为绝热体系,前50s内,体系温度逐渐降低,平衡逆移 |
您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的有几个
①其他条件不变,温度越高,化学反应速率越快,反应现象越明显
②其他条件不变,升高温度,能增大反应物分子中活化分子的百分数,则速率增大
③如果活化分子百分数未变,但增加单位体积内活化分子数,可以使有效碰撞次数增多,则速率增大
④增大反应物浓度,可增大活化分子的百分数,从而使单位时间内有效碰撞次数增多,则速率增大
⑤有气体参加的化学反应,若增大压强,可增加活化分子数目,则速率增大
⑥如果使反应物分子的能量增加,则活化分子的百分数增大,有效碰撞次数增多,则速率增大
⑦如果使用催化剂,可使反应活化能降低,活化分子的百分数增大,则速率增大
①其他条件不变,温度越高,化学反应速率越快,反应现象越明显
②其他条件不变,升高温度,能增大反应物分子中活化分子的百分数,则速率增大
③如果活化分子百分数未变,但增加单位体积内活化分子数,可以使有效碰撞次数增多,则速率增大
④增大反应物浓度,可增大活化分子的百分数,从而使单位时间内有效碰撞次数增多,则速率增大
⑤有气体参加的化学反应,若增大压强,可增加活化分子数目,则速率增大
⑥如果使反应物分子的能量增加,则活化分子的百分数增大,有效碰撞次数增多,则速率增大
⑦如果使用催化剂,可使反应活化能降低,活化分子的百分数增大,则速率增大
| A.3个 | B.4个 | C.5个 | D.6个 |
您最近一年使用:0次
名校
解题方法
8 . 下列说法正确的是
A.31g白磷固体比31g红磷固体能量多bkJ,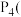 白磷,s 白磷,s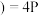 (红磷,s) (红磷,s) 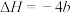  ,所以白磷比红磷稳定 ,所以白磷比红磷稳定 |
B.500℃、30MPa下,  ;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ ;将1.5molH2和过量的N2在此条件下充分反应,放出热量46.2kJ |
C.H2的燃烧热为 ,则 ,则 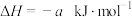 |
D.稀氢氟酸溶液与稀氢氧化钠溶液反应生成1mol水时的反应热大于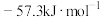 |
您最近一年使用:0次
名校
解题方法
9 . 关于能量的说法正确的是
| A.水变成水蒸气时吸收的能量就是该过程的反应热 |
B.可逆反应的 与反应进行的程度有关 与反应进行的程度有关 |
| C.放热反应在任何条件下都可以发生,吸热反应不加热就不能发生 |
| D.等压条件下进行的化学反应的反应热等于反应的焓变 |
您最近一年使用:0次
名校
解题方法
10 . 某研究小组利用下图所示装置制备氯气并进行卤素性质的探究。回答下列问题:
I.制备 并进行性质实验(夹持装置和加热仪器略)
并进行性质实验(夹持装置和加热仪器略) 与浓盐酸反应制取
与浓盐酸反应制取 ,反应的化学方程式为
,反应的化学方程式为_______ 。
(2)B中发生反应的离子方程式为_______ 。
(3)装置D的作用是_______ 。
(4)取一支试管,加入2mLC中橙黄色溶液,再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,_______ (填“能”或“不能”)得出结论: 的氧化性强于
的氧化性强于 ,理由是
,理由是_______ 。
Ⅱ.研究小组为了验证 和
和 能否将
能否将 氧化为
氧化为 ,设计如下实验:
,设计如下实验:
(5)同学甲认为实验ⅰ的现象说明溴水能将 氧化;同学乙认为仅从“溶液为黄色”不能得出“溴水能将
氧化;同学乙认为仅从“溶液为黄色”不能得出“溴水能将 氧化”的结论,黄色可能是溴水溶于水溶液形成的颜色。同学乙补充了实验方案,证明了“溴水能将
氧化”的结论,黄色可能是溴水溶于水溶液形成的颜色。同学乙补充了实验方案,证明了“溴水能将 氧化”。同学乙补充的实验方案是:
氧化”。同学乙补充的实验方案是:_______ 。
(6)分析上述实验,判断 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是_______ 。
I.制备
 并进行性质实验(夹持装置和加热仪器略)
并进行性质实验(夹持装置和加热仪器略)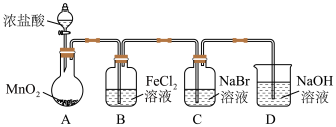
 与浓盐酸反应制取
与浓盐酸反应制取 ,反应的化学方程式为
,反应的化学方程式为(2)B中发生反应的离子方程式为
(3)装置D的作用是
(4)取一支试管,加入2mLC中橙黄色溶液,再滴入几滴淀粉KI溶液,观察到溶液变为蓝色。通过以上实验,
 的氧化性强于
的氧化性强于 ,理由是
,理由是Ⅱ.研究小组为了验证
 和
和 能否将
能否将 氧化为
氧化为 ,设计如下实验:
,设计如下实验:| 实验 | 操作 | 现象 |
| ⅰ | 先向试管中加入 溶液和0.5mL苯(浮于液面上),将胶头滴管伸入下层溶液中,滴加少量稀溴水 溶液和0.5mL苯(浮于液面上),将胶头滴管伸入下层溶液中,滴加少量稀溴水 | 下层溶液为黄色 |
| ⅱ | 先向试管中加入 溶液和0.5mL苯(浮于液面上),将胶头滴管伸入下层溶液中,滴加0.5mL稀碘水 溶液和0.5mL苯(浮于液面上),将胶头滴管伸入下层溶液中,滴加0.5mL稀碘水 | 下层溶液为黄色 |
| 再滴加0.5mLKSCN溶液于下层溶液中 | 无红色出现 |
(5)同学甲认为实验ⅰ的现象说明溴水能将
 氧化;同学乙认为仅从“溶液为黄色”不能得出“溴水能将
氧化;同学乙认为仅从“溶液为黄色”不能得出“溴水能将 氧化”的结论,黄色可能是溴水溶于水溶液形成的颜色。同学乙补充了实验方案,证明了“溴水能将
氧化”的结论,黄色可能是溴水溶于水溶液形成的颜色。同学乙补充了实验方案,证明了“溴水能将 氧化”。同学乙补充的实验方案是:
氧化”。同学乙补充的实验方案是:(6)分析上述实验,判断
 、
、 、
、 的氧化性由强到弱的顺序是
的氧化性由强到弱的顺序是
您最近一年使用:0次



