1 . I.化学小组的同学用10mol/L的浓硫酸配制100mL物质的量浓度为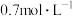 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。
(1)需要量取________ mL上述浓硫酸进行配制。
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是________ 。
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是________ (填序号)。
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为________ 。
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是________ ;产生该现象原因是________________ (用化学方程式解释)。
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是________ 。
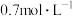 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。(1)需要量取
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是
您最近一年使用:0次
2 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是________ 。
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为________ 。
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为________ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是________ (填化学式,用“>”连接)。
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为________ 。
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是________ 。

(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是
您最近一年使用:0次
解题方法
3 . 表示下列反应的离子方程式正确的是
A.铁跟稀硫酸反应: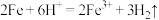 |
B.NaHCO3溶液和NaOH溶液反应: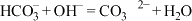 |
C.氢氧化钡溶液和稀硫酸反应: |
D.向澄清石灰水中通入少量CO2: |
您最近一年使用:0次
解题方法
4 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
| A.Fe2O3(Al2O3):加入足量NaOH溶液,过滤 |
| B.NaHCO3溶液(Na2CO3):通入足量的CO2 |
| C.FeCl3溶液(FeCl2):通入足量的氯气 |
| D.CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
5 . 樱黄素(乙)具有抗过敏、抗炎、抗肿瘤和保护心脑血管等多方面生物活性。以金雀异黄酮(甲)为原料,经碘甲烷甲基化合成樱黄素的反应如下,下列说法正确的是

| A.甲、乙所含官能团种类不相同 |
B.乙分子中所有原子杂化类型均为 |
C.一定条件下,甲与足量的 加成产物的分子中有8个手性碳原子 加成产物的分子中有8个手性碳原子 |
D.甲、乙既能与 溶液反应,又能与 溶液反应,又能与 溶液反应 溶液反应 |
您最近一年使用:0次
6 . 某研究性学习小组用如图所示的装置进行实验,探究原电池、电解池和电解精炼钴的工作原理。一段时间后装置甲的两极均有气体产生,且X极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。请根据实验现象及所查资料,回答下列问题:
查阅资料:高铁酸根( )在溶液中呈紫红色。
)在溶液中呈紫红色。
(2)装置丙中,若外电路中有0.2 mol电子转移,则有___________ mol  透过隔膜,隔膜右侧溶液质量如何变化:
透过隔膜,隔膜右侧溶液质量如何变化:___________ 。
(3)反应过程中,X极处发生的电极反应为 和
和___________ 。
(4)一段时间后,若X极质量减小1.12 g,Y极收集到2.24 L气体,则在X极收集到的气体为___________ mL(均已折算为标准状况时的气体体积)。
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中
___________ (填“变大”“变小”或“不变”),该电解池总反应的化学方程式是___________ 。
(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除O2外,还可能有___________ 。
查阅资料:高铁酸根(
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
| A.X(Fe) | B.Y(C) | C.Co | D.Zn |
(2)装置丙中,若外电路中有0.2 mol电子转移,则有
 透过隔膜,隔膜右侧溶液质量如何变化:
透过隔膜,隔膜右侧溶液质量如何变化:(3)反应过程中,X极处发生的电极反应为
 和
和(4)一段时间后,若X极质量减小1.12 g,Y极收集到2.24 L气体,则在X极收集到的气体为
(5)乙池是电解制备金属钴的装置图,理论上Ⅰ室中

(6)若撤掉装置乙中的阳离子交换膜,石墨电极上产生的气体除O2外,还可能有
您最近一年使用:0次
7 . 水溶液中的离子反应与平衡是化学反应原理的重要组成部分,回答下列问题:
(1)常温下,pH均为5的NH4Cl溶液与稀硫酸中,水电离出的 浓度之比约为
浓度之比约为___________ 。
(2)将FeCl3溶液加热,溶液pH___________ (填“增大”“不变”或“减小”)。
(3)已知:25℃时,H3PO3的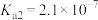 ,H3PO3溶液与过量的NaOH溶液反应生成Na2HPO3,则H3PO3为
,H3PO3溶液与过量的NaOH溶液反应生成Na2HPO3,则H3PO3为___________ 元酸; 的NaH2PO3溶液显
的NaH2PO3溶液显___________ (填“酸”“中”或“碱”)性,在该溶液中存在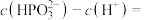
___________ 。
(4)某学习小组用“间接碘量法”测定含有 晶体的试样(不含能与
晶体的试样(不含能与 发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用
发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。已知:
Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。已知: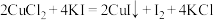 ,
, 。
。
①可选用___________ 作滴定指示剂,滴定终点的现象是___________ 。
②该试样中 的质量分数为
的质量分数为___________ 。
(1)常温下,pH均为5的NH4Cl溶液与稀硫酸中,水电离出的
 浓度之比约为
浓度之比约为(2)将FeCl3溶液加热,溶液pH
(3)已知:25℃时,H3PO3的
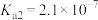 ,H3PO3溶液与过量的NaOH溶液反应生成Na2HPO3,则H3PO3为
,H3PO3溶液与过量的NaOH溶液反应生成Na2HPO3,则H3PO3为 的NaH2PO3溶液显
的NaH2PO3溶液显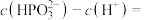
(4)某学习小组用“间接碘量法”测定含有
 晶体的试样(不含能与
晶体的试样(不含能与 发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用
发生反应的氧化性杂质)的纯度,过程如下:取0.36 g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用 Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。已知:
Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00 mL。已知: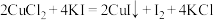 ,
, 。
。①可选用
②该试样中
 的质量分数为
的质量分数为
您最近一年使用:0次
8 . 根据要求回答下列问题。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ 。
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①与铁同周期元素中,4s轨道半充满的元素为___________ (填元素符号)。
② 、
、 、
、 、
、 的半径由大到小的顺序为
的半径由大到小的顺序为___________ 。
③由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出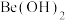 与NaOH反应的化学方程式:
与NaOH反应的化学方程式:___________ 。
(3)我国科研人员研制出了M-LiH(M为Fe、Mn、Sc等金属)等催化剂,使得合成氨工业的温度、压强分别降到了350℃、1 MPa,这是近年来合成氨反应研究中的重要突破。
①已知元素呈气态时,从它的阳离子中将一个电子移至无穷远处时所需做的功,称为该元素的电离势,单位为电子伏特(eV)。Sc的三种气态离子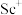 、
、 、
、 的电离势分别为6.54 eV、12.80 eV、24.76 eV,上述三种气态离子的电离势依次增大的原因为
的电离势分别为6.54 eV、12.80 eV、24.76 eV,上述三种气态离子的电离势依次增大的原因为___________ 。
②第三电离能
___________ (填“>”或“<”) ,原因是
,原因是___________ 。
(1)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
(2)铁触媒是普遍使用的以铁为主体的多成分催化剂,通常还含有Al2O3、K2O、CaO、MgO、Cr2O3等氧化物中的几种。
①与铁同周期元素中,4s轨道半充满的元素为
②
 、
、 、
、 、
、 的半径由大到小的顺序为
的半径由大到小的顺序为③由于Be与Al处于对角线位置,性质具有相似性,根据“对角线规则”,写出
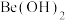 与NaOH反应的化学方程式:
与NaOH反应的化学方程式:(3)我国科研人员研制出了M-LiH(M为Fe、Mn、Sc等金属)等催化剂,使得合成氨工业的温度、压强分别降到了350℃、1 MPa,这是近年来合成氨反应研究中的重要突破。
①已知元素呈气态时,从它的阳离子中将一个电子移至无穷远处时所需做的功,称为该元素的电离势,单位为电子伏特(eV)。Sc的三种气态离子
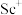 、
、 、
、 的电离势分别为6.54 eV、12.80 eV、24.76 eV,上述三种气态离子的电离势依次增大的原因为
的电离势分别为6.54 eV、12.80 eV、24.76 eV,上述三种气态离子的电离势依次增大的原因为②第三电离能

 ,原因是
,原因是
您最近一年使用:0次
9 . 下列说法错误的是
| A.钠原子的核外电子有11种运动状态 |
| B.电子仅从激发态跃迁到基态才产生原子光谱 |
| C.1个原子轨道里最多容纳2个电子,且自旋相反 |
| D.基态原子的电子排布遵循能量最低原理、洪特规则和泡利原理 |
您最近一年使用:0次
10 . 下列热化学方程式或离子方程式中,不正确的是
A. 的电离: 的电离: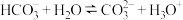 |
B.钢铁发生吸氧腐蚀时正极的电极反应式: |
C.甲烷的燃烧热为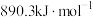 ,则甲烷燃烧的热化学方程式为 ,则甲烷燃烧的热化学方程式为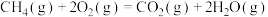 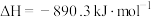 |
D.用饱和碳酸钠溶液处理水垢(CaSO4): |
您最近一年使用:0次



