1 . 已知A是一种气态烃,其密度在标准状况下是H2的14倍。下列关系图中部分产物可能略去,试回答下列问题: R—OH+NaX(R代表烃基,X代表卤素原子)。
R—OH+NaX(R代表烃基,X代表卤素原子)。
(1)写出A、C分子中的官能团名称:A__________ ,C__________ 。
(2)反应①~⑦中属于取代反应的是________ 。
(3)C与F以物质的量之比2∶1反应生成G,反应④的化学方程式为______________ 。
(4)B物质可在催化剂作用下被空气中的氧气氧化为具有刺激性气味的物质,写出反应的化学方程式:_________________ 。
(5)聚苯乙烯的结构简式为____________ 。
(6)下列说法正确的是________ (填字母)。
a.D在一定条件下可能会和水反应生成B和C
b.B和F互为同系物
c.A、B、F和I都能使酸性高锰酸钾溶液褪色
d.与E互为同分异构体的有机物只有1种

 R—OH+NaX(R代表烃基,X代表卤素原子)。
R—OH+NaX(R代表烃基,X代表卤素原子)。(1)写出A、C分子中的官能团名称:A
(2)反应①~⑦中属于取代反应的是
(3)C与F以物质的量之比2∶1反应生成G,反应④的化学方程式为
(4)B物质可在催化剂作用下被空气中的氧气氧化为具有刺激性气味的物质,写出反应的化学方程式:
(5)聚苯乙烯的结构简式为
(6)下列说法正确的是
a.D在一定条件下可能会和水反应生成B和C
b.B和F互为同系物
c.A、B、F和I都能使酸性高锰酸钾溶液褪色
d.与E互为同分异构体的有机物只有1种
您最近一年使用:0次
2 . 铁元素在细菌的作用下可发生如图所示的转化。下列说法中正确的是

| A.反硝化过程均属于氮的固定 |
| B.硝化过程中,含氮物质均发生还原反应 |
C. 将 将 转化为 转化为 的离子方程式为 的离子方程式为 |
D.在氨氧化细菌作用下,水体中的铵态氮和硝态氮可转移到大气中,该反应中每产生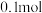 氮气时转移 氮气时转移 电子 电子 |
您最近一年使用:0次
3 . 下列有关化学反应速率的说法正确的是
A.用铁片与稀硫酸反应制取氢气时,改用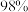 的浓硫酸可增大产生氢气的速率 的浓硫酸可增大产生氢气的速率 |
B. 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 的盐酸与锌片反应,加入适量的氯化钠溶液,化学反应速率不变 |
C. 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 的催化氧化反应是一个放热反应,所以升高温度,化学反应速率减小 |
D.汽车尾气中的 与 与 可以缓慢反应生成 可以缓慢反应生成 和 和 ,增大压强,化学反应速率增大 ,增大压强,化学反应速率增大 |
您最近一年使用:0次
4 . 下表列出9种元素在元素周期表(元素周期表只给出部分)中的位置
(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是________ 。
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为________ 。
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为________ 。
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是________ (填化学式,用“>”连接)。
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为________ 。
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是________ 。

(1)考古工作者利用表中某元素的一种核素测定一些文物的年代,这种核素的原子符号是
(2)由元素②和元素④形成原子个数比为1:2的化合物的电子式为
(3)元素⑦的最高价氧化物与元素⑥的最高价氧化物的水化物的水溶液反应的离子方程式为
(4)③、④、⑤三种元素的简单氢化物稳定性顺序是
(5)元素④和⑥形成的淡黄色固体与元素①和④形成的常用化合物反应的离子方程式为
(6)将元素⑧的单质通入元素⑥和⑨形成的化合物水溶液中,观察到的现象是
您最近一年使用:0次
解题方法
5 . 下列除杂的方法(括号里为少量杂质)中,所用试剂或操作不正确的是
| A.Fe2O3(Al2O3):加入足量NaOH溶液,过滤 |
| B.NaHCO3溶液(Na2CO3):通入足量的CO2 |
| C.FeCl3溶液(FeCl2):通入足量的氯气 |
| D.CO2(HCl):将气体通过盛有饱和Na2CO3溶液的洗气瓶 |
您最近一年使用:0次
名校
解题方法
6 . 化学反应中的热量问题,对于化工生产有重要的意义
(1)已知CO、H2、液态C2H5OH的燃烧热△H分别是-283.0 kJ/mol、-285.8 kJ/mol、-1366.8kJ/mol 。则101kPa、25℃时用冶铁炼钢废中的CO与H2合成乙醇的反应:2CO(g)+4H2(g)=C2H5OH(l)+H2O(l),该反应的△H=_______ kJ/mol。
(2)已知在微生物作用条件下, 经过两步反应被氧化成
经过两步反应被氧化成 ,两步反应的能量变化示意图如下。
,两步反应的能量变化示意图如下。 (aq)全部被氧化成
(aq)全部被氧化成 (aq)的热化学方程式为:
(aq)的热化学方程式为:_______ 。
(3)由天然气和水反应制备氢气:CH4(g)+2H2O(g)=CO2(g)+4H2(g),该反应过程中能量变化如下图所示,则该反应为_______ (填“吸热”或“放热”)反应。 _______ kJ(用含a、b、c、d的代数式表示)。
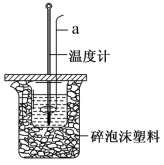
(4)室温下,用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示装置中进行中和反应。回答下列问题:_______ ,保持其他条件不变,实验中改用100mL0.50mol/L盐酸与100mL0.55mol/LNaOH溶液进行反应,与上述实验相比,二者所测的中和热_______ (填“相等”或“不相等”),原因是_______ 。
②若四次操作测得终止温度与起始温度差(T2 -T1)分别为_______ 。
①3.1℃ ②5.1℃ ③3.2℃;④33℃,则所得的中和反应的中和热△H=_______ kJ/mol(已知该温度下水的比热容:c=4.18J/(g·℃),保留三位有效数字)。
(1)已知CO、H2、液态C2H5OH的燃烧热△H分别是-283.0 kJ/mol、-285.8 kJ/mol、-1366.8kJ/mol 。则101kPa、25℃时用冶铁炼钢废中的CO与H2合成乙醇的反应:2CO(g)+4H2(g)=C2H5OH(l)+H2O(l),该反应的△H=
(2)已知在微生物作用条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 ,两步反应的能量变化示意图如下。
,两步反应的能量变化示意图如下。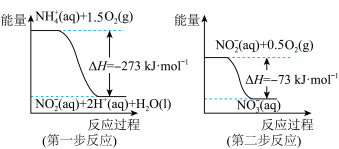
 (aq)全部被氧化成
(aq)全部被氧化成 (aq)的热化学方程式为:
(aq)的热化学方程式为:(3)由天然气和水反应制备氢气:CH4(g)+2H2O(g)=CO2(g)+4H2(g),该反应过程中能量变化如下图所示,则该反应为
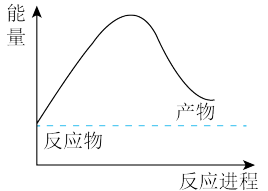
| 化学键 | C-H | O-H | C=O | H-H |
| 吸收热量(kJ/mol) | a | b | c | d |
②若四次操作测得终止温度与起始温度差(T2 -T1)分别为
①3.1℃ ②5.1℃ ③3.2℃;④33℃,则所得的中和反应的中和热△H=
您最近一年使用:0次
名校
解题方法
7 . 利用电化学装置原理可以设计出许多应用于环境保护、化学品提取的装置。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。_______ 极, 电极b表面发生的电极反应为_______ 。
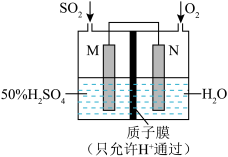
(2)可用电化学原理处理SO2制备硫酸并提供电能,装置如图,电极为多孔材料。写出M极的电极方程式:_______ ,外电路中电流方向为:_______ (填“从M到N”或者“从N到M”)_______ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。

(2)可用电化学原理处理SO2制备硫酸并提供电能,装置如图,电极为多孔材料。写出M极的电极方程式:

您最近一年使用:0次
名校
解题方法
8 . 一定条件下,反应H2(g)+Br2(g) 2HBr(g)的速率方程为v=kca(H2)·cb(Br2) ·cz(HBr),某温度下,该反应在不同浓度下的反应速率如下:
2HBr(g)的速率方程为v=kca(H2)·cb(Br2) ·cz(HBr),某温度下,该反应在不同浓度下的反应速率如下:
根据表中的测定结果,下列结论错误的是
 2HBr(g)的速率方程为v=kca(H2)·cb(Br2) ·cz(HBr),某温度下,该反应在不同浓度下的反应速率如下:
2HBr(g)的速率方程为v=kca(H2)·cb(Br2) ·cz(HBr),某温度下,该反应在不同浓度下的反应速率如下:| c(H2)/mol·L-l | c(Br2)/ mol·L-l | c(HBr)/ mol·L-l | 反应速率 |
| 0.1 | 0.1 | 2 | v |
| 0.1 | 0.4 | 2 | 8v |
| 0.2 | 0.4 | 2 | 16v |
| 0.4 | 0.1 | 4 | 2v |
| 0.2 | 0.1 | c | 4v |
| A.a的值为1 |
| B.表中c的值为2 |
| C.反应体系的三种物质中,Br2(g)的浓度对反应速率影响最大 |
| D.在反应体系中保持其他物质浓度不变,增大HBr(g)浓度,会使反应速率增大 |
您最近一年使用:0次
名校
解题方法
9 . 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。
(1)正四面体烷的分子式为___________ ,其二氯取代产物有___________ 种。
(2)关于乙烯基乙炔分子的说法错误的是___________ 。
a.能使酸性KMnO4溶液褪色
b.1mol乙烯基乙炔能与3mol Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:___________ 。
(4)以乙炔为主要原料,自选必要的无机试剂,合成聚氯乙烯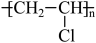 ,试写出有关化学反应方程式:
,试写出有关化学反应方程式:___________ 。

(1)正四面体烷的分子式为
(2)关于乙烯基乙炔分子的说法错误的是
a.能使酸性KMnO4溶液褪色
b.1mol乙烯基乙炔能与3mol Br2发生加成反应
c.乙烯基乙炔分子内含有两种官能团
d.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
(3)写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:
(4)以乙炔为主要原料,自选必要的无机试剂,合成聚氯乙烯
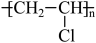 ,试写出有关化学反应方程式:
,试写出有关化学反应方程式:
您最近一年使用:0次
10 . 天然乳酸是乳制品中的天然固有成分,它有着乳制品的口味和良好的抗微生物作用,已广泛用于调配酸奶奶酪、冰淇淋等食品中,成为倍受青睐的乳制品酸味剂。乳酸的结构简式如图所示。下列关于乳酸性质的描述错误的是
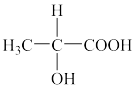
| A.乳酸易溶于水 | B.乳酸含有两种官能团,可以发生取代反应 |
| C.乳酸可以使酸性高锰酸钾溶液褪色 | D. 乳酸与足量钠反应一定产生 乳酸与足量钠反应一定产生 |
您最近一年使用:0次



