解题方法
1 . 我国科研团队研究出一种MB(亚甲基蓝)/MnO2固态无扩散氢离子电池,该电池模型如图所示,充电时,Mn2+沉积在石墨毡上生成MnO2,下列说法错误的是
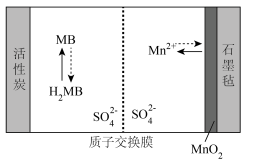
| A.放电时,石墨毡作正极 |
| B.放电时,H+从右侧区移到左侧区 |
| C.充电时,阴极发生反应MB+2H++2e-=H2MB |
| D.充电时,若转移0.2NA个电子石墨毡质量增加8.7g |
您最近一年使用:0次
解题方法
2 . 向一恒容密闭容器中,加入1molCH4和一定量的CO2,发生反应:CH4(g)+CO2(g) 2CO(g)+2H2(g)。CH4的平衡转化率按不同投料比x[x=
2CO(g)+2H2(g)。CH4的平衡转化率按不同投料比x[x=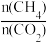 ]随温度的变化曲线如图所示。下列说法正确的是
]随温度的变化曲线如图所示。下列说法正确的是
 2CO(g)+2H2(g)。CH4的平衡转化率按不同投料比x[x=
2CO(g)+2H2(g)。CH4的平衡转化率按不同投料比x[x=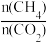 ]随温度的变化曲线如图所示。下列说法正确的是
]随温度的变化曲线如图所示。下列说法正确的是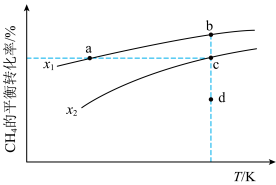
| A.投料比:x1>x2 | B.正反应速率:va>vb |
| C.压强:pa<pb | D.投料比为x2时d点浓度商Q大于c点平衡常数K |
您最近一年使用:0次
3 . 利用催化剂将汽车尾气中的NO和CO发生反应:2NO+2CO 2CO2+N2。使用等量的同种催化剂,设计实验探究温度、催化剂比表面积对反应速率的影响,实验结果如表。已知:x>y>z,下列分析错误的是
2CO2+N2。使用等量的同种催化剂,设计实验探究温度、催化剂比表面积对反应速率的影响,实验结果如表。已知:x>y>z,下列分析错误的是
 2CO2+N2。使用等量的同种催化剂,设计实验探究温度、催化剂比表面积对反应速率的影响,实验结果如表。已知:x>y>z,下列分析错误的是
2CO2+N2。使用等量的同种催化剂,设计实验探究温度、催化剂比表面积对反应速率的影响,实验结果如表。已知:x>y>z,下列分析错误的是| 实验编号 | 温度(℃) | NO起始浓度(mol•L-1) | CO起始浓度(mol•L-1) | 催化剂比表面积(m2•g-1) | CO平衡浓度(mol•L-1) | 平衡时间(min) |
| 1 | 280 | 6.5×10-3 | 4.0×10-3 | 80 | a | x |
| 2 | 280 | 6.5×10-3 | 4.0×10-3 | 120 | 1.0×10-3 | y |
| 3 | 360 | 6.5×10-3 | 4.0×10-3 | 80 | 2.0×10-3 | z |
| A.对比实验1、2可知,a=1.0×10-3 |
| B.实验2中,CO平衡转化率为75% |
| C.对比实验1、2可知,增大催化剂比表面积可加快反应速率 |
| D.对比实验1、3可知,该反应的△H>0 |
您最近一年使用:0次
解题方法
4 . T℃时,恒容密闭容器中发生反应PCl3(g)+Cl2(g) PCl5(g) △H<0,下列说法正确的是
PCl5(g) △H<0,下列说法正确的是
 PCl5(g) △H<0,下列说法正确的是
PCl5(g) △H<0,下列说法正确的是| A.该反应的△S<0,在高温下才能自发进行 |
| B.反应物断键所需总能量大于生成物成键所放出总能量 |
| C.增大反应物浓度能增加单位体积内的有效碰撞次数 |
| D.平衡后,向该容器中充入氦气,平衡向正反应方向移动 |
您最近一年使用:0次
解题方法
5 . 常温下,等体积的下列溶液混合后,混合液呈碱性的是
| A.等浓度的HCl与Na2CO3溶液 |
| B.pH=3的CH3COOH与pH=11的NaOH溶液 |
| C.等浓度的HCl与氨水 |
| D.pH=1的H2SO4与pH=12的NaOH溶液 |
您最近一年使用:0次
6 . 常温下,物质的量浓度均为0.1mol/L的下列溶液中,pH最小的是
| A.硫酸氢钠 | B.次氯酸钠 | C.食盐 | D.硫酸铜 |
您最近一年使用:0次
7 . 回答下列问题:
(1)肼(N2H4)常用于火箭或原电池的燃料。
已知:I.N2(g)+2O2(g) 2NO2(g);
2NO2(g);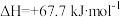
II.2N2H4(g)+2O2(g) 2N2(g)+4H2O(g);
2N2(g)+4H2O(g);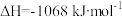
请写出N2H4和NO2反应的热化学方程式_______ ;
(2)氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
查阅资料:标准摩尔生成焓是指在 25℃和101kPa时,由元素最稳定的单质生成1mol纯化合物时的焓变,符号为 。已知以下物质的标准摩尔生成焓如下表所示。
。已知以下物质的标准摩尔生成焓如下表所示。
由此可得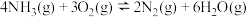 △H=
△H=_______  。
。
(3)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:_______
A接_______、_______接_______;B接_______、_______接_______;体现氯气的氧化性的实验现象为:_______ ,甲中发生反应的离子方程式为_______ 。
②实验时,电极材料为铁电极与石墨电极,装置中的石墨电极为_______ 极(填X、Y),此电解反应的离子方程式为_______ 。
③若要使电解后溶液恢复到电解前的状态,则需加入(或通入)_______ 。
(1)肼(N2H4)常用于火箭或原电池的燃料。
已知:I.N2(g)+2O2(g)
 2NO2(g);
2NO2(g);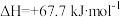
II.2N2H4(g)+2O2(g)
 2N2(g)+4H2O(g);
2N2(g)+4H2O(g);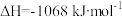
请写出N2H4和NO2反应的热化学方程式
(2)氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
查阅资料:标准摩尔生成焓是指在 25℃和101kPa时,由元素最稳定的单质生成1mol纯化合物时的焓变,符号为
 。已知以下物质的标准摩尔生成焓如下表所示。
。已知以下物质的标准摩尔生成焓如下表所示。| 物质 |  |  |
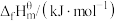 | -46 | -242 |
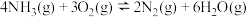 △H=
△H= 。
。(3)电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
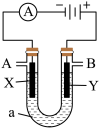
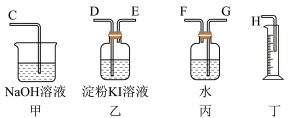
A接_______、_______接_______;B接_______、_______接_______;体现氯气的氧化性的实验现象为:
②实验时,电极材料为铁电极与石墨电极,装置中的石墨电极为
③若要使电解后溶液恢复到电解前的状态,则需加入(或通入)
您最近一年使用:0次
解题方法
8 . 利用所学电化学反应原理,解决以下问题:
(1)如图是电解未知浓度的硝酸银溶液的示意图,请根据要求答题。_______ 。
②当某电极的固体质量增重21.6g时,整个装置共产生气体(标准状况下)体积2.24L,推断该气体的组成_______ 。
(2)图中甲池的总反应式为N2H4+O2=N2+2H2O。_______
②要使乙池恢复到电解前的状态,应向溶液中加入适量的_______ 。
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(3)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:_______ 。
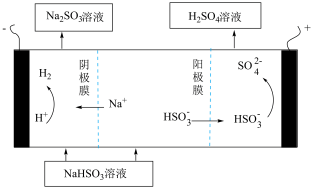
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图。请写出开始时阳极反应的电极反应式_______
(1)如图是电解未知浓度的硝酸银溶液的示意图,请根据要求答题。
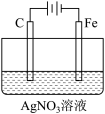
②当某电极的固体质量增重21.6g时,整个装置共产生气体(标准状况下)体积2.24L,推断该气体的组成
(2)图中甲池的总反应式为N2H4+O2=N2+2H2O。
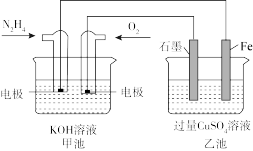
②要使乙池恢复到电解前的状态,应向溶液中加入适量的
A.CuO B.Cu(OH)2 C.CuCO3 D.CuSO4
(3)某科研小组用SO2为原料制取硫酸。
①利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池负极的电极反应式:
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如图。请写出开始时阳极反应的电极反应式
您最近一年使用:0次
9 . 回答下列问题。
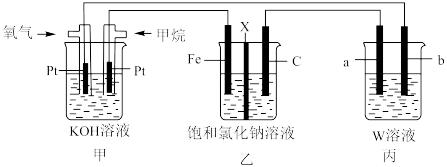
(1)铅蓄电池是典型的可充型电池,电池总反应为: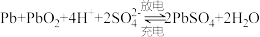 。请回答下列问题:
。请回答下列问题:
①放电时,负极电极反应式是_______ ;电解液中H2SO4的浓度将变_______ (选“变大”“变小”或“不变”);
②充电时,阳极的电极反应式是_______ 。
(2)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题:_______
②乙池中,若将乙装置中两电极用导线直接相连,则铁发生吸氧腐蚀,写出正极电极反应式:_______ 。
③若丙中要实现铁上镀银,b电极材料为_______ 。
(1)铅蓄电池是典型的可充型电池,电池总反应为:
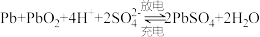 。请回答下列问题:
。请回答下列问题:①放电时,负极电极反应式是
②充电时,阳极的电极反应式是
(2)能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题:
②乙池中,若将乙装置中两电极用导线直接相连,则铁发生吸氧腐蚀,写出正极电极反应式:
③若丙中要实现铁上镀银,b电极材料为
您最近一年使用:0次
解题方法
10 . 新能源汽车是国家战略产业的重要组成部分,LiFePO4电池是能源汽车关键部件之一,电池工作时的总反应为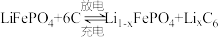 ,其工作原理如图所示:
,其工作原理如图所示:
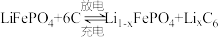 ,其工作原理如图所示:
,其工作原理如图所示: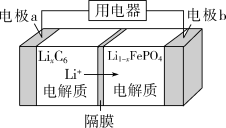
| A.充电时,电极a与电源负极连接,电极b与电源正极连接 |
| B.电池工作时,负极材料质量减少1.4g,转移0.4mol电子 |
C.电池工作时,正极的电极反应为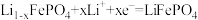 |
| D.电池进水后将会大大降低其使用寿命 |
您最近一年使用:0次



