设NA是阿伏加德罗常数的值。下列说法正确的是
| A.1molCH≡CH分子中所含的σ键数目为5NA |
| B.22.4LCH4分子中含有的C-H数目为4NA |
| C.标准状况下,28gCH2=CH2中含π键数目为NA |
| D.CH4和2.2.4LCl2恰好完全反应,生成的CH3Cl数目为0.1NA |
更新时间:2024/05/22 08:09:11
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】NA为阿伏加德罗常数,下列叙述正确的是
| A.22.4LCH4和CH3Cl的混合物所含有的分子数目为NA |
| B.用惰性电极电解1 L浓度均为2 mol/L的AgNO3与Cu(NO3)2的混合溶液,当有0.2 NA个电子转移时,阴极析出6.4g金属 |
| C.1mol过氧化氢分子中共用电子对数为3NA |
| D.0.1mol Na2CO3·10H2O在晶体中或溶液中,含有的CO32-离子均小于0.1 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.7.8gNa2S和Na2O2的混合物中,含有的离子总数为0.3NA |
| B.已知CrO5中Cr的化合价为+6价,则1molCrO5分子中过氧键的数目为NA |
| C.1L1mol/LH2O2溶液完全反应,转移的电子数目一定为2NA |
| D.常温下,pH=5的盐酸溶液中水电离出的H+数目为10-9NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设NA为阿伏加 德罗常数的值。下列说法正确的是( )
| A.71 g Cl2溶于足量水,所得溶液中Cl-、HClO和ClO-三种微粒总数为2NA |
| B.标准状况下,22.4 L H2O2中含有3NA个共价键 |
| C.常温下,将5.6 g铁块投入足量稀硝酸中,转移0.3NA个电子 |
| D.用电解法精炼铜时,若电路中转移2 mol电子,阳极质量减轻64 g |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下22.4L乙醇中,含O-H 键的数目为NA |
| B.密闭容器中2molNO与1molO2充分反应,产物的分子数目为2NA |
C.1L0.50mol/L的硝酸铵溶液中,含NO 数目为0.5NA 数目为0.5NA |
| D.1molCH4与1molCl2在光照下充分反应生成的CH3Cl分子数目为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于气体摩尔体积的说法正确的是( )
| A.22.4L任何气体的物质的量均为1mol |
| B.非标准状况下,1mol任何气体不可能占有22.4 L体积 |
| C.标况下,CO2气体摩尔体积是22.4L/mol |
| D.某物质含有6.02×1023个粒子,则该物质的体积为22.4L |
您最近一年使用:0次
单选题-单题
|
适中
(0.65)
名校
【推荐3】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.23.0 g乙醇与过量冰醋酸在浓硫酸、加热条件下反应,生成的乙酸乙酯分子数为0.5NA |
| B.常温常压下,100 g46%的乙醇溶液中,含H-O键的数目为NA |
| C.标准状况下,11.2 L己烷中所含分子数目为0.5NA |
| D.30 gHCHO和CH3COOH的混合物中含H原子数为2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列针对有机实验的说法正确的是
| 实验目的 | 实验操作、现象或结论 | 实验解释 | |
| A | 检验电石和水反应可产生乙炔 | 将产生的气体通过饱和食盐水后,再通入酸性 溶液中;若酸性 溶液中;若酸性 溶液褪色,说明有乙炔生成 溶液褪色,说明有乙炔生成 | 因为用饱和食盐水可以除去乙炔中混有的还原性杂质,所以证明有乙炔生成 |
| B | 探究光照条件下甲烷与氯气反应产物的种类 | 当氯气少量时,生成物中含有 、 、 、 、 、 、 等 等 | 因为 、 、 、 、 、 、 中碳氢键极性逐渐增强,所以与氯气发生取代反应的能力逐渐增强 中碳氢键极性逐渐增强,所以与氯气发生取代反应的能力逐渐增强 |
| C | 比较钠与水、钠与乙醇两个反应速率的大小 | 向两只分别盛有水和无水乙醇的烧杯中,各加入相同大小的钠,发现钠与水反应更剧烈 | 因为钠与水反应放出热量更多,温度升高更快,所以反应更剧烈 |
| D | 检验苯和液溴在 催化剂作用下生成的气体 催化剂作用下生成的气体 | 将苯、液溴、铁粉混合物反应产生的气体通入到 溶液中有淡黄色沉淀产生 溶液中有淡黄色沉淀产生 | 因为产生了淡黄色沉淀,所以证明有HBr气体生成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1molCH4与Cl2在光照下反应生成的CH3Cl分子数为NA |
| B.92g甘油中含有羟基数为NA |
| C.0.1mol·L-1 的盐酸中含有氯离子总数为0.1NA |
| D.1mol Na2O2与足量H2O反应,转移的电子数目为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】解释下列现象的原因不正确的是
| 选项 | 现象 | 原因 |
| A | 键的极性: | 非金属性差异越大,键的极性越小 |
| B | 白磷( )为正四面体分子 )为正四面体分子 | 白磷分子中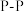 键间的夹角是 键间的夹角是 |
| C | 分子内不同化学键之间存在一定的夹角 | 共价键具有方向性 |
| D | 熔点: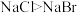 |  、 、 随着离子间距的增大,晶格能减小,晶体的熔点降低 随着离子间距的增大,晶格能减小,晶体的熔点降低 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】理论化学模拟得到一种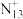 离子,结构如图所示。下列关于该离子的说法不正确的是
离子,结构如图所示。下列关于该离子的说法不正确的是
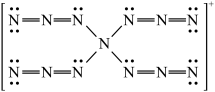
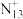 离子,结构如图所示。下列关于该离子的说法不正确的是
离子,结构如图所示。下列关于该离子的说法不正确的是
| A.该离子内存在σ键与π键 |
| B.N原子的杂化方式有3种 |
| C.该离子中所有N原子可能在同一平面内 |
| D.所有原子均满足8电子结构 |
您最近一年使用:0次

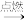 CO2+ 2H2O
CO2+ 2H2O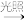 CH3CHCl2+ HCl
CH3CHCl2+ HCl

