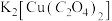 可用于功能材料的制备。下列说法正确的是
可用于功能材料的制备。下列说法正确的是| A.碳原子与氮原子形成的(CN)2属于极性分子 |
| B.钾晶体中1个K+只与1个价层电子存在强烈的相互作用 |
| C.第二周期中,第一电离能大于氧元素的有三种 |
| D.基态铜原子的4s电子能量较高,总是在比3s电子离核更远的地方运动 |
更新时间:2024-05-22 08:10:01
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】H、Li、Na、K位于周期表中IA族。下列说法正确的是
| A.离子半径大小:r(H-)<r(Li+) | B.碱性强弱:NaOH>KOH |
| C.电负性大小:χ(Li)<χ(Na) | D.可在IA族找到制造光电材料的元素 |
您最近一年使用:0次
【推荐2】2016年6月国际纯粹与应用化学联合会宣布,将合成的117号元素( )提名为化学新元素,该元素有两种原子:
)提名为化学新元素,该元素有两种原子: 、
、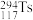 ,下列说法不正确的是( )
,下列说法不正确的是( )
 )提名为化学新元素,该元素有两种原子:
)提名为化学新元素,该元素有两种原子: 、
、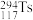 ,下列说法不正确的是( )
,下列说法不正确的是( )A. 和 和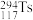 是两种核素 是两种核素 |
B. 和 和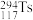 互为同位素 互为同位素 |
C. 和 和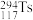 的中子数分别为176和177 的中子数分别为176和177 |
D. 和 和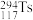 的第一电离能不相等 的第一电离能不相等 |
您最近一年使用:0次
【推荐1】如图是某无机化合物的二聚分子,该分子中A、B两种元素都只有3个能层,分子中所有原子的最外层都达到8个电子的稳定结构。下列说法不正确的是
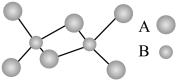
| A.元素A位于元素周期表第三周期第ⅢA族 |
| B.该化合物是共价化合物,在熔融状态下能导电 |
| C.该化合物在固态时所形成的晶体是分子晶体 |
| D.该化合物中存在极性共价键,无非极性共价键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】利用离子液体 可电沉积还原金属Ge,其中
可电沉积还原金属Ge,其中 的结构如图所示。下列有关说法错误的是
的结构如图所示。下列有关说法错误的是
 可电沉积还原金属Ge,其中
可电沉积还原金属Ge,其中 的结构如图所示。下列有关说法错误的是
的结构如图所示。下列有关说法错误的是
| A.该离子液体能导电 | B. 的空间构型为正四面体形 的空间构型为正四面体形 |
C.该物质中碳原子的杂化类型为 | D.电解沉积金属时,金属在阴极析出 |
您最近一年使用:0次
【推荐1】SiH4的分子结构与CH4类似,对SiH4作出如下推测,其中不正确的是
| A. SiH4晶体是分子晶体 | B. SiH4的热稳定性比CH4弱 |
| C. SiH4是由极性键形成的非极性分子 | D. SiH4的沸点低于CH4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】“中国芯”的主要原材料是高纯单晶硅,反应SiCl4(g)+2H2(g)  Si(s)+4HCl(g)可用于纯硅的制备。下列有关说法正确的是
Si(s)+4HCl(g)可用于纯硅的制备。下列有关说法正确的是
 Si(s)+4HCl(g)可用于纯硅的制备。下列有关说法正确的是
Si(s)+4HCl(g)可用于纯硅的制备。下列有关说法正确的是| A.SiCl4为极性分子 | B.HCl中含有s-pσ键 |
| C.单晶硅为分子晶体 | D.Si原子的结构示意图为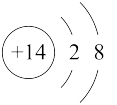 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于金属及金属键的说法正确的是
| A.金属键具有方向性与饱和性 |
| B.金属键是金属阳离子与“自由电子”间的相互作用 |
| C.金属导电是因为在外加电场作用下产生“自由电子” |
| D.金属具有光泽是因为金属阳离子吸收并放出可见光 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.由于铵盐是由离子键构成的,因而化学性质相当稳定 |
| B.金属晶体中一定含有金属键,金属键没有方向性和饱和性 |
| C.在常见的四种晶体类型中,都有“原子(离子)半径越大,物质熔点越低”的规律 |
| D.水晶在不同方向上的硬度、导热性、导电性相同 |
您最近一年使用:0次

 和
和 均可发生水解反应,其中
均可发生水解反应,其中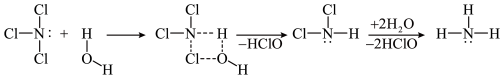
 模型为三角锥形
模型为三角锥形 中的N均为
中的N均为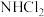 和
和 形成氢键
形成氢键 的空间共构型为平面三角形
的空间共构型为平面三角形

