名校
1 . 2023年7月17日,习近平主席在全国生态环境保护大会上发表重要讲话,其中强调要实现绿色低碳转型,以更加积极的姿态参与全球气候治理。回答下列问题:
(1)一定条件下, 与
与 反应可转化为
反应可转化为 、
、 ,该反应不仅可应用于温室气体的消除,实现低碳发展,还可以应用于空间站中
,该反应不仅可应用于温室气体的消除,实现低碳发展,还可以应用于空间站中 与
与 的循环,实现
的循环,实现 的再生。
的再生。
已知:反应Ⅰ.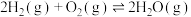

反应Ⅱ.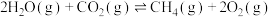
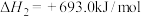
反应Ⅲ.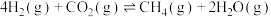

则
______  ,推测反应Ⅲ在
,推测反应Ⅲ在______ (填“较高温度”、“较低温度”或“任何温度”)条件下能自发进行。
(2)一定条件下,利用甲烷可将 还原为
还原为 。在一密闭容器中充入
。在一密闭容器中充入 、
、 气体各
气体各 ,发生反应
,发生反应
 。测得
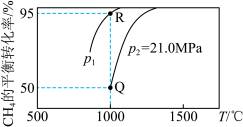
。测得 的平衡转化率随温度、压强的变化曲线如图所示,
的平衡转化率随温度、压强的变化曲线如图所示,
______ 0(填“>”“<”或“=”),
______  (填“>”“<”或“=”);
(填“>”“<”或“=”); 点的压强平衡常数
点的压强平衡常数
______  (用平衡分压代替平衡浓度计算,气体的分压=气体总压强×该气体的物质的量分数)。
(用平衡分压代替平衡浓度计算,气体的分压=气体总压强×该气体的物质的量分数)。
(3)利用强氧化剂可以对烟气进行脱硫脱硝。在某工厂中,用 溶液作氧化剂,控制
溶液作氧化剂,控制 ,将烟气中
,将烟气中 和
和 转化为高价含氧酸根离子。测得溶液在不同温度时,脱除率如下表:
转化为高价含氧酸根离子。测得溶液在不同温度时,脱除率如下表:
请写出 脱除原理的离子方程式
脱除原理的离子方程式________________________ ;温度高于 时,脱除率逐渐降低,原因是
时,脱除率逐渐降低,原因是________________________ 。
(4)科学家近日发明了一种无污染、无需净化的高效产氢可充电电池,电池示意图如下。电极为金属锌和选择性催化材料,实现了放电析氢和充电 氧化两个独立的反应。
氧化两个独立的反应。
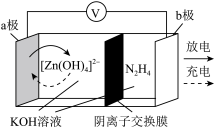
①放电时,负极区溶液
____________ (填“增大”“减小”或“不变”);
②充电时 极的电极反应方程式为
极的电极反应方程式为__________________ ;若两电极池充电前质量相等,当外电路转移 时,阴阳两极电解池的质量之差为
时,阴阳两极电解池的质量之差为__________________  。
。
(1)一定条件下,
 与
与 反应可转化为
反应可转化为 、
、 ,该反应不仅可应用于温室气体的消除,实现低碳发展,还可以应用于空间站中
,该反应不仅可应用于温室气体的消除,实现低碳发展,还可以应用于空间站中 与
与 的循环,实现
的循环,实现 的再生。
的再生。已知:反应Ⅰ.
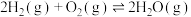

反应Ⅱ.
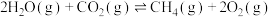
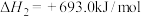
反应Ⅲ.
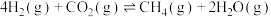

则

 ,推测反应Ⅲ在
,推测反应Ⅲ在(2)一定条件下,利用甲烷可将
 还原为
还原为 。在一密闭容器中充入
。在一密闭容器中充入 、
、 气体各
气体各 ,发生反应
,发生反应
 。测得
。测得 的平衡转化率随温度、压强的变化曲线如图所示,
的平衡转化率随温度、压强的变化曲线如图所示,

 (填“>”“<”或“=”);
(填“>”“<”或“=”); 点的压强平衡常数
点的压强平衡常数
 (用平衡分压代替平衡浓度计算,气体的分压=气体总压强×该气体的物质的量分数)。
(用平衡分压代替平衡浓度计算,气体的分压=气体总压强×该气体的物质的量分数)。
(3)利用强氧化剂可以对烟气进行脱硫脱硝。在某工厂中,用
 溶液作氧化剂,控制
溶液作氧化剂,控制 ,将烟气中
,将烟气中 和
和 转化为高价含氧酸根离子。测得溶液在不同温度时,脱除率如下表:
转化为高价含氧酸根离子。测得溶液在不同温度时,脱除率如下表:温度 | 10 | 20 | 40 | 50 | 60 | 80 | |
| 脱除率% |  | 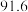 | 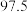 | 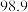 | 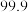 | 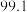 | 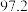 |
 |  | 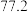 | 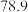 |  | 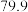 |  | |
 脱除原理的离子方程式
脱除原理的离子方程式 时,脱除率逐渐降低,原因是
时,脱除率逐渐降低,原因是(4)科学家近日发明了一种无污染、无需净化的高效产氢可充电电池,电池示意图如下。电极为金属锌和选择性催化材料,实现了放电析氢和充电
 氧化两个独立的反应。
氧化两个独立的反应。
①放电时,负极区溶液

②充电时
 极的电极反应方程式为
极的电极反应方程式为 时,阴阳两极电解池的质量之差为
时,阴阳两极电解池的质量之差为 。
。
您最近一年使用:0次
2024-02-14更新
|
223次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
2 . 关于第Ⅳ 族的元素——碳(
族的元素——碳( )、硅(
)、硅( )、锗(
)、锗( )、锡(
)、锡( )和铅(
)和铅( ),它们可形成许多结构各异的物质。回答下列问题:
),它们可形成许多结构各异的物质。回答下列问题:
(1)基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为______ ,有______ 种不同运动状态的电子。
(2) 中
中 原子的杂化类型是
原子的杂化类型是______ , 的空间结构是
的空间结构是______ 。
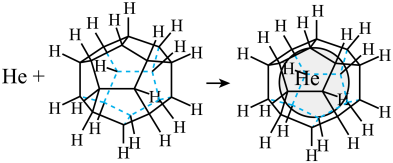
(3)1999年,科学家成功地将一个 原子“装入”了一个
原子“装入”了一个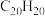 的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为
的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为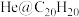 )。则
)。则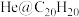 中,
中, 与
与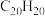 之间的作用力为
之间的作用力为______ 。
(4)第Ⅳ 族的金属元素可形成
族的金属元素可形成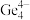 、
、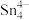 和
和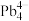 等阴离子,根据等电子体原理判断,
等阴离子,根据等电子体原理判断,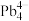 中的键角为
中的键角为______ 。
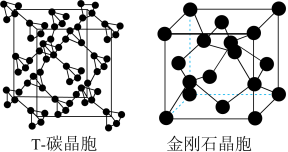
(5)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成 碳,
碳, 碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
碳的密度约为金刚石的一半 , 碳晶体的晶胞、金刚石的晶胞如图所示。则
碳晶体的晶胞、金刚石的晶胞如图所示。则 碳晶胞的棱长是金刚石晶胞棱长的
碳晶胞的棱长是金刚石晶胞棱长的______ 倍。
(6) 与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。
与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。 与
与 形成的一种超导材料的晶胞如图所示,图中白球表示
形成的一种超导材料的晶胞如图所示,图中白球表示 ,黑球表示钾原子。
,黑球表示钾原子。
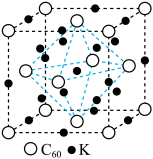
①该材料的化学式是____________ 。
②已知晶胞边长为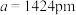 ,则该超导材料的理论密度为
,则该超导材料的理论密度为
____________  (写出表达式)。
(写出表达式)。
 族的元素——碳(
族的元素——碳( )、硅(
)、硅( )、锗(
)、锗( )、锡(
)、锡( )和铅(
)和铅( ),它们可形成许多结构各异的物质。回答下列问题:
),它们可形成许多结构各异的物质。回答下列问题:(1)基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)
 中
中 原子的杂化类型是
原子的杂化类型是 的空间结构是
的空间结构是(3)1999年,科学家成功地将一个
 原子“装入”了一个
原子“装入”了一个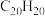 的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为
的空腔内,得到了“世界上最小的氦气球”(如图所示,产物记为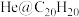 )。则
)。则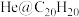 中,
中, 与
与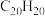 之间的作用力为
之间的作用力为
(4)第Ⅳ
 族的金属元素可形成
族的金属元素可形成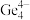 、
、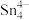 和
和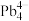 等阴离子,根据等电子体原理判断,
等阴离子,根据等电子体原理判断,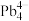 中的键角为
中的键角为(5)科研团队通过皮秒激光照射悬浮在甲醇溶液中的多臂碳纳米管合成
 碳,
碳, 碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
碳的晶体结构可以看成金刚石晶体中每个碳原子被一个由四个碳原子组成的正四面体结构单元取代,
 碳晶体的晶胞、金刚石的晶胞如图所示。则
碳晶体的晶胞、金刚石的晶胞如图所示。则 碳晶胞的棱长是金刚石晶胞棱长的
碳晶胞的棱长是金刚石晶胞棱长的
(6)
 与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。
与碱金属形成的盐具有特别的意义,他们能在低温时转变为超导材料。 与
与 形成的一种超导材料的晶胞如图所示,图中白球表示
形成的一种超导材料的晶胞如图所示,图中白球表示 ,黑球表示钾原子。
,黑球表示钾原子。
①该材料的化学式是
②已知晶胞边长为
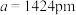 ,则该超导材料的理论密度为
,则该超导材料的理论密度为
 (写出表达式)。
(写出表达式)。
您最近一年使用:0次
2024-02-14更新
|
236次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
3 . 市场上的静脉补铁剂以三价铁为主。如蔗糖铁,其具备结构稳定、毒性很低、安全、快速有效、副作用小的补铁治疗效果。已知某蔗糖铁绿色环保合成过程如下:
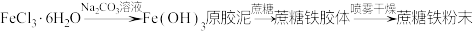 现实验室制备氢氧化铁原胶泥并进行其铁含量的测定(已知氢氧化铁原胶泥粒子大小介于
现实验室制备氢氧化铁原胶泥并进行其铁含量的测定(已知氢氧化铁原胶泥粒子大小介于 之间)。回答下列问题:
之间)。回答下列问题:
Ⅰ.氢氧化铁原胶泥的制备
在装置 中加入
中加入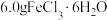 和
和 蒸馏水,搅拌,控制水浴温度在
蒸馏水,搅拌,控制水浴温度在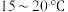 缓慢滴加
缓慢滴加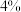 的
的 溶液,
溶液, 滴完,继续搅拌
滴完,继续搅拌 ,分离制得
,分离制得 原胶泥。加入蒸馏水重复洗涤、分离四次。
原胶泥。加入蒸馏水重复洗涤、分离四次。

(1)仪器 的名称是
的名称是__________________ 。
(2)制备 Fe(OH)3原胶泥的离子方程式为__________________ 。
(3)水浴温度不宜过高,Na2CO3溶液滴加速度不宜过快的原因均是____________ 。
(4)分离得到Fe(OH)3原胶泥的方法是____________(填标号)。
(5)检验 Fe(OH)3原胶泥已洗净的方法是__________________ 。
Ⅱ.氢氧化铁原胶泥中铁含量的测定
准确称量3.00g原胶泥于碘量瓶中(如图所示,用于碘量法测定的专用锥形瓶;即在锥形瓶口上使用磨口塞子,盖塞子后可以水封瓶口),加 蒸馏水和
蒸馏水和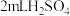 ,加热至微沸,充分溶解。加足量盐酸和
,加热至微沸,充分溶解。加足量盐酸和 溶液后,
溶液后,盖紧瓶塞 ,静置 。用
。用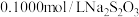 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: ,至接近终点时,加淀粉指示剂,继续滴定至终点,消耗标准溶液
,至接近终点时,加淀粉指示剂,继续滴定至终点,消耗标准溶液 。
。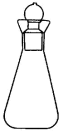
(6)实验中碘量瓶盖紧瓶塞的目的是__________________ 。
(7)在滴定过程中淀粉指示剂不能过早加入,否则较多I2会被淀粉包裹而导致终点迟滞,使铁含量的测定结果____________ (填“偏高”或“偏低”)。
(8)计算氢氧化铁原胶泥样品中铁的质量分数为____________  (结果保留三位有效数字)。
(结果保留三位有效数字)。
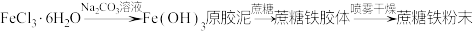 现实验室制备氢氧化铁原胶泥并进行其铁含量的测定(已知氢氧化铁原胶泥粒子大小介于
现实验室制备氢氧化铁原胶泥并进行其铁含量的测定(已知氢氧化铁原胶泥粒子大小介于 之间)。回答下列问题:
之间)。回答下列问题:Ⅰ.氢氧化铁原胶泥的制备
在装置
 中加入
中加入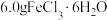 和
和 蒸馏水,搅拌,控制水浴温度在
蒸馏水,搅拌,控制水浴温度在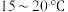 缓慢滴加
缓慢滴加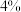 的
的 溶液,
溶液, 滴完,继续搅拌
滴完,继续搅拌 ,分离制得
,分离制得 原胶泥。加入蒸馏水重复洗涤、分离四次。
原胶泥。加入蒸馏水重复洗涤、分离四次。 
(1)仪器
 的名称是
的名称是(2)制备 Fe(OH)3原胶泥的离子方程式为
(3)水浴温度不宜过高,Na2CO3溶液滴加速度不宜过快的原因均是
(4)分离得到Fe(OH)3原胶泥的方法是____________(填标号)。
| A.离心分离(对比重不同的物质借助于离心力进行分离) | B.过滤 |
| C.减压过滤 | D.蒸馏 |
Ⅱ.氢氧化铁原胶泥中铁含量的测定
准确称量3.00g原胶泥于碘量瓶中(如图所示,用于碘量法测定的专用锥形瓶;即在锥形瓶口上使用磨口塞子,盖塞子后可以水封瓶口),加
 蒸馏水和
蒸馏水和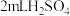 ,加热至微沸,充分溶解。加足量盐酸和
,加热至微沸,充分溶解。加足量盐酸和 溶液后,
溶液后, 。用
。用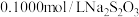 标准溶液滴定,发生反应:
标准溶液滴定,发生反应: ,至接近终点时,加淀粉指示剂,继续滴定至终点,消耗标准溶液
,至接近终点时,加淀粉指示剂,继续滴定至终点,消耗标准溶液 。
。
(6)实验中碘量瓶盖紧瓶塞的目的是
(7)在滴定过程中淀粉指示剂不能过早加入,否则较多I2会被淀粉包裹而导致终点迟滞,使铁含量的测定结果
(8)计算氢氧化铁原胶泥样品中铁的质量分数为
 (结果保留三位有效数字)。
(结果保留三位有效数字)。
您最近一年使用:0次
2024-02-14更新
|
157次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
4 . 电解水是一种简单、低成本的制氢方法。在酸性电解质中,阴极反应包括以下步骤:Ⅰ. ;Ⅱ.
;Ⅱ. (注:“
(注:“ ”代表活性表面位点);而碱性条件下电解过程则需更多能耗(无其他反应)。下列说法正确的是
”代表活性表面位点);而碱性条件下电解过程则需更多能耗(无其他反应)。下列说法正确的是
 ;Ⅱ.
;Ⅱ. (注:“
(注:“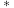 ”代表活性表面位点);而碱性条件下电解过程则需更多能耗(无其他反应)。下列说法正确的是
”代表活性表面位点);而碱性条件下电解过程则需更多能耗(无其他反应)。下列说法正确的是A.阴极总反应为: |
| B.酸性条件下反应活化能更大 |
| C.碱性条件下反应速率更快 |
| D.同温同压下,产生等体积的氢气,酸性、碱性电解质条件下转移电子的物质的量不等 |
您最近一年使用:0次
2024-02-14更新
|
139次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
5 .  时,用等浓度的
时,用等浓度的 溶液分别滴定一元酸
溶液分别滴定一元酸 溶液和
溶液和 溶液,
溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 ]与溶液
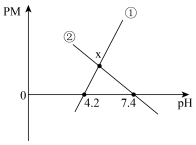
]与溶液 的变化关系如图所示。已知:
的变化关系如图所示。已知: 易溶于水,一般认为反应的平衡常数
易溶于水,一般认为反应的平衡常数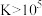 时反应进行完全。下列说法错误的是
时反应进行完全。下列说法错误的是
 时,用等浓度的
时,用等浓度的 溶液分别滴定一元酸
溶液分别滴定一元酸 溶液和
溶液和 溶液,
溶液, [
[ 表示负对数,
表示负对数, 表示
表示 、
、 ]与溶液
]与溶液 的变化关系如图所示。已知:
的变化关系如图所示。已知: 易溶于水,一般认为反应的平衡常数
易溶于水,一般认为反应的平衡常数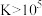 时反应进行完全。下列说法错误的是
时反应进行完全。下列说法错误的是
A.线①代表滴定 溶液时 溶液时 与溶液 与溶液 的变化关系 的变化关系 |
B. 为一元弱酸, 为一元弱酸, 时 时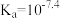 |
C. 的 的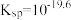 |
D.滴定 溶液至 溶液至 点时,改为滴加 点时,改为滴加 溶液,沉淀最后能完全溶解 溶液,沉淀最后能完全溶解 |
您最近一年使用:0次
2024-02-14更新
|
195次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
6 . 由下列实验及现象推出的相应结论正确的是
实验 | 现象 | 结论 | |
A | 向 溶液中滴加过量氯水,再加入淀粉 溶液中滴加过量氯水,再加入淀粉 溶液 溶液 | 先变橙色,后变蓝色 | 氧化性: |
B | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 | 增大氢离子浓度,转化平衡向生成 |
C | 向含有 和 和 的悬浊液中滴加 的悬浊液中滴加 溶液 溶液 | 生成黑色沉淀 |
|
D | ①某溶液中加入 溶液 溶液②再加足量盐酸 | ①产生白色沉淀 ②仍有白色沉淀 | 原溶液中有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-14更新
|
169次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
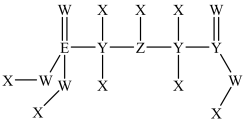
7 . 草甘膦,是一种有机膦类除草剂,其结构式如图。其中 、
、 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素。其中
为原子序数依次增大的短周期主族元素。其中 只有
只有 能级上有电子,
能级上有电子, 原子的电子总数为价层电子数三倍,
原子的电子总数为价层电子数三倍, 的电子排布式中有三对成对电子。下列说法正确的是
的电子排布式中有三对成对电子。下列说法正确的是
 、
、 、
、 、
、 、
、 为原子序数依次增大的短周期主族元素。其中
为原子序数依次增大的短周期主族元素。其中 只有
只有 能级上有电子,
能级上有电子, 原子的电子总数为价层电子数三倍,
原子的电子总数为价层电子数三倍, 的电子排布式中有三对成对电子。下列说法正确的是
的电子排布式中有三对成对电子。下列说法正确的是
A. 、 、 、 、 三种元素中原子半径最大的是 三种元素中原子半径最大的是 |
B. 、 、 的第一电离能 的第一电离能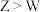 |
C. 、 、 、 、 、 、 、 、 最外层均达到8电子稳定结构 最外层均达到8电子稳定结构 |
D.电负性 ,则其简单氢化物的还原性 ,则其简单氢化物的还原性 |
您最近一年使用:0次
2024-02-14更新
|
329次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
8 . 已知某温度下 和
和 的电离常数相等。现向
的电离常数相等。现向 浓度为
浓度为 的氨水溶液中滴加相同浓度的醋酸溶液,在滴加过程中,下列说法不正确的是
的氨水溶液中滴加相同浓度的醋酸溶液,在滴加过程中,下列说法不正确的是
 和
和 的电离常数相等。现向
的电离常数相等。现向 浓度为
浓度为 的氨水溶液中滴加相同浓度的醋酸溶液,在滴加过程中,下列说法不正确的是
的氨水溶液中滴加相同浓度的醋酸溶液,在滴加过程中,下列说法不正确的是A. 与 与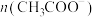 之和始终增大 之和始终增大 |
| B.水的电离程度始终增大 |
C. 先增大再减小 先增大再减小 |
D.当加入该醋酸溶液的体积为 时, 时,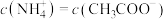 |
您最近一年使用:0次
2024-02-14更新
|
151次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
解题方法
9 . 下列实验装置或操作能够达到实验目的的是
A | B | C | D |
配制一定浓度的盐酸标准液 | 用乙醇萃取碘水中的碘 | 蒸干 | 排除碱式滴定管中的气泡 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-14更新
|
187次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题
名校
10 . 下列有关方程式错误的是
A. 燃烧热的热化学方程式: 燃烧热的热化学方程式: 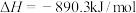 |
B.铅酸蓄电池充电时的阳极反应: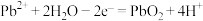 |
C. 沉淀转化为 沉淀转化为 沉淀: 沉淀: |
D.煅烧黄铁矿制 : : |
您最近一年使用:0次
2024-02-14更新
|
119次组卷
|
2卷引用:重庆市西南大学附中2023-2024学年高二上学期期末考试化学试题


 溶液中缓慢滴加硫酸,黄色变为橙色
溶液中缓慢滴加硫酸,黄色变为橙色 的溶解度小于
的溶解度小于
 溶液得
溶液得