1 . 下列有机物的系统命名正确的是
A.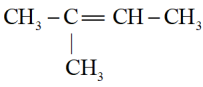 3—甲基—2—丁烯 3—甲基—2—丁烯 |
B.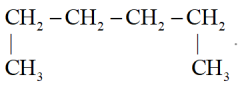 1,4—二甲基丁烷 1,4—二甲基丁烷 |
C.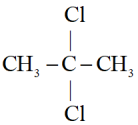 2—二氯丙烷 2—二氯丙烷 |
D. 2,3—二甲基戊烷 2,3—二甲基戊烷 |
您最近一年使用:0次
名校
解题方法
2 . 一种超导材料中含 、P、O、S等元素。下列说法正确的是
、P、O、S等元素。下列说法正确的是
 、P、O、S等元素。下列说法正确的是
、P、O、S等元素。下列说法正确的是A.原子半径: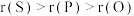 | B.第一电离能: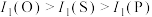 |
C.酸性强弱: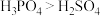 | D.电负性: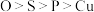 |
您最近一年使用:0次
名校
3 .  也可支持燃烧,金属镁在
也可支持燃烧,金属镁在 中的燃烧反应:
中的燃烧反应: ,下列说法正确的是
,下列说法正确的是
 也可支持燃烧,金属镁在
也可支持燃烧,金属镁在 中的燃烧反应:
中的燃烧反应: ,下列说法正确的是
,下列说法正确的是A. 的电子式: 的电子式: | B. 是含有极性键的非极性分子 是含有极性键的非极性分子 |
C. 和 和 所含化学键类型完全相同 所含化学键类型完全相同 | D.氧原子核外能量最高的电子的电子云图: |
您最近一年使用:0次
名校
解题方法
4 . 我国在新材料领域研究的重大突破,为“天宫”空间站的建设提供了坚实的物质基础。“天宫”空间站使用的材料中含有Li、B、C、N、P、Ni、Fe等元素。回答下列问题:
(1)下列不同状态的硼中,用光谱仪可捕捉到发射光谱的是___________(填标号)。
(2)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。___________ 。
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为___________ 。
③立方相氮化硼晶胞边长为apm,NA代表阿伏加德罗常数的值,则该晶体的密度为___________ g∙cm-3。
(3)FeSO4∙7H2O的结构如图所示,其中∠1、∠2、∠3由大到小的顺序是___________ 。___________ 。
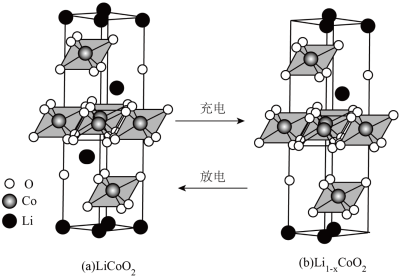
(5)锂离子电池具有可靠性高、寿命长、没有记忆效应等优势,能够提高飞船靠泊时间,是解决空间站问题的重要举措。正极材料LiCoO2的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有___________ 个O;充电时,LiCoO2脱出部分Li+,形成Li1-xCoO2,结构如图(b),则n(Co3+):n(Co4+)=___________ 。
(1)下列不同状态的硼中,用光谱仪可捕捉到发射光谱的是___________(填标号)。
A.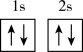 | B.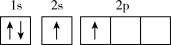 |
C. | D.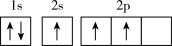 |
(2)氮化硼(BN)晶体有多种结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,质地软,可作润滑剂。立方相氮化硼与金刚石相似,是超硬材料,有优异的耐磨性。它们的晶体结构及晶胞如图所示。
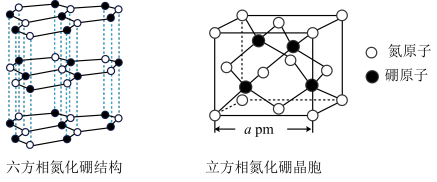
②立方相氮化硼晶体中“一般共价键”与配位键的数目之比为
③立方相氮化硼晶胞边长为apm,NA代表阿伏加德罗常数的值,则该晶体的密度为
(3)FeSO4∙7H2O的结构如图所示,其中∠1、∠2、∠3由大到小的顺序是

(5)锂离子电池具有可靠性高、寿命长、没有记忆效应等优势,能够提高飞船靠泊时间,是解决空间站问题的重要举措。正极材料LiCoO2的晶胞结构如图(a)(Li位于晶胞顶点和内部,部分O位于晶胞之外),每个晶胞中含有
您最近一年使用:0次
名校
5 . 使用下列装置及试剂,可以实现元素不同价态之间的转化的是
| 选项 | 转化 | 试剂a | 试剂b | 试剂c |
|
| A | 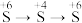 | 浓硫酸 | Cu |  溶液 溶液 | |
| B | 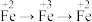 | 稀硫酸 | FeS |  溶液 溶液 | |
| C | 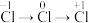 | 浓盐酸 |  | 水 | |
| D | 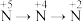 | 浓硝酸 | Cu | 水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 我国化学家开创性提出聚集诱导发光(AIE)概念,HPS作为经典的AIE分子,可由如图路线合成

| A.X中苯环上的一溴代物有5种 | B.X中所有原子肯定共平面 |
| C.HPS可使酸性高锰酸钾溶液褪色 | D.生成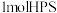 同时生成 同时生成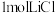 |
您最近一年使用:0次
名校
解题方法
7 . 下列化学用语表示不正确的是
A.联氨 的分子模型为: 的分子模型为: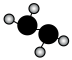 |
B.氯原子的结构示意图: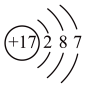 |
C.HClO的电子式: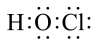 |
D.溴化铵的电子式: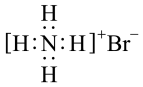 |
您最近一年使用:0次
名校
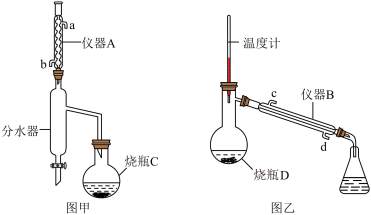
8 . 苯甲酸乙酯可用于配制香水香精和人造精油,还可以作为食用香精用于食品中。实验室可用苯甲酸与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)
(2)制备方法:
①在烧瓶C中加入一定量的下列物质(如下表)。按图甲所示安装好装置,加热烧瓶C.反应一段时间后,停止加热。
②将烧瓶C中的反应液倒入盛有30mL水的烧杯中,加入Na2CO3至溶液呈中性。
③用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,二者合并,加入图乙的烧瓶D中,加入沸石并加入无水硫酸镁,加热蒸馏,制得产品2.6mL。回答下列问题:
(1)仪器A的名称是___________ 。
(2)苯甲酸与乙醇制备苯甲酸乙酯的化学方程式为___________ 。
(3)环己烷、乙醇与水可形成共沸物,沸点为62.1℃,烧瓶C的最佳加热方式是___________ 。分水器“分水”的过程为___________ 。
(4)Na2CO3的作用是___________ 。
(5)采用图乙装置进行蒸馏操作,加入无水硫酸镁的目的是___________ ,在锥形瓶中,收集___________ ℃的馏分。
(6)该制备方法中苯甲酸乙酯的产率是___________ 。
| 物质 | 乙醇 | 苯甲酸 | 环己烷 | 乙醚 | 苯甲酸乙酯 |
| 密度/( g∙cm-3) | 0.7893 | 1.2659 | 0.7785 | 0.7318 | 1.0500 |
| 熔点/℃ | -114.0 | 122.1 | 6.5 | -116.3 | -34.6 |
| 沸点/℃ | 78.5 | 249.0 | 80.0 | 34.5 | 211.0~213.0 |
①在烧瓶C中加入一定量的下列物质(如下表)。按图甲所示安装好装置,加热烧瓶C.反应一段时间后,停止加热。
| 物质 | 苯甲酸 | 乙醇 | 环己烷 | 浓硫酸 |
| 用量 | 2.44g |  |  |  |
③用分液漏斗分出有机层,再用乙醚萃取水层中的残留产品,二者合并,加入图乙的烧瓶D中,加入沸石并加入无水硫酸镁,加热蒸馏,制得产品2.6mL。回答下列问题:
(1)仪器A的名称是
(2)苯甲酸与乙醇制备苯甲酸乙酯的化学方程式为
(3)环己烷、乙醇与水可形成共沸物,沸点为62.1℃,烧瓶C的最佳加热方式是
(4)Na2CO3的作用是
(5)采用图乙装置进行蒸馏操作,加入无水硫酸镁的目的是
(6)该制备方法中苯甲酸乙酯的产率是
您最近一年使用:0次
名校
9 . 钼酸铵[(NH4)2MoO4]是生产高纯度钼制品、钼催化剂、钼颜料等的基本原料。一种以钼精矿(主要含MoS2,还含有少量SiO2、As、Sn、P、Cu、Pb、CaO)为原料制备钼酸铵的工艺流程如图所示: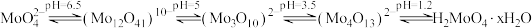 回答下列问题:
回答下列问题:
(1)锡为主族元素,在周期表中的位置是___________ ,(NH4)2MoO4中Mo元素的化合价为___________ 价。
(2)“氧化焙烧”时MoS2转化为MoO3,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)“除铜”时选择在60~80℃的条件下进行的原因为___________ 。
(4)“沉淀”过程中加入H2SO4调节溶液pH=2.1,则所得沉淀的化学式为___________ ,加入氨水后生成(NH4)2MoO4的化学方程式为___________ 。
(5)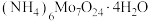 的热重曲线如图所示:
的热重曲线如图所示: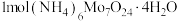 在A点失去H2O的物质的量为
在A点失去H2O的物质的量为___________ ,B点所得的物质为___________ (填化学式)。

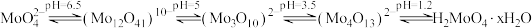 回答下列问题:
回答下列问题:(1)锡为主族元素,在周期表中的位置是
(2)“氧化焙烧”时MoS2转化为MoO3,该反应中氧化剂与还原剂的物质的量之比为
(3)“除铜”时选择在60~80℃的条件下进行的原因为
(4)“沉淀”过程中加入H2SO4调节溶液pH=2.1,则所得沉淀的化学式为
(5)
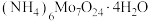 的热重曲线如图所示:
的热重曲线如图所示: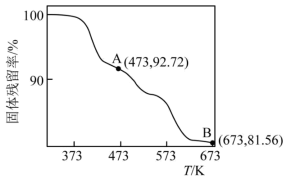
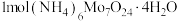 在A点失去H2O的物质的量为
在A点失去H2O的物质的量为
您最近一年使用:0次
10 . S2Cl2常温下是一种黄红色液体,沸点为137 ℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140 ℃反应制得。
Ⅰ.选用以下装置制取少量S2Cl2(加热及夹持装置已省略):
(1)A中发生反应的化学方程式为___________ 。
(2)装置的连接顺序为_________ 。
A→___________→__________→___________→___________。
(3)B中玻璃纤维的作用是___________ 。
(4)D装置的作用为___________ 。
Ⅱ.S2Cl2遇水会生成SO2气体、HCl和一种淡黄色固体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。___________ 。
(6)W溶液可以是___________ (填一种即可);若无溶液W,测得SO2体积分数会___________ 。
(7)该混合气体中SO2的体积分数为___________ (用含V、m的代数式表示)。
Ⅰ.选用以下装置制取少量S2Cl2(加热及夹持装置已省略):
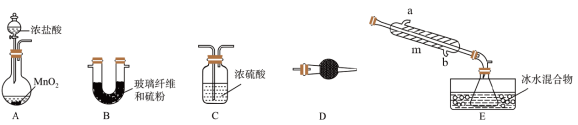
(1)A中发生反应的化学方程式为
(2)装置的连接顺序为
A→___________→__________→___________→___________。
(3)B中玻璃纤维的作用是
(4)D装置的作用为
Ⅱ.S2Cl2遇水会生成SO2气体、HCl和一种淡黄色固体,某同学设计了如下实验方案来测定该混合气体中SO2的体积分数。

(6)W溶液可以是
(7)该混合气体中SO2的体积分数为
您最近一年使用:0次




