1 . 下列图示与对应的叙述不相符的是
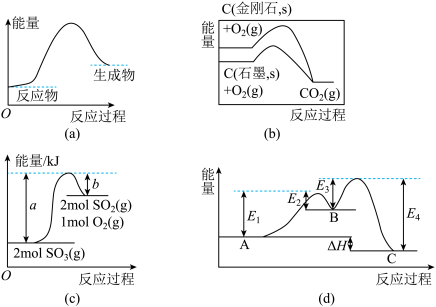
| A.(a)图表示反应物断键吸收的能量大于生成物成键放出的能量 |
B.(d)图是某反应:A→C(由两步反应A→B→C完成,B为中间产物)的能量曲线(E表示能量),整个反应中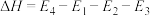 |
C.由(c)图可知,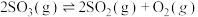 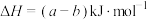 |
D.(b)图是金刚石与石墨分别被氧化生成CO2的能量关系曲线,说明石墨转化为金刚石的反应的 |
您最近一年使用:0次
名校
2 . SF6(结构如图所示)可用作高压发电系统的绝缘气体,分子呈八面体结构。下列说法正确的是
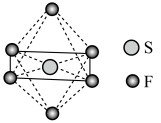
| A.未成对电子数:F>S |
| B.S难溶于CS2 |
| C.SF6中,F原子提供空轨道,S给出孤电子对 |
| D.相同条件下,在水中的溶解度:HF>H2S |
您最近一年使用:0次
名校
3 .  为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是
 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是A.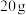 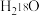 中含有的中子数为 中含有的中子数为 |
B.常温常压下,  和 和 的混合物中含有氧原子数为 的混合物中含有氧原子数为 |
C.  粉与足量氯气充分反应,转移电子数为 粉与足量氯气充分反应,转移电子数为 |
D.  与足量的水充分反应后的形成的 与足量的水充分反应后的形成的 分子数为 分子数为 |
您最近一年使用:0次
名校
解题方法
4 . 下列各组离子在给定溶液中能大量共存的是
A.在 醋酸溶液中: 醋酸溶液中: 、 、 、 、 、 、 |
B.在 氯化钠溶液中: 氯化钠溶液中: 、 、 、 、 、 、 |
C.在 氨水中: 氨水中: 、 、 、 、 、 、 |
D.在 硝酸银溶液中: 硝酸银溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
解题方法
5 . 下列关于反应能量的说法正确的是
| A.化学反应中的能最变化,全都表现为热量的变化 |
| B.化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C.需要加热才能进行的反应一定是吸热反应、放热反应不需要加热 |
| D.相同条件下1mol氢原子所具有的能量为E1,1mol氢分子的能量为E2,则2E1=E2 |
您最近一年使用:0次
名校
解题方法
6 . 中国化学家研究出一种新型复合光催化剂(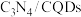 ),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是
),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是
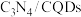 ),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是
),可以利用太阳光高效分解水其原理如图所示。下列说法错误的是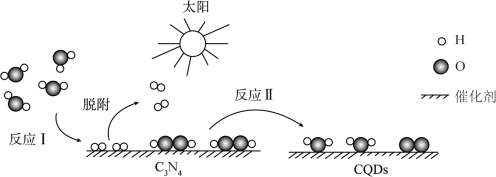
| A.反应Ⅰ是放热反应 |
| B.反应Ⅰ涉及极性键的断裂与非极性键的形成 |
C. 是中间产物, 是中间产物,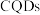 能催化其分解 能催化其分解 |
| D.整个过程实现了太阳能向化学能转化 |
您最近一年使用:0次
名校
7 . 硫的化合物有重要用途,硫代硫酸钠(Na2S2O3)可用于氰化物中毒的解毒和治疗荨麻疹等皮肤病,下列说法正确的是
| A.最高正化合价:Na<O=S | B.HCN中碳原子的杂化方式为sp |
| C.沸点:SO2>SO3 | D. 的空间结构与VSEPR模型相同 的空间结构与VSEPR模型相同 |
您最近一年使用:0次
8 . 几种晶体的晶胞(或晶体结构)如图所示,下列说法正确的是
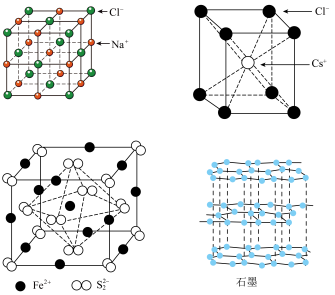
A. 中 中 的配位数大于干冰中 的配位数大于干冰中 分子的配位数 分子的配位数 |
B. 晶胞中,若 晶胞中,若 作顶点,则 作顶点,则 应在面心处 应在面心处 |
C.若 的晶胞边长为apm,其中S原子的半径为 的晶胞边长为apm,其中S原子的半径为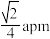 |
| D.石墨晶体层内作用力是共价键,层间作用力是范德华力,所以石墨是一种混合型晶体 |
您最近一年使用:0次
名校
9 . 化学反应中的能量变化,通常表现为热量的变化,研究化学反应中的热量变化具有重要的意义。
(1)下列变化属于吸热反应的是_______ (填序号)。
①液态水气化;②胆矾加热变成白色粉末;③浓硫酸稀释;④氢气还原氧化铜;⑤盐酸和碳酸氢钠反应;⑥氢氧化钾和稀硫酸反应;⑦灼热的木炭与 的反应;⑧
的反应;⑧ 晶体与
晶体与 晶体的反应;⑨甲烷在空气中燃烧的反应
晶体的反应;⑨甲烷在空气中燃烧的反应
(2)已知:
 ;
;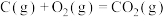
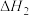
则
_______ 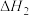 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(3)若
 ,则
,则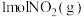 置于密闭容器中充分反应放出的热量
置于密闭容器中充分反应放出的热量_______ 28.45kJ(填“>”、“<”或“=”)。
(4)①已知:
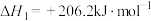

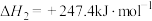
则 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为_______ 。
(5)用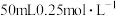 稀
稀 与
与 溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:_______ 。
②实验中若用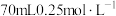 稀
稀 与
与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”)。
③已知:中和反应后生成的溶液的比热容 为
为 ,溶液的密度均为
,溶液的密度均为 ,某学习小组三次实验测得温度平均升高3.4℃。则生成
,某学习小组三次实验测得温度平均升高3.4℃。则生成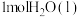 时放出的热量为
时放出的热量为_______ kJ。(结果保留一位小数)
④若上述实验所测中和热数值偏小,产生偏差的原因可能是_______ 。
a.实验装置保温、隔热效果差
b.量筒量取溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定 溶液的温度
溶液的温度
(1)下列变化属于吸热反应的是
①液态水气化;②胆矾加热变成白色粉末;③浓硫酸稀释;④氢气还原氧化铜;⑤盐酸和碳酸氢钠反应;⑥氢氧化钾和稀硫酸反应;⑦灼热的木炭与
 的反应;⑧
的反应;⑧ 晶体与
晶体与 晶体的反应;⑨甲烷在空气中燃烧的反应
晶体的反应;⑨甲烷在空气中燃烧的反应(2)已知:

 ;
;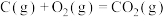
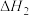
则

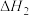 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(3)若

 ,则
,则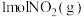 置于密闭容器中充分反应放出的热量
置于密闭容器中充分反应放出的热量(4)①已知:

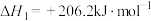

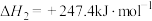
则
 与
与 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(5)用
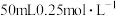 稀
稀 与
与 溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题:
溶液在如图所示的装置中进行反应。通过测定反应过程中所放出的热量可计算出中和反应反应热。回答下列问题: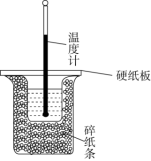
②实验中若用
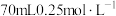 稀
稀 与
与 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量③已知:中和反应后生成的溶液的比热容
 为
为 ,溶液的密度均为
,溶液的密度均为 ,某学习小组三次实验测得温度平均升高3.4℃。则生成
,某学习小组三次实验测得温度平均升高3.4℃。则生成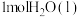 时放出的热量为
时放出的热量为④若上述实验所测中和热数值偏小,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量筒量取溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定
 溶液的温度
溶液的温度
您最近一年使用:0次
名校
解题方法
10 . 回答下列问题。
(1)下列化学反应可以设计成原电池的是_______。
(2)观察图,回答问题。_______ 能。
②Zn电极是_______ 极(填“正”或“负”)极,正极反应为_______ (填“氧化反应”或“还原反应”),电极反应式_______ 。
③电子移动方向_______ ,溶液中氢离子向_______ (填“正”或“负”)极移动。
④标准状况下,若反应过程中溶解了6.5g锌,则正极生成的产物的体积为_______ L。
(1)下列化学反应可以设计成原电池的是_______。
A. | B. |
C. | D. |
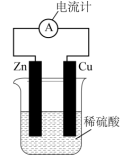
②Zn电极是
③电子移动方向
④标准状况下,若反应过程中溶解了6.5g锌,则正极生成的产物的体积为
您最近一年使用:0次



