名校
解题方法
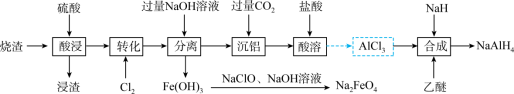
1 . NaAlH4是常用的还原剂;Na2FeO4常做净水剂和消毒剂。工业上以制备硫酸的烧渣(主要成分为Fe3O4、Fe2O3和Al2O3含少量SiO2)为原料制备NaAlH4和Na2FeO4的流程如下:
(1)NaAlH4中氢的化合价为___________ 。
(2)浸渣的主要成分是___________ (填化学式);“转化”中Cl2的作用是___________ (用离子方程式表示)。
(3)由Fe(OH)3制备Na2FeO4的离子方程式为___________ ;“分离”中铝元素转化成___________ (填离子符号)。
(4)“沉铝”后所得滤液经蒸干、灼烧得到固体是___________ 。
(5)“合成”中乙醚作溶剂,该过程发生反应的化学方程式为___________ 。
(6)“有效氢”指单位质量(1 g)含氢还原剂的还原能力相当于多少克氢气的还原能力,一般含氢还原剂的氢被氧化成H2O。则NaAlH4有效氢含量为___________ (计算结果保留三位有效数字)。
(1)NaAlH4中氢的化合价为
(2)浸渣的主要成分是
(3)由Fe(OH)3制备Na2FeO4的离子方程式为
(4)“沉铝”后所得滤液经蒸干、灼烧得到固体是
(5)“合成”中乙醚作溶剂,该过程发生反应的化学方程式为
(6)“有效氢”指单位质量(1 g)含氢还原剂的还原能力相当于多少克氢气的还原能力,一般含氢还原剂的氢被氧化成H2O。则NaAlH4有效氢含量为
您最近一年使用:0次
名校
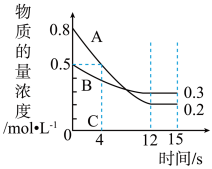
2 . 在体积固定为2 L的密闭容器中投入一定量的A和B,两种气体的物质的量浓度随时间变化的曲线如图所示,已知物质C也为气体。则:___________ (填“>”、“<”或“=”)逆反应速率;该反应达到最大限度的时间是___________ s。经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为___________ 。
(2)从反应开始到12 s内,A的转化率为___________ 。
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的反应速率分别为:甲:v(A)=0.3 mol·L-1·s-1;乙:v(B)=0.12 mol·L-1·s-1;丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为___________ (用甲、乙、丙表示)。
(4)一定能够判断该反应达到平衡状态的依据是___________ (填选项)。
A.该条件下,混合气体的密度不再发生变化
B.该条件下,混合气体的压强不再发生变化
C.该条件下,单位时间内消耗3 mol A的同时生成2 mol C
D.该条件下,n(A):n(B):n(C)=2:3:4
E.该条件下,混合气体颜色不再发生变化
(5)为加快上述反应速率的,可以改变的外界条件是___________ (写出一种即可)。
(2)从反应开始到12 s内,A的转化率为
(3)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,反应相同时间后,测得三个容器中的反应速率分别为:甲:v(A)=0.3 mol·L-1·s-1;乙:v(B)=0.12 mol·L-1·s-1;丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
(4)一定能够判断该反应达到平衡状态的依据是
A.该条件下,混合气体的密度不再发生变化
B.该条件下,混合气体的压强不再发生变化
C.该条件下,单位时间内消耗3 mol A的同时生成2 mol C
D.该条件下,n(A):n(B):n(C)=2:3:4
E.该条件下,混合气体颜色不再发生变化
(5)为加快上述反应速率的,可以改变的外界条件是
您最近一年使用:0次
名校
3 . 《Science》杂志报道了王浩天教授团队发明的制取H2O2的绿色方法,原理如图所示。下列说法正确的是
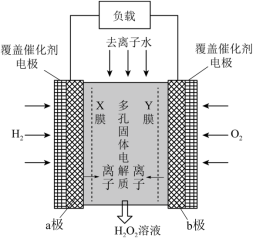
| A.该装置可实现由化学能向电能的转化 |
| B.a极为正极,发生还原反应 |
| C.X膜为阴离子交换膜(只允许阴离子通过) |
| D.当外电路通过4 mol e-时,消耗22.4 L O2(标准状况下) |
您最近一年使用:0次
4 . 下列有关除去杂质(括号内为杂质),所选试剂可行的是
| A.NO(NO2),蒸馏水 |
| B.CO2(SO2),饱和Na2CO3溶液 |
| C.CaO(CaCO3),稀盐酸 |
| D.FeCl3(FeCl2),Fe粉 |
您最近一年使用:0次
名校
5 . 如图是金属和卤素单质X2反应的能量变化示意图,下列说法正确的是
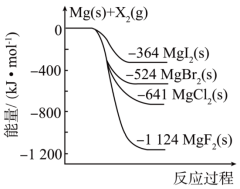
| A.稳定性:MgF2(s)>MgCl2(s)>MgBr2(s)>MgI2(s) |
| B.由MgI2(s)转化为MgCl2(s)需要吸收能量 |
| C.22.4 L F2(g)与足量Mg反应生成MgF2(s)放热1124 kJ |
| D.由图可知,MgBr2(s)分解吸收的能量比MgCl2(s)多 |
您最近一年使用:0次
名校
解题方法
6 . 工业制备高纯硅的主要过程如下,其中下列说法正确的是
石英砂 粗硅
粗硅 高纯硅
高纯硅
石英砂
 粗硅
粗硅 高纯硅
高纯硅| A.单晶硅是应用广泛的半导体材料,常用来生产光导纤维 |
B.制备粗硅的反应方程式为SiO2+C Si+CO2↑ Si+CO2↑ |
| C.原料气HCl和H2应充分去除水和氧气 |
| D.原料气中仅HCl可循环利用 |
您最近一年使用:0次
名校
7 . 现有下列几种有机物,其中叙述错误的是
① ②CH4 ③CH3CH2CH3 ④CH2=CH2 ⑤
②CH4 ③CH3CH2CH3 ④CH2=CH2 ⑤
| A.沸点②<③ |
| B.②有2种二氯代物 |
| C.①和⑤互为同分异构体 |
| D.⑤在一定条件下能和Cl2发生取代反应 |
您最近一年使用:0次
8 . 下列实验装置及操作能达到实验目的的是
|
|
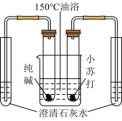
| A.测定新制氯水pH | B.实验室模拟侯氏制碱法 |
|
|
| C.稀释浓硫酸 | D.比较纯碱和小苏打的热稳定性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 下列微粒在指定溶液中能大量共存的是
A.pH=1的溶液中: |
B.某透明溶液中: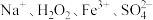 |
C.饱和食盐水中: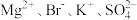 |
D.强碱性溶液中: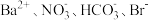 |
您最近一年使用:0次
名校
10 . NA为阿伏加德罗常数的值。下列叙述正确的是
| A.标况下11.2 L CH4和22.4 L Cl2在光照条件下充分反应后的分子数为1.5 NA |
| B.1 mol NH4Cl晶体中含有共价键数目为3NA |
C.18 g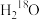 中含有中子数为10NA 中含有中子数为10NA |
| D.100 mL 0.1 mol · L-1 NaOH溶液中O原子数目为0.01NA |
您最近一年使用:0次