相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则下列关于同温、同体积、同浓度的HCN和HClO的说法正确的是
| A.酸的强弱:HCN<HClO |
| B.pH:HClO>HCN |
| C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
| D.酸根离子浓度:c平(CN-)<c平(ClO-) |
更新时间:2023-08-27 12:10:21
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向一密闭容器充入 ,保持温度不变,慢慢扩大容器体积 ,保持温度不变,慢慢扩大容器体积 | 平衡后容器中气体颜色比开始浅 |  平衡逆向移动 平衡逆向移动 |
B | 向两支均盛有 溶液的试管中分别滴加硼酸、盐酸 溶液的试管中分别滴加硼酸、盐酸 | 滴加盐酸的试管产生气泡,滴加硼酸的试管无明显现象 | 酸性: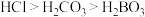 |
C | 向滴有酚酞的氨水中加入 固体 固体 | 溶液的红色变浅 |  溶液呈酸性 溶液呈酸性 |
D | 铁锈溶于浓盐酸,将所得溶液加入酸性 溶液中 溶液中 | 紫色褪去 | 铁锈中含有二价铁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】已知部分弱电解质的电离平衡常数如下表:
常温下,下列分析正确的是
| 弱电解质 | CH3COOH | H2CO3 | HClO | NH3∙H2O |
| 电离平衡常数 (25℃) | 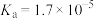 |   |  |  |
| A.pH相同的①CH3COONa②NaHCO3③NaClO溶液中的c(Na+):③>②>① |
B.0.1 mol∙L-1CH3COONH4溶液中:c( )=c(CH3COO-) )=c(CH3COO-) |
| C.中和等体积等浓度的醋酸和次氯酸,需要NaOH的物质的量相同 |
D.反应 + CH3COOH = CH3COO-+ H2CO3,K=2.4×10-3 + CH3COOH = CH3COO-+ H2CO3,K=2.4×10-3 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐3】已知:①pOH=-lgc(OH-);②N2H4+H2O N2H5++OH-、N2H5++H2O
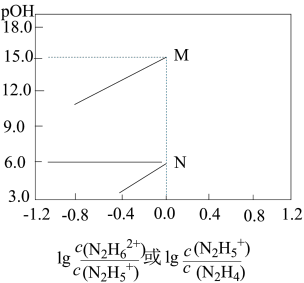
N2H5++OH-、N2H5++H2O N2H62++OH-,分别对应有pOH1和pOH2。常温下,将盐酸滴加到N2H4的水溶液中,混合溶液中pOH随离子浓度变化的关系如图所示。下列叙述错误的是
N2H62++OH-,分别对应有pOH1和pOH2。常温下,将盐酸滴加到N2H4的水溶液中,混合溶液中pOH随离子浓度变化的关系如图所示。下列叙述错误的是
 N2H5++OH-、N2H5++H2O
N2H5++OH-、N2H5++H2O N2H62++OH-,分别对应有pOH1和pOH2。常温下,将盐酸滴加到N2H4的水溶液中,混合溶液中pOH随离子浓度变化的关系如图所示。下列叙述错误的是
N2H62++OH-,分别对应有pOH1和pOH2。常温下,将盐酸滴加到N2H4的水溶液中,混合溶液中pOH随离子浓度变化的关系如图所示。下列叙述错误的是
A.曲线M表示 变化关系 变化关系 |
| B.N2H4与硫酸形成的酸式盐的化学式为N2H5HSO4 |
| C.pOH1>pOH2 |
D.反应N2H5++ H2O N2H62++ OH-的K=10-15 N2H62++ OH-的K=10-15 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】常温下,向含少量HCl的0.1mol⋅L-1CrCl3溶液中逐滴滴加NaOH溶液,所加NaOH溶液的体积V(NaOH)与溶液pH变化关系如图所示。(已知:图中C点Cr3+浓度为10-5mol⋅L-1;Cr(OH)3+OH-=[Cr(OH)4]-)

下列说法错误的是

下列说法错误的是
| A.AB段发生了:H++OH-=H2O |
| B.A到D过程中,水的电离程度先增大后减小 |
| C.溶液pH=4.4时,c(Cr3+)=1.0×10-2mol⋅L-1 |
| D.D点溶液中c(Cl-)>c(Na+)>c([Cr(OH)4]-)>c(OH-)>c(H+) |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】NaClO溶液具有漂白能力,已知25℃时Ka(HClO)=4.0×10-8。下列关于NaClO溶液说法不正确的是
| A.0.01mol/L NaClO溶液中,c(ClO-)<0.01mol/L |
| B.长期露置在空气中,释放Cl2,漂白能力减弱 |
C.通入过量SO2,反应的离子方程式为SO2+ClO-+H2O=SO +2H++Cl- +2H++Cl- |
| D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)<c(ClO-)=c(Na+) |
您最近一年使用:0次
【推荐3】下列实验操作或设计与实验现象、结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 取少量某溶液于试管中,加入 浓溶液并加热,用湿润的红色石蕊试纸检验产生的气体 浓溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 湿润的红色石蕊试纸变蓝 | 溶液中一定含有 |
| B | 向 浓度为 浓度为 的 的 溶液中逐滴加入等浓度的 溶液中逐滴加入等浓度的 溶液 溶液 | 溶液褪色 |  漂白溶液,表现强氧化性 漂白溶液,表现强氧化性 |
| C | 取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入适量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入适量 溶液 溶液 | 白色沉淀产生 | 样品已经变质 |
| D | 室温下,用 试纸分别测定浓度均为 试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 溶液 : : 约为9, 约为9, 约为10 约为10 | 酸性: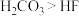 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】25℃时,Ka(CH3COOH)=1.8×10-5,Kb(NH3·H2O)=1.8×10-5。室温时,下列关于指定溶液的说法正确的是
| A.0.1mol·L-1CH3COOH溶液:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) |
B.0.1mol·L-1CH3COONH4溶液:c( )=c(CH3COO-)>c(H+)=c(OH-) )=c(CH3COO-)>c(H+)=c(OH-) |
C.将0.1mol·L-1CH3COOH溶液和0.1mol·L-1NH3·H2O溶液按一定体积比混合,混合溶液中:c( )+c(H+)=c(CH3COO-)+c(OH-) )+c(H+)=c(CH3COO-)+c(OH-) |
D.0.1mol·L-1CH3COOH溶液与0.1mol·L-1CH3COONH4溶液等体积混合的溶液:c( )+c(NH3·H2O)=2c(CH3COO-)+2c(CH3COOH) )+c(NH3·H2O)=2c(CH3COO-)+2c(CH3COOH) |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】室温下,向一定体积的0.1mol·L-1的Na2CO3溶液中逐滴加入0.1mol·L-1盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示(CO2因逸出未画出,滴加盐酸的过程中温度的变化忽略不计)。下列说法正确的是
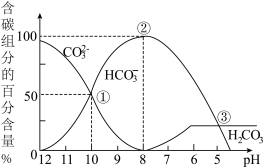

| A.由图可知,碳酸的-lgKa2=10 |
B.点②所示溶液中:c(HCO )=0.1mol·L-1 )=0.1mol·L-1 |
| C.当滴加盐酸到点③时,才开始放出CO2气体 |
| D.Na2CO3第一步水解反应的平衡常数:①=②=③ |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】下列各溶液中,微粒的物质的量浓度关系正确的是( )
| A.(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) |
| B.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(OH-)>c(H2CO3)>c(CO32-) |
| C.0.1mol/L的NH4Cl溶液与0.05mol/L的NaOH溶液等体积混合:c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+) |
| D.c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:c(NH4)2SO4<c(NH4)2CO3<c(NH4Cl) |
您最近一年使用:0次



