若HA为一元弱酸,MOH为一元弱碱,已知:MA水解常数为Kh,HA的电离常数为Ka,MOH的电离常数Kb,水的离子积为KW试推导Kh、Ka、Kb、KW之间的关系___________ 。
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-08-27 09:47:32
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】水溶液存在离子平衡,回答下列问题:
(1)AlCl3 水溶液呈______ (填“酸”、“中”、“碱”)性 ,原因是(用离子方程式):________ ;把 AlCl3 溶液加热蒸干,灼烧,最后得到的主要固体产物是________ 。
(2)为防止 FeSO4 溶液变质,在保存时需加入的试剂为__________ (填试剂名称)
(3)已知 25 ℃时,纯水中 c(OH-)为 10-7mol·L-1,则:
①该温度时水的离子积常数 Kw=___________ 。
②该温度下,将 pH=3 的 H2SO4 溶液与 pH=11 的 NaOH 溶液按等体积混合,所得混合溶液的 pH 为______ 。
(4)常温下,在 25mL 的氢氧化钠溶液中逐滴加入 0.2 mol·L-1 醋酸溶液,滴定曲线如图所示。

①该氢氧化钠溶液浓度为________ 。
②在 B 点,溶液中离子浓度大小关系为_______ 。
③在 D 点,c(CH3COO-)_________ c(Na+) (填“<”“>”或“=”)。
(1)AlCl3 水溶液呈
(2)为防止 FeSO4 溶液变质,在保存时需加入的试剂为
(3)已知 25 ℃时,纯水中 c(OH-)为 10-7mol·L-1,则:
①该温度时水的离子积常数 Kw=
②该温度下,将 pH=3 的 H2SO4 溶液与 pH=11 的 NaOH 溶液按等体积混合,所得混合溶液的 pH 为
(4)常温下,在 25mL 的氢氧化钠溶液中逐滴加入 0.2 mol·L-1 醋酸溶液,滴定曲线如图所示。

①该氢氧化钠溶液浓度为
②在 B 点,溶液中离子浓度大小关系为
③在 D 点,c(CH3COO-)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知水在25 ℃和95 ℃时的电离平衡曲线如图所示:

(1)25 ℃时水的电离平衡曲线应为__________ (填“A”或“B”)。
(2)95 ℃时水的离子积Kw=__________ ,cH+==__________
(3)25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为_____ 。
(4)95 ℃时,若100 mL pH1=a的某强酸溶液与1 mL pH2=b的某强碱溶液混合后,所得溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是____ 。
(5)在曲线B对应的温度下,将pH=2的某HA溶液和pH=10的NaOH溶液等体积混合,所得溶液的pH=5。请分析其原因:_________________ 。

(1)25 ℃时水的电离平衡曲线应为
(2)95 ℃时水的离子积Kw=
(3)25 ℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为
(4)95 ℃时,若100 mL pH1=a的某强酸溶液与1 mL pH2=b的某强碱溶液混合后,所得溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
(5)在曲线B对应的温度下,将pH=2的某HA溶液和pH=10的NaOH溶液等体积混合,所得溶液的pH=5。请分析其原因:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在不同温度下的水溶液中离子浓度曲线如图所示。

(1)图中T1___________ T2(填写“>”,“<”或“=”)
(2)C点溶液的性质___________ 。(填写“酸性”、“碱性”或“中性”)
(3)将D点变为E点,采取的措施是___________ 。
(4)在48mL0.1mol/LHNO3溶液中加入12mL0.4mol/LKOH溶液,所得溶液呈
(5)用已知浓度HCl溶液滴定未知浓度NaOH溶液,选用酚酞做指示剂,
①判断滴定终点到达时的现象为___________ 。
②若出现下列情况,测定结果偏高的是___________ (选填字母序号)
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失

(1)图中T1
(2)C点溶液的性质
(3)将D点变为E点,采取的措施是
(4)在48mL0.1mol/LHNO3溶液中加入12mL0.4mol/LKOH溶液,所得溶液呈
| A.弱酸性 | B.强酸性 | C.碱性 | D.中性 |
①判断滴定终点到达时的现象为
②若出现下列情况,测定结果偏高的是
a.滴定前用蒸馏水冲洗锥形瓶
b.滴定过程中振荡锥形瓶时不慎将瓶内溶液溅出
c.滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管在滴定前有气泡,滴定后气泡消失
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示:
(1)根据上表可知,酸性
_____  ,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3
,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3_____ Na2SO3。(填“>” “<”或 “=”,下同)
(2)向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是______ 。
A NaCl溶液 B Na2CO3固体 C NH4Cl溶液 D CH3COONa固体
(3)已知常温下NH3∙H2O的电离常数 ,则常温下CH3COONH4溶液的pH
,则常温下CH3COONH4溶液的pH_______ 7。
(4)将pH=4的 溶液稀释100倍后溶液的pH范围是
溶液稀释100倍后溶液的pH范围是_______ ,图中的纵坐标可以是______ 。

a.溶液的pH
b.醋酸的电离平衡常数
c.溶液的导电能力
d.醋酸的电离程度
(5)NaHSO3是中学化学常见的物质。 在水溶液中存在如下两个平衡:
在水溶液中存在如下两个平衡:
 Ka2
Ka2
 Kh2 (水解平衡常数,表示水解程度)
Kh2 (水解平衡常数,表示水解程度)
已知25 ℃时,Ka2 > Kh2,则0.1 mol∙L−1 NaHSO3溶液:
①溶液呈__________ (填“酸性”“碱性”或“中性”);
②溶液中c(Na+)______ c( )(填“>”“<”或“=”);
)(填“>”“<”或“=”);
③写出该溶液中的守恒式:
电荷守恒:_____________ ,物料守恒:________________ ,质子守恒:_______________ 。
| 酸 | 电离平衡常数 |
| 醋酸 | 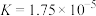 |
| 碳酸 | 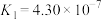 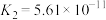 |
| 亚硫酸 |   |
(1)根据上表可知,酸性

 ,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3
,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3(2)向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是
A NaCl溶液 B Na2CO3固体 C NH4Cl溶液 D CH3COONa固体
(3)已知常温下NH3∙H2O的电离常数
 ,则常温下CH3COONH4溶液的pH
,则常温下CH3COONH4溶液的pH(4)将pH=4的
 溶液稀释100倍后溶液的pH范围是
溶液稀释100倍后溶液的pH范围是
a.溶液的pH
b.醋酸的电离平衡常数
c.溶液的导电能力
d.醋酸的电离程度
(5)NaHSO3是中学化学常见的物质。
 在水溶液中存在如下两个平衡:
在水溶液中存在如下两个平衡: Ka2
Ka2 Kh2 (水解平衡常数,表示水解程度)
Kh2 (水解平衡常数,表示水解程度)已知25 ℃时,Ka2 > Kh2,则0.1 mol∙L−1 NaHSO3溶液:
①溶液呈
②溶液中c(Na+)
 )(填“>”“<”或“=”);
)(填“>”“<”或“=”);③写出该溶液中的守恒式:
电荷守恒:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】硫及其化合物在人类生产生活中起着重要作用。回答下列问题:
(1)基态S原子的价层电子轨道表示式为__________ ,其原子核外电子共有__________ 种空间运动状态。
(2)已知:25℃时 的电离常数:
的电离常数: ,
,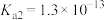 ,则
,则 的水解常数
的水解常数
__________ , 溶液的pH
溶液的pH______ 7(填“>”“<”或“=”)。
(3)锅炉水垢既会降低燃料的利用率,义会影响锅炉的使用寿命。为了除去水垢中的 可先用
可先用 溶液处理,写出该反应的离子方程式:
溶液处理,写出该反应的离子方程式:__________ 。
(4)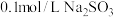 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是__________ 。
(1)基态S原子的价层电子轨道表示式为
(2)已知:25℃时
 的电离常数:
的电离常数: ,
,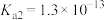 ,则
,则 的水解常数
的水解常数
 溶液的pH
溶液的pH(3)锅炉水垢既会降低燃料的利用率,义会影响锅炉的使用寿命。为了除去水垢中的
 可先用
可先用 溶液处理,写出该反应的离子方程式:
溶液处理,写出该反应的离子方程式:(4)
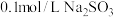 溶液中各种离子浓度由大到小的顺序是
溶液中各种离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】I、(1)25℃时,有浓度均为0.1 mol·L-1的6种溶液:①Ba(OH)2,②CH3OOH, ③HCl,④Na2CO3,⑤NH4Cl,⑥KCl溶液pH由小到大的顺序为_________ (填写编号)。
(2)25℃时,pH=4的CH3COOH溶液中,由水电离出的c(H+)=_____ mol/L;往溶液中加入少量NaOH固体(不考虑温度变化),则溶液中 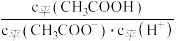
_____ (填“增大”、“减小”或“不变”)。
II、某实验小组拟用pH试纸验证醋酸是弱酸。甲、乙两同学的方案分别是:
甲:①准确配制0.1mol·L-1的醋酸钠溶液100mL;
②用pH试纸测出该溶液的pH,即可证明醋酸是弱酸。
乙:①量取一定量的冰醋酸准确配制pH=1的醋酸溶液100mL;
②取醋酸溶液1mL,加水稀释为10mL;
③用pH试纸测出②中溶液的pH,即可证明醋酸是弱酸。
(3)乙方案中,说明醋酸是弱酸的理由是测得醋酸溶液的pH____ 2(选填“<”“>”或“=”,下同),甲方案中,说明醋酸是弱酸的理由是测得醋酸钠溶液的pH____ 7。
(4)请你结合所学知识再列举一种方法证明醋酸是弱酸:__________________ 。
(2)25℃时,pH=4的CH3COOH溶液中,由水电离出的c(H+)=
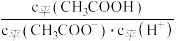
II、某实验小组拟用pH试纸验证醋酸是弱酸。甲、乙两同学的方案分别是:
甲:①准确配制0.1mol·L-1的醋酸钠溶液100mL;
②用pH试纸测出该溶液的pH,即可证明醋酸是弱酸。
乙:①量取一定量的冰醋酸准确配制pH=1的醋酸溶液100mL;
②取醋酸溶液1mL,加水稀释为10mL;
③用pH试纸测出②中溶液的pH,即可证明醋酸是弱酸。
(3)乙方案中,说明醋酸是弱酸的理由是测得醋酸溶液的pH
(4)请你结合所学知识再列举一种方法证明醋酸是弱酸:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】25℃时,H2SO3
 +H+的电离常数 Ka=1×10-2mol/L,则该温度下 NaHSO3的水解平衡常数Kh=
+H+的电离常数 Ka=1×10-2mol/L,则该温度下 NaHSO3的水解平衡常数Kh= _______ mol/L。

 +H+的电离常数 Ka=1×10-2mol/L,则该温度下 NaHSO3的水解平衡常数Kh=
+H+的电离常数 Ka=1×10-2mol/L,则该温度下 NaHSO3的水解平衡常数Kh=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】平衡移动原理在实验、生活、生产中应用广泛。回答下列问题:

(1)实验室配制 溶液时需将
溶液时需将 粉末加浓盐酸进行溶解,请用平衡移动原理解释原因:
粉末加浓盐酸进行溶解,请用平衡移动原理解释原因:___________ [已知: 水解生成
水解生成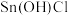 ]。
]。
(2)泡沫灭火器里的药品是 溶液和
溶液和 溶液,其工作原理为
溶液,其工作原理为___________ (用离子方程式表示)。泡沫灭火器有内筒(塑料材质)和外筒(钢质)两部分组成,外筒放入的药品是___________ (填化学式)。
(3)只用一种试剂就可以鉴别下列溶液: 溶液、
溶液、 溶液、
溶液、 溶液。该试剂为
溶液。该试剂为___________ 。
(4)相同物质的量浓度的下列溶液:① 、②
、② 、③
、③ 、④
、④ ,
,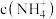 由大到小的顺序是
由大到小的顺序是___________ (用序号表示)。
(5)向少量 悬浊液中加入适量的饱和
悬浊液中加入适量的饱和 溶液,结果固体完全溶解,固体溶解的原因可能是:
溶液,结果固体完全溶解,固体溶解的原因可能是:
猜想甲:①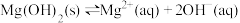
②
③
结论:由于③反应的发生,使反应①平衡正向移动, 溶解。
溶解。
猜想乙:①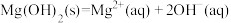
②___________
结论:由于②反应的发生,___________ 。
(6)设计一个简单的实验方案证明纯碱溶液中存在水解平衡:向盛有碳酸钠溶液的试管中滴入几滴酚酞溶液,振荡,溶液变红,___________ ,证明纯碱溶液中存在水解平衡。已知25℃时,Na2CO3溶液的第一步水解常数Kh=2×10-4,则当溶液pH=10时
___________ 。

(1)实验室配制
 溶液时需将
溶液时需将 粉末加浓盐酸进行溶解,请用平衡移动原理解释原因:
粉末加浓盐酸进行溶解,请用平衡移动原理解释原因: 水解生成
水解生成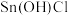 ]。
]。(2)泡沫灭火器里的药品是
 溶液和
溶液和 溶液,其工作原理为
溶液,其工作原理为(3)只用一种试剂就可以鉴别下列溶液:
 溶液、
溶液、 溶液、
溶液、 溶液。该试剂为
溶液。该试剂为(4)相同物质的量浓度的下列溶液:①
 、②
、② 、③
、③ 、④
、④ ,
,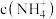 由大到小的顺序是
由大到小的顺序是(5)向少量
 悬浊液中加入适量的饱和
悬浊液中加入适量的饱和 溶液,结果固体完全溶解,固体溶解的原因可能是:
溶液,结果固体完全溶解,固体溶解的原因可能是:猜想甲:①
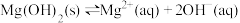
②

③

结论:由于③反应的发生,使反应①平衡正向移动,
 溶解。
溶解。猜想乙:①
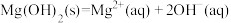
②
结论:由于②反应的发生,
(6)设计一个简单的实验方案证明纯碱溶液中存在水解平衡:向盛有碳酸钠溶液的试管中滴入几滴酚酞溶液,振荡,溶液变红,

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】运用化学反应原理,研究硫、磷化合物的反应具有重要意义。
(1)已知H3PO2(次磷酸)的水溶液中存在H3PO2分子。H3PO2与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为_____ ,该盐属于_____ (填“正盐”或“酸式盐”)。H3PO2易被氧化为H3PO4,已知常温下,H3PO4的电离常数为Ka1=6.9×10-3,Ka2=6.2×10-8,Ka3=4.8×10-13,请利用以上数据计算推测Na2HPO4溶液呈_____ 性。
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡_____ (填“向左”“向右”或“不”)移动。试计算该溶液中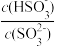 =
=_____ (常温下,H2SO3的电离平衡常数Ka1=1.0×10-2,Ka2=6.0×10-8)。
(3)化工生产中常用FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(aq)+FeS(s) CuS(s)+Fe2+(aq)。下列有关叙述正确的是
CuS(s)+Fe2+(aq)。下列有关叙述正确的是_____ 。
a.Ksp(FeS)<Ksp(CuS)
b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量Na2S固体后,溶液中c(Fe2+)、c(Cu2+)都减小
d.该反应平衡常数K= 。
。
(1)已知H3PO2(次磷酸)的水溶液中存在H3PO2分子。H3PO2与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,则生成盐的化学式为
(2)常温下,用NaOH溶液吸收SO2得到pH=9的Na2SO3溶液,吸收过程中水的电离平衡
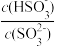 =
=(3)化工生产中常用FeS作沉淀剂除去工业废水中的Cu2+,其反应原理为Cu2+(aq)+FeS(s)
 CuS(s)+Fe2+(aq)。下列有关叙述正确的是
CuS(s)+Fe2+(aq)。下列有关叙述正确的是a.Ksp(FeS)<Ksp(CuS)
b.达到平衡时c(Fe2+)=c(Cu2+)
c.溶液中加入少量Na2S固体后,溶液中c(Fe2+)、c(Cu2+)都减小
d.该反应平衡常数K=
 。
。
您最近一年使用:0次



