已知Ka(CH3COOH)=1.75×10-5,试计算0.1 mol·L-1 CH3COOH溶液中H+的浓度(写出计算过程) ______ 。
23-24高二上·全国·课时练习 查看更多[1]
更新时间:2023-08-27 16:26:33
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】按要求完成下列填空。
(1)H2SO3在水溶液中的电离方程式____ 。
(2)NH4HSO4在水溶液中的电离方程式____ 。
(3)AlCl3在水溶液中的电离方程式____ 。
(4)NaHCO3在水溶液中的电离方程式____ 。
(5)H2CO3溶液中各种含碳微粒(不考虑CO2)以及氢离子的浓度由大到小的顺序为:____ 。
(1)H2SO3在水溶液中的电离方程式
(2)NH4HSO4在水溶液中的电离方程式
(3)AlCl3在水溶液中的电离方程式
(4)NaHCO3在水溶液中的电离方程式
(5)H2CO3溶液中各种含碳微粒(不考虑CO2)以及氢离子的浓度由大到小的顺序为:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡.根据要求回答问题
(1)生活中明矾常作净水剂,其净水的原理是___________ (用离子方程式表示).
(2)物质的量浓度相同的CH3COOH 溶液和NaOH 溶液混合后,溶液中c(CH3COO‾)=c(Na+),则CH3COOH 溶液的体积_____ NaOH 溶液的体积.(填“大于”、“小于”或“等于”.)
(3)常温下,取0.2mol•L﹣1 HCl溶液与0.2mol•L﹣1 MOH溶液等体积混合,测得混合溶液后的pH=5.写出MOH的电离方程式:_______________________ .
(4)含 的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的
的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的 .为了使废水的排放达标,进行如下处理:
.为了使废水的排放达标,进行如下处理:
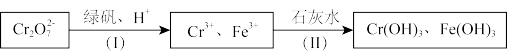
①绿矾为FeSO4•7H2O.反应(I)中Cr2O72﹣与FeSO4的物质的量之比为_____ .
②常温下若处理后的废水中c(Cr3+)=6.0×10﹣7 mol•L﹣1,则处理后的废水的pH=_____ (Ksp[Cr(OH)3]=6.0×10﹣31)
(1)生活中明矾常作净水剂,其净水的原理是
(2)物质的量浓度相同的CH3COOH 溶液和NaOH 溶液混合后,溶液中c(CH3COO‾)=c(Na+),则CH3COOH 溶液的体积
(3)常温下,取0.2mol•L﹣1 HCl溶液与0.2mol•L﹣1 MOH溶液等体积混合,测得混合溶液后的pH=5.写出MOH的电离方程式:
(4)含
 的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的
的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的 .为了使废水的排放达标,进行如下处理:
.为了使废水的排放达标,进行如下处理: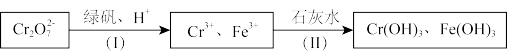
①绿矾为FeSO4•7H2O.反应(I)中Cr2O72﹣与FeSO4的物质的量之比为
②常温下若处理后的废水中c(Cr3+)=6.0×10﹣7 mol•L﹣1,则处理后的废水的pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】结合水溶液中离子平衡的相关知识回答下列问题:
Ⅰ.已知室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
(1)该溶液c(H+)=_______ ,pH值为_______ 。
(2)HA的电离平衡常数表达式K=_______ 。
Ⅱ.
(3)用离子方程式解释0.1 mol•L-1 Na2CO3溶液呈碱性的原因_______ 。
(4)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红。说明该溶液中HSO 的电离程度
的电离程度_______ HSO 的水解程度。(填“>”、“=”、“<”)。
的水解程度。(填“>”、“=”、“<”)。
Ⅰ.已知室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,回答下列各问题:
(1)该溶液c(H+)=
(2)HA的电离平衡常数表达式K=
Ⅱ.
(3)用离子方程式解释0.1 mol•L-1 Na2CO3溶液呈碱性的原因
(4)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红。说明该溶液中HSO
 的电离程度
的电离程度 的水解程度。(填“>”、“=”、“<”)。
的水解程度。(填“>”、“=”、“<”)。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知 时,HCOOH:
时,HCOOH: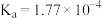 ,HCN:
,HCN: 。
。
(1)相同条件下,等浓度、等体积的HCOOH和HCN,导电性HCOOH_______ HCN,完全中和两溶液所需NaOH的物质的量HCOOH_______ HCN (填>、<或=)。
(2)一定浓度的稀HCN溶液,能使HCN电离程度增大的是_______ ,能使溶液酸性增强的是_______ (以上均填字母代号)
a.滴加少量浓度更大的HCN溶液 b.加水稀释 c.加入少量NaCN固体 d.加入少量NaOH固体
(3)下列反应不能发生的是_______
 时,HCOOH:
时,HCOOH: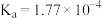 ,HCN:
,HCN: 。
。(1)相同条件下,等浓度、等体积的HCOOH和HCN,导电性HCOOH
(2)一定浓度的稀HCN溶液,能使HCN电离程度增大的是
a.滴加少量浓度更大的HCN溶液 b.加水稀释 c.加入少量NaCN固体 d.加入少量NaOH固体
(3)下列反应不能发生的是_______
A. |
B. |
C.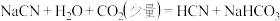 |
D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】按要求科学表达下列化学用语:
(1)含20.0gNaOH的稀溶液与稀硫酸反应,放出28.7kJ的热量,表示该反应中和热的热化学反应方程式:___ 。
(2)碱性锌锰电池总反应为:2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2,写出负极电板反应__ 。
(3)氨在催化剂作用下与氧气反应生成一氧化氮,写出其化学反应方程式___ 。
(4)根据下表提供的数据,写出往NaClO溶液中通入少量CO2的离子方程式__ 。
(1)含20.0gNaOH的稀溶液与稀硫酸反应,放出28.7kJ的热量,表示该反应中和热的热化学反应方程式:
(2)碱性锌锰电池总反应为:2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2,写出负极电板反应
(3)氨在催化剂作用下与氧气反应生成一氧化氮,写出其化学反应方程式
(4)根据下表提供的数据,写出往NaClO溶液中通入少量CO2的离子方程式
| 化学式 | 电离常数 |
| HClO | K1=3×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
您最近一年使用:0次



