按要求完成下列填空。
(1)H2SO3在水溶液中的电离方程式____ 。
(2)NH4HSO4在水溶液中的电离方程式____ 。
(3)AlCl3在水溶液中的电离方程式____ 。
(4)NaHCO3在水溶液中的电离方程式____ 。
(5)H2CO3溶液中各种含碳微粒(不考虑CO2)以及氢离子的浓度由大到小的顺序为:____ 。
(1)H2SO3在水溶液中的电离方程式
(2)NH4HSO4在水溶液中的电离方程式
(3)AlCl3在水溶液中的电离方程式
(4)NaHCO3在水溶液中的电离方程式
(5)H2CO3溶液中各种含碳微粒(不考虑CO2)以及氢离子的浓度由大到小的顺序为:
更新时间:2022-09-29 19:03:44
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】现有下列物质:①铜 ②硫酸溶液③CO2 ④NaHCO3固体 ⑤Ba(OH)2固体 ⑥熔化的KNO3 ⑦Na2CO3•10H2O晶体 ⑧红褐色的氢氧化铁胶体 ⑨氨水 ⑩稀硝酸
(1)上述物质属于电解质的有___________ (填编号,有错不给分)。
(2)写出④的电离方程式___________ ,⑤的电离方程式___________ 。
(3)上述物质中有两种物质之间可发生离子反应:H++OH-= H2O,写出该离子反应对应的化学方程式___________ 。
(4)制取⑧的化学方程式___________ ;将④的溶液滴加到NaOH溶液中反应的离子方程式___________ 。
(5)在电解质溶液的导电性实验中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是___________
(1)上述物质属于电解质的有
(2)写出④的电离方程式
(3)上述物质中有两种物质之间可发生离子反应:H++OH-= H2O,写出该离子反应对应的化学方程式
(4)制取⑧的化学方程式
(5)在电解质溶液的导电性实验中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是___________
| A.盐酸中逐滴加入氢氧化钠溶液 | B.硫酸铜溶液中逐滴加入氢氧化钡溶液 |
| C.硫酸中逐滴加入氯化钡溶液 | D.盐酸中逐滴加入硝酸银溶液 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求填空
现有以下物质:①NaHCO3溶液 ②干冰 ③CaCO3固体 ④HCl ⑤Fe(OH)3 胶体 ⑥铜 ⑦熔融Na2O ⑧Ba(OH)2固体 ⑨蔗糖 ⑩稀硫酸
(1)上述物质中能导电的是_______ (填序号,下同),属于电解质的是_______ ;属于非电解质的是_______ ;
(2)写出①的电离方程式:_______ ;
(3)写出④的水溶液与③反应的离子方程式:_______ ;氢氧化钡溶液和稀硫酸(写出离子方程式)_______ 。
(4)CO + 2H+ = CO2↑+ H2O(写出对应的化学方程式)
+ 2H+ = CO2↑+ H2O(写出对应的化学方程式)_______ 。
(5)实验室制备物质⑤的方法为:在烧杯中加入适量蒸馏水,加热煮沸,向沸水中逐滴加入几滴_______ 溶液,继续煮沸至溶液呈_______ 色,即制得Fe(OH)3胶体。
现有以下物质:①NaHCO3溶液 ②干冰 ③CaCO3固体 ④HCl ⑤Fe(OH)3 胶体 ⑥铜 ⑦熔融Na2O ⑧Ba(OH)2固体 ⑨蔗糖 ⑩稀硫酸
(1)上述物质中能导电的是
(2)写出①的电离方程式:
(3)写出④的水溶液与③反应的离子方程式:
(4)CO
 + 2H+ = CO2↑+ H2O(写出对应的化学方程式)
+ 2H+ = CO2↑+ H2O(写出对应的化学方程式)(5)实验室制备物质⑤的方法为:在烧杯中加入适量蒸馏水,加热煮沸,向沸水中逐滴加入几滴
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】现有以下物质:①铁②稀硝酸 ③硫酸氢钠④氢硫酸 ⑤冰醋酸⑥蔗糖溶液⑦三氧化硫气体⑧硫酸钡晶体。回答下列问题(用相应物质序号填写):
(1)属于弱电解质的有__________________________ 。
(2)写出⑧的溶解平衡的离子方程式__________________________ 。
(3)写出③熔融状态下的电离方程式__________________________ 。
(4)写出④在水中的电离方程式__________________________ 。
(1)属于弱电解质的有
(2)写出⑧的溶解平衡的离子方程式
(3)写出③熔融状态下的电离方程式
(4)写出④在水中的电离方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】25℃时,部分物质的电离平衡常数如下表所示:
(1)NH3·H2O的电离方程式是_______ ,25℃时,物质的量浓度为0.10mol/L的氨水中,c(OH-)为_______ (列出算式即可)。
(2)下列方法中可以使0.10mol/L醋酸溶液中CH3COOH电离程度增大的是_______(填字母序号)。
(3)25°C时,pH与体积均相同的醋酸溶液A与盐酸B分别与足量镁条充分反应,下列说法不正确的是_______ (填字母序号)。
a.开始反应时的速率:A<B
b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A>B
| 化学式 | CH3COOH | H2CO3 | HClO | NH3·H2O |
| 电离平衡常数 | Ka=1.75×105 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=3.0×10-8 | Kb=1.8×10-5 |
(2)下列方法中可以使0.10mol/L醋酸溶液中CH3COOH电离程度增大的是_______(填字母序号)。
| A.加水稀释 | B.微热溶液 |
| C.滴加少量浓氢氧化钠 | D.加入少量醋酸钠晶体 |
a.开始反应时的速率:A<B
b.放出等量氢气所需要的时间A=B
c.生成氢气的总体积:A>B
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空
(1)写出下列物质在水中电离方程式:
NaHSO4_____________________________ NH3·H2O______________________________________________________
(2)写出下列物质水解的离子方程式:
NaHCO3___________________________ FeCl3_____________________________
(3)常温时,0.1mol/L的NaOH和0.06mol/L 的H2SO4溶液等体积混合,求混合溶液的pH为_______ 。
(1)写出下列物质在水中电离方程式:
NaHSO4
(2)写出下列物质水解的离子方程式:
NaHCO3
(3)常温时,0.1mol/L的NaOH和0.06mol/L 的H2SO4溶液等体积混合,求混合溶液的pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】描述弱电解质电离情况可以用电离度和电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
表1
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________ (填字母序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________ (选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是_____________________________ 。
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为________________________ 。
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3·H2O | 1.8×10-5 |
表1
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有四种电解质溶液:
①NaHCO3 ②NaAlO2 ③CH3COONa ④NaOH
(1)若上述四种溶液pH相同,其物质的量浓度由大到小的顺序是___________________________________ (填编号,下同)。
(2)将四种溶液稀释相同倍数时,其pH变化最大的是________ 。
(3)在上述四种溶液中,分别加入FeCl3溶液,能产生的共同现象是_____________________________________ ,能产生气体的是________ 。
①NaHCO3 ②NaAlO2 ③CH3COONa ④NaOH
(1)若上述四种溶液pH相同,其物质的量浓度由大到小的顺序是
(2)将四种溶液稀释相同倍数时,其pH变化最大的是
(3)在上述四种溶液中,分别加入FeCl3溶液,能产生的共同现象是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】强弱电解质在水中的行为是不同的。
(1)醋酸在水中的电离方程式为___________ 。
(2)室温下,用0.1mol/LNaOH溶液分别滴定20.00mL0.1mol/L的醋酸和盐酸溶液,滴定曲线如图所示。
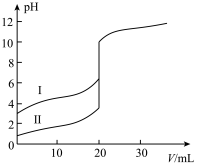
①II表示滴定___________ 的曲线(填“盐酸”或“醋酸”)。
②当滴定到pH=7时,消耗NaOH溶液的体积大的是___________ (填“盐酸”或“醋酸”)。
③当V(NaOH)=10.00mL时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是___________ 。
④在上述滴定过程中,需要使用的玻璃仪器是___________ (填序号)。
A.碱式滴定管 B.锥形瓶 C.容量瓶 D.玻璃棒
(1)醋酸在水中的电离方程式为
(2)室温下,用0.1mol/LNaOH溶液分别滴定20.00mL0.1mol/L的醋酸和盐酸溶液,滴定曲线如图所示。

①II表示滴定
②当滴定到pH=7时,消耗NaOH溶液的体积大的是
③当V(NaOH)=10.00mL时,醋酸溶液中各离子的物质的量浓度由大到小的顺序是
④在上述滴定过程中,需要使用的玻璃仪器是
A.碱式滴定管 B.锥形瓶 C.容量瓶 D.玻璃棒
您最近一年使用:0次



