描述弱电解质电离情况可以用电离度和电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb)
表1
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是________ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是________ (填字母序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈________ (选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系是_____________________________ 。
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为________________________ 。
酸或碱 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.6×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
NH3·H2O | 1.8×10-5 |
表1
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈
(3)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH >7,该溶液中离子浓度从大到小的排列为
更新时间:2019-12-14 19:09:36
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】已知H2CO3、H2S的电离常数如表,判断下列反应能否发生,若能,写出离子方程式。
(1)往Na2S溶液中加入少量NaHCO3溶液:_______ 。
(2)往Na2CO3溶液中加入少量NaHS溶液:_______ 。
(3)往Na2S溶液中通入少量CO2:_______ 。
(4)往Na2S溶液中通入过量CO2:_______ 。
(5)往Na2CO3溶液中通入少量H2S:_______ 。
(6)往Na2CO3溶液中通入过量H2S:_______ 。
| H2CO3 | H2S |
| K1=4.3×10-7,K2=5.6×10-11 | K1=9.1×10-8,K2=1.1×10-12 |
(2)往Na2CO3溶液中加入少量NaHS溶液:
(3)往Na2S溶液中通入少量CO2:
(4)往Na2S溶液中通入过量CO2:
(5)往Na2CO3溶液中通入少量H2S:
(6)往Na2CO3溶液中通入过量H2S:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列物质的电离方程式。
(1)Ba(OH)2:___________ ;
(2)NH4Cl:___________ ;
(3)NaHCO3:___________ ,___________ ;
(1)Ba(OH)2:
(2)NH4Cl:
(3)NaHCO3:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】电离平衡常数(用 表示)的大小可以判断电解质的相对强弱。
表示)的大小可以判断电解质的相对强弱。
(1)水是极弱的电解质, 可表示水的电离程度,其表达式是
可表示水的电离程度,其表达式是_______ ,温度升高, 的值
的值_______ (填“变大”“变小”或“不变”)。
(2) 通常表示弱酸的电离平衡常数,
通常表示弱酸的电离平衡常数, 值越大表示该弱酸的酸性
值越大表示该弱酸的酸性_______ ,当用蒸馏水稀释 醋酸时,醋酸的
醋酸时,醋酸的
_______ (填“变大”“变小”或“不变”)。
(3)常温下, 的盐酸中由水电离出的
的盐酸中由水电离出的 浓度为
浓度为_______ , 的NaOH溶液中由水电离出的
的NaOH溶液中由水电离出的 浓度为
浓度为_______ 。
(4)常温下,4种酸的电离平衡常数如下:
①物质的量浓度相同的HF、 、
、 、HClO中,
、HClO中, 由大到小的顺序是
由大到小的顺序是_______ 。
② 、
、 、
、 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是_______ 。
 表示)的大小可以判断电解质的相对强弱。
表示)的大小可以判断电解质的相对强弱。(1)水是极弱的电解质,
 可表示水的电离程度,其表达式是
可表示水的电离程度,其表达式是 的值
的值(2)
 通常表示弱酸的电离平衡常数,
通常表示弱酸的电离平衡常数, 值越大表示该弱酸的酸性
值越大表示该弱酸的酸性 醋酸时,醋酸的
醋酸时,醋酸的
(3)常温下,
 的盐酸中由水电离出的
的盐酸中由水电离出的 浓度为
浓度为 的NaOH溶液中由水电离出的
的NaOH溶液中由水电离出的 浓度为
浓度为(4)常温下,4种酸的电离平衡常数如下:
| 化学式 | HF |  |  | HClO |
| 电离平衡常数 | 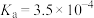 |  |   | 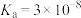 |
 、
、 、HClO中,
、HClO中, 由大到小的顺序是
由大到小的顺序是②
 、
、 、
、 、
、 、
、 结合
结合 的能力由大到小的顺序是
的能力由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】一水合氨(NH3·H2O)是一种常见的弱碱,回答下列问题:
在0.1mol·L﹣1氨水中加入下列物质,一水合氨的电离平衡及平衡时物质的浓度的变化:
(1)写出NH3·H2O的电离方程式____ 。
(2)向氨水中加入NH4Cl固体,电离平衡向___ 移动(填“正向”、“逆向”或“不移动”,下同);pH ___ (填“增大”、“减小”或“不变”,下同)
(3)向氨水中加入FeCl3固体,电离平衡向_____ 移动;c(NH3·H2O)______
(4)已知常温下,NH3·H2O的电离常数为Kb=1.8×10-5,若氨水的浓度为2.0mol∙L-1,则溶液中OH-的浓度是___ mol∙L-1。
在0.1mol·L﹣1氨水中加入下列物质,一水合氨的电离平衡及平衡时物质的浓度的变化:
(1)写出NH3·H2O的电离方程式
(2)向氨水中加入NH4Cl固体,电离平衡向
(3)向氨水中加入FeCl3固体,电离平衡向
(4)已知常温下,NH3·H2O的电离常数为Kb=1.8×10-5,若氨水的浓度为2.0mol∙L-1,则溶液中OH-的浓度是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知常温下H2C2O4的电离平衡常数Ka1=5.4×10-2,Ka2=5.4×10-5,反应NH3·H2O+ =
= +
+ +H2O的平衡常数K=9.45×104,则NH3·H2O的电离平衡常数Kb=
+H2O的平衡常数K=9.45×104,则NH3·H2O的电离平衡常数Kb=_______ 。
 =
= +
+ +H2O的平衡常数K=9.45×104,则NH3·H2O的电离平衡常数Kb=
+H2O的平衡常数K=9.45×104,则NH3·H2O的电离平衡常数Kb=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】回答下列问题:
(1)氮肥硝酸铵不能与钾肥碳酸钾混合施用的原因是_______ 。
(2)已知苯酚(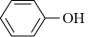 )具有弱酸性,其
)具有弱酸性,其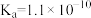 ,水杨酸第一级电离形成的离子
,水杨酸第一级电离形成的离子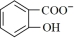 能形成分子内氢键。据此判断,相同温度下电离平衡常数
能形成分子内氢键。据此判断,相同温度下电离平衡常数 (水杨酸)
(水杨酸)_______  (苯酚)(填“>”或“<”),其原因是
(苯酚)(填“>”或“<”),其原因是_______ 。
(1)氮肥硝酸铵不能与钾肥碳酸钾混合施用的原因是
(2)已知苯酚(
 )具有弱酸性,其
)具有弱酸性,其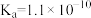 ,水杨酸第一级电离形成的离子
,水杨酸第一级电离形成的离子 能形成分子内氢键。据此判断,相同温度下电离平衡常数
能形成分子内氢键。据此判断,相同温度下电离平衡常数 (水杨酸)
(水杨酸) (苯酚)(填“>”或“<”),其原因是
(苯酚)(填“>”或“<”),其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】常温下,有下列五种溶液:① 、②
、② 、③HCl、④
、③HCl、④ 、⑤NaOH
、⑤NaOH
(1)pH相等的④和⑤溶液,稀释相同的倍数,稀释之后pH较大的是_______ (填字号)
(2)等浓度的上述溶液中,水电离的程度由大到小的顺序_______ (填序号,用>、<、=连接)
(3)向④中加入少量氯化铵固体,此时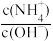 的值
的值_______ (填“增大”“减小”或“不变”)
(4)若将等浓度的③和④的溶液混合后溶液恰好呈中性,则混合前③的体积_______ ④的体积(填“大于”、“小于”或“等于”),此时溶液中离子度由大到小的顺序是_______ 。
(5)取0.1 mol∙L−1,10mL的溶液③,加水稀释到1000mL,则此时溶液中由水电离出的
_______ 。
(6)某学生用已知物质的量浓度的③来滴定未知物质的量浓度的⑤溶液用以测定⑤的浓度,选择甲基橙作指示剂,下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______(填字母序号)。
 、②
、② 、③HCl、④
、③HCl、④ 、⑤NaOH
、⑤NaOH(1)pH相等的④和⑤溶液,稀释相同的倍数,稀释之后pH较大的是
(2)等浓度的上述溶液中,水电离的程度由大到小的顺序
(3)向④中加入少量氯化铵固体,此时
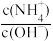 的值
的值(4)若将等浓度的③和④的溶液混合后溶液恰好呈中性,则混合前③的体积
(5)取0.1 mol∙L−1,10mL的溶液③,加水稀释到1000mL,则此时溶液中由水电离出的

(6)某学生用已知物质的量浓度的③来滴定未知物质的量浓度的⑤溶液用以测定⑤的浓度,选择甲基橙作指示剂,下列操作中可能使所测NaOH溶液的浓度数值偏低的是_______(填字母序号)。
| A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸 |
| B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 |
| C.酸式滴定管在滴定前有气泡,滴定后气泡消失 |
| D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】(1)氯化铝水溶液呈__ 性,(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):___ ;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是__ 。
(2)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是___ 。
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
回答下列问题
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为___ 。
②向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:___ 。
(2)室温下,若向0.1mol/L氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子的物质的量浓度由大到小的顺序是
(3)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三溶液的pH由大到小的顺序为
②向NaCN溶液中通入少量CO2,所发生反应的化学方程式为:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】现有①0.2 mol·L-1 NaOH溶液 ②0.2 mol·L-1 HX溶液,两溶液等体积混合后,测得溶液中c(Na+)>c(X-)。则
(1)①中由水电离出的c(OH-)________ ②中由水电离出的c(H+) (填“>”、“=”或“<”)。
(2)上述混合液中共存在______ 种粒子,且c(HX)________ c(X-)(填“>”“=”或“<”,下同),c(HX)+c(X-)________ 0.1 mol·L-1(忽略体积变化)。
(3)上述混合液显________ 性(填“酸”、“碱”或“中”),其原因用离子方程式表示为______________________________________ 。
(1)①中由水电离出的c(OH-)
(2)上述混合液中共存在
(3)上述混合液显
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】室温下,有浓度均为 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。
① ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离常数,醋酸 ;碳酸
;碳酸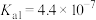 ,
, 。
。
(1)上述溶液加入水中,对水的电离无影响的是______ (填序号),溶液④中溶质与水作用的离子方程式为______ 。
(2)上述溶液的 由小到大的顺序为
由小到大的顺序为______ (填序号)。
(3)比较溶液③和④中 的物质的量浓度:③
的物质的量浓度:③______ ④(填“大于”、“等于”或“小于”)。
(4)室温下,向溶液①中加水稀释至原体积的100倍,所得溶液的 为
为______ 。
(5)向20mL0.1mol/L 中滴加0.1mol/L
中滴加0.1mol/L 过程中,
过程中, 变化如图所示。
变化如图所示。
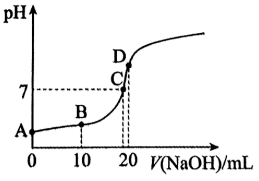
①滴加过程中发生反应的离子方程式是______ 。
②下列说法正确的是______ 。
a. 、
、 两点水的电离程度:
两点水的电离程度:
b. 点溶液中微粒浓度满足:
点溶液中微粒浓度满足: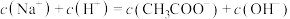
c. 点溶液微粒浓度满足:
点溶液微粒浓度满足: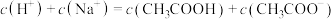
 的下列五种溶液,请回答问题。
的下列五种溶液,请回答问题。①
 ②
② ③
③ ④
④ ⑤
⑤
资料:室温下电离常数,醋酸
 ;碳酸
;碳酸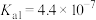 ,
, 。
。(1)上述溶液加入水中,对水的电离无影响的是
(2)上述溶液的
 由小到大的顺序为
由小到大的顺序为(3)比较溶液③和④中
 的物质的量浓度:③
的物质的量浓度:③(4)室温下,向溶液①中加水稀释至原体积的100倍,所得溶液的
 为
为(5)向20mL0.1mol/L
 中滴加0.1mol/L
中滴加0.1mol/L 过程中,
过程中, 变化如图所示。
变化如图所示。
①滴加过程中发生反应的离子方程式是
②下列说法正确的是
a.
 、
、 两点水的电离程度:
两点水的电离程度:
b.
 点溶液中微粒浓度满足:
点溶液中微粒浓度满足: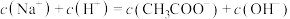
c.
 点溶液微粒浓度满足:
点溶液微粒浓度满足: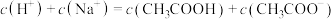
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】按要求回答下列问题:
(1)HClO的电离方程式为__________________________ 。
(2)用离子方程式解释铁盐可用于净水的原理__________________________ 。
(3)在NaOH 溶液中逐渐加入稀醋酸至溶液呈中性,则所得溶液中c(Na+)_______ c(CH3COO-)(填“>”“<”或“=”下同)。
(4)相同pH的NH4Cl溶液与NH4HSO4溶液中NH4+浓度的大小关系:前者_______ 后者。
(5)用惰性电极电解500mL某浓度的CuSO4溶液一段时间后,CuSO4刚好反应完,需要加入16gCuO才能复原,则原CuSO4溶液的物质量浓度为___________ 。
(1)HClO的电离方程式为
(2)用离子方程式解释铁盐可用于净水的原理
(3)在NaOH 溶液中逐渐加入稀醋酸至溶液呈中性,则所得溶液中c(Na+)
(4)相同pH的NH4Cl溶液与NH4HSO4溶液中NH4+浓度的大小关系:前者
(5)用惰性电极电解500mL某浓度的CuSO4溶液一段时间后,CuSO4刚好反应完,需要加入16gCuO才能复原,则原CuSO4溶液的物质量浓度为
您最近一年使用:0次



