完成下面的题。
(1)CH3COOH溶于水的电离方程式为_______ ;向CH3COOH溶液中加入醋酸钠固体时,电离平衡向_______ 移动(填“左”或者“右”),c(CH3COO-)_______ 。(填“增大”、“减小”“不变”,下同)
(2)0.05mol/LH2SO4溶液的pH为_______ 。
(3)某温度下,水的离子积常数Kw=1×10-12,则此温度大于25℃,原因是_______ 。
(1)CH3COOH溶于水的电离方程式为
(2)0.05mol/LH2SO4溶液的pH为
(3)某温度下,水的离子积常数Kw=1×10-12,则此温度大于25℃,原因是
更新时间:2021-01-23 10:15:28
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】弱电解质电离情况可以用电离度和电离平衡常数表示,下表是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),请回答下面问题:
(1)CH3COONH4的水溶液呈___ (选填“酸性”、“中性”或“碱性”)。理由是___ 。溶液中各离子浓度大小关系是___ 。
温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,请回答下列问题:
(2)该温度下水的离子积常数Kw=___ 。
(3)该NaOH溶液中由水电离出的c(OH-)是___ mol/L。
(4)给该NaOH溶液加热(水不挥发),pH=____ 。(填变大、变小或不变)
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3•H2O | 1.8×10-5 |
(1)CH3COONH4的水溶液呈
温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,请回答下列问题:
(2)该温度下水的离子积常数Kw=
(3)该NaOH溶液中由水电离出的c(OH-)是
(4)给该NaOH溶液加热(水不挥发),pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】若HA为一元弱酸,MOH为一元弱碱,已知:MA水解常数为Kh,HA的电离常数为Ka,MOH的电离常数Kb,水的离子积为KW试推导Kh、Ka、Kb、KW之间的关系___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】某温度下的水溶液中,c(H+)=10-xmol/L,c(OH-)=10-y mol/L。x与y的关系如图所示:
(1)该温度下水的离子积为__________ ;该温度_____________ 常温(填“高于”、“低于”或“等于”)。
(2)该温度下0.01 mol/L NaOH溶液的pH为_____ 。
(3)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg 。则该温度下,0.01mol/L盐酸的酸度AG=
。则该温度下,0.01mol/L盐酸的酸度AG=_________ 。

(1)该温度下水的离子积为
(2)该温度下0.01 mol/L NaOH溶液的pH为
(3)除了用pH外,科学家还建议用酸度(AG)来表示溶液的酸碱性:AG=lg
 。则该温度下,0.01mol/L盐酸的酸度AG=
。则该温度下,0.01mol/L盐酸的酸度AG=
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】某酸HA是一元弱酸,25℃时的电离平衡常数Ka=4.0×10-8。
(1)写出该酸的电离方程式____ ,其电离平衡常数表达式Ka=____ 。
(2)25℃时,向1mol•L-1HA溶液中加入1mol•L-1盐酸,会____ (“抑制”或“促进”)HA的电离,c(H+)____ (填“增大”、“减小”或“不变”),电离平衡常数Ka____ (填“增大”、“减小”或“不变”)。
(3)常温条件下,某浓度的盐酸溶液的pH=3,则其中c(H+)=____ mol/L,c(OH-)=____ mol/L。
(4)常温下等体积混合0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液后,溶液pH=____ 。
(1)写出该酸的电离方程式
(2)25℃时,向1mol•L-1HA溶液中加入1mol•L-1盐酸,会
(3)常温条件下,某浓度的盐酸溶液的pH=3,则其中c(H+)=
(4)常温下等体积混合0.1mol/L的盐酸和0.06mol/L的Ba(OH)2溶液后,溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】回答下列问题:
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
(1)25℃时, 盐酸的pH约为
盐酸的pH约为______ ,该溶液中水电离出的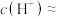
______  。
。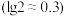
(2)少量的 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为______ 。
(3) 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为______ ;25℃时, 的水解平衡常数
的水解平衡常数
______ 其电离平衡常数 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显______ 性。
Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为______ (填“原电池”“电解池”或“电镀池”),通入 电极的电极反应式正确的为
电极的电极反应式正确的为______ 。
A. B.
B.
C.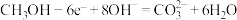 D.
D.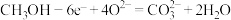
(5)当甲池中消耗 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加______ g。
(6)丙池中发生的总反应化学方程式为______ ;为了防止丙池中两极产物相互反应,实际生产中在两极之间设有______ 离子交换膜(填“阴”或“阳”或“质子”)。
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
弱电解质 |
|
| HClO |
电离常数 |
|
|
|
(1)25℃时,
 盐酸的pH约为
盐酸的pH约为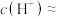
 。
。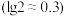
(2)少量的
 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为(3)
 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为 的水解平衡常数
的水解平衡常数
 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为
 电极的电极反应式正确的为
电极的电极反应式正确的为A.
 B.
B.
C.
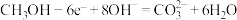 D.
D.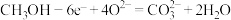
(5)当甲池中消耗
 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加(6)丙池中发生的总反应化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列物质的电离方程式:
(1)NaHCO3__________________ ;
(2)NaHSO4___________________________ ;
(3)H2S_____________________________ ;
(4)NH3·H2O___________________________ ;
(1)NaHCO3
(2)NaHSO4
(3)H2S
(4)NH3·H2O
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求回答下列问题
(1)写出氮化镁的化学式________ 。
(2)写出 的离子结构示意图
的离子结构示意图________ 。
(3)写出醋酸在水溶液中的电离方程式________ 。
(4)写出溴水使湿润的淀粉碘化钾试纸变蓝的化学方程式________ 。
(1)写出氮化镁的化学式
(2)写出
 的离子结构示意图
的离子结构示意图(3)写出醋酸在水溶液中的电离方程式
(4)写出溴水使湿润的淀粉碘化钾试纸变蓝的化学方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空
(1)写出下列物质在水中电离方程式:
NaHSO4_____________________________ NH3·H2O______________________________________________________
(2)写出下列物质水解的离子方程式:
NaHCO3___________________________ FeCl3_____________________________
(3)常温时,0.1mol/L的NaOH和0.06mol/L 的H2SO4溶液等体积混合,求混合溶液的pH为_______ 。
(1)写出下列物质在水中电离方程式:
NaHSO4
(2)写出下列物质水解的离子方程式:
NaHCO3
(3)常温时,0.1mol/L的NaOH和0.06mol/L 的H2SO4溶液等体积混合,求混合溶液的pH为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】Ⅰ. 醋酸是一种常见的弱酸,在0.1 mol·L-1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:(填“正向”、“逆向”或“不移动”,“增大”、“减小”或“不变”,填“>”、“<”或“=”)
(1)向醋酸中加入醋酸钠固体,电离平衡向_____________ 移动,pH_____________ 。
(2)向醋酸中加入碳酸钙固体,电离平衡向_____________ 移动;
(3)向醋酸中加入大量的水,c(OH-)_____________ ,导电能力_____________ 。
(1)向醋酸中加入醋酸钠固体,电离平衡向
(2)向醋酸中加入碳酸钙固体,电离平衡向
(3)向醋酸中加入大量的水,c(OH-)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在6份0.01mol/L氨水中分别加入下列各物质:
A.浓氨水B.纯水C.少量浓H2SO4 D.少量NaOH固体E.少量Al2(SO4)3 固体
(1)能使c(OH-)减小、c(NH4+)增大的是_______
(2)能使c(OH-)增大、c(NH4+)减小的是_______
(3)能使c(OH-)和c(NH4+)都增大的是_________
(4)能使c(OH-)和c(NH4+)都减小的是_________
A.浓氨水B.纯水C.少量浓H2SO4 D.少量NaOH固体E.少量Al2(SO4)3 固体
(1)能使c(OH-)减小、c(NH4+)增大的是
(2)能使c(OH-)增大、c(NH4+)减小的是
(3)能使c(OH-)和c(NH4+)都增大的是
(4)能使c(OH-)和c(NH4+)都减小的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】25℃时,三种酸的电离平衡常数如表所示。
回答下列问题:
(1)浓度均为0.1mol/L的CH3COOH,HClO,H3PO3溶液中,c(H+)最小的是___ 。
(2)亚磷酸(H3PO3)为二元酸,具有较强的还原性Na2HPO3是___ (填“酸式盐”“碱式盐”或“正盐”)。H3PO3的第二级电离方程式为___ 。此时的电离平衡常数表达式K=___ 。
(3)常温下,0.1mol/L的CH3COOH溶液加水稀释的过程中,下列表达式的数值变大的是___ (填字母)。
A.c(H+) B. C.c(CH3COO-) D.c(CH3COOH)
C.c(CH3COO-) D.c(CH3COOH)
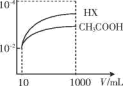
(4)体积均为10mL、c(H+)均为10-2mol/L的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中c(H+)的变化如图所示测HX的电离平衡常数___ (填“大于”、“小于”或“等于”)醋酸的电离平衡常数,理由是___ 。
| 化学式 | CH3COOH | HClO | H3PO3 |
| 名称 | 醋酸 | 次氯酸 | 亚磷酸 |
| 电离平衡常数 | 1.8×10-5 | 3.0×10-8 | Ki=8.3×10-3 K2=5.6×10-6 |
回答下列问题:
(1)浓度均为0.1mol/L的CH3COOH,HClO,H3PO3溶液中,c(H+)最小的是
(2)亚磷酸(H3PO3)为二元酸,具有较强的还原性Na2HPO3是
(3)常温下,0.1mol/L的CH3COOH溶液加水稀释的过程中,下列表达式的数值变大的是
A.c(H+) B.
 C.c(CH3COO-) D.c(CH3COOH)
C.c(CH3COO-) D.c(CH3COOH)(4)体积均为10mL、c(H+)均为10-2mol/L的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中c(H+)的变化如图所示测HX的电离平衡常数

您最近一年使用:0次

 的硫酸溶液中由水电离出的
的硫酸溶液中由水电离出的
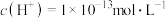 的
的 溶液中,
溶液中,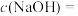
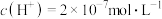 ,则此时纯水的
,则此时纯水的 为
为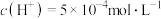 ,则溶液中
,则溶液中