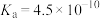回答下列问题:
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
(1)25℃时, 盐酸的pH约为
盐酸的pH约为______ ,该溶液中水电离出的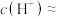
______  。
。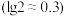
(2)少量的 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为______ 。
(3) 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为______ ;25℃时, 的水解平衡常数
的水解平衡常数
______ 其电离平衡常数 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显______ 性。
Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为______ (填“原电池”“电解池”或“电镀池”),通入 电极的电极反应式正确的为
电极的电极反应式正确的为______ 。
A. B.
B.
C.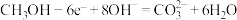 D.
D.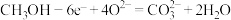
(5)当甲池中消耗 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加______ g。
(6)丙池中发生的总反应化学方程式为______ ;为了防止丙池中两极产物相互反应,实际生产中在两极之间设有______ 离子交换膜(填“阴”或“阳”或“质子”)。
Ⅰ.25℃时,某些弱电解质的电离常数如表所示,回答下列问题。
弱电解质 |
|
| HClO |
电离常数 |
|
|
|
(1)25℃时,
 盐酸的pH约为
盐酸的pH约为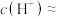
 。
。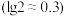
(2)少量的
 通入
通入 溶液中,发生反应的离子方程式为
溶液中,发生反应的离子方程式为(3)
 发生水解反应的水解平衡常数
发生水解反应的水解平衡常数 表达式为
表达式为 的水解平衡常数
的水解平衡常数
 (填“>”或“<”),故
(填“>”或“<”),故 溶液显
溶液显Ⅱ.请分析如下电化学装置,回答下列问题:

(4)甲池为
 电极的电极反应式正确的为
电极的电极反应式正确的为A.
 B.
B.
C.
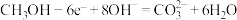 D.
D.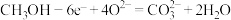
(5)当甲池中消耗
 为1.12L(标准状况下)时,理论上乙池中B极质量增加
为1.12L(标准状况下)时,理论上乙池中B极质量增加(6)丙池中发生的总反应化学方程式为
更新时间:2023-12-13 15:09:38
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】根据所学知识,回答下列问题:
(1)K2FeO4是常见的水处理剂,净水原理如图所示。请回答下列问题:___________ 。
②过程a中K2FeO4体现___________ (填“氧化”或“还原”)性,反应过程中转移5.418×1022个电子,需要___________ mol K2FeO4。
(2)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:___________ 。
___________Fe(OH)3+___________KOH+___________KClO=___________K2FeO4+___________KCl+___________H2O
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是___________ ,生产1mol的高铁酸钠,需要转移电子的物质的量是___________ mol。
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:___________ ;反应片刻后,可观察到有气体产生。
(1)K2FeO4是常见的水处理剂,净水原理如图所示。请回答下列问题:
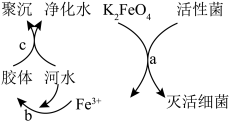
②过程a中K2FeO4体现
(2)碱性条件下用Fe(OH)3和KClO反应制备K2FeO4。配平其反应的化学方程式:
___________Fe(OH)3+___________KOH+___________KClO=___________K2FeO4+___________KCl+___________H2O
(3)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中的还原剂是
(4)将铝箔放入NaOH稀溶液中,开始时无气体生成,写出反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求写出下列反应的方程式:
(1)氯气和水反应的离子方程式:_______ ;
(2)过量铁粉在氯气中燃烧的化学方程式:_______ ;
(3)工业制漂白粉的化学方程式:_______ ;
(4)漂白粉工作原理的化学方程式:_______ ;
(5)Ca(OH)2溶液与足量的NaHCO3溶液反应的离子方程式:_______ ;
(6)碳酸氢钠的电离方程式:_______ ;
(7)氢氧化铜的电离方程式:_______ ;
(8)Na与水反应的离子方程式:_______ ;
(9)Na2O2与二氧化碳反应的化学方程式:_______ ;
(10)Na2CO3溶液与少量盐酸反应的离子方程式:_______ 。
(1)氯气和水反应的离子方程式:
(2)过量铁粉在氯气中燃烧的化学方程式:
(3)工业制漂白粉的化学方程式:
(4)漂白粉工作原理的化学方程式:
(5)Ca(OH)2溶液与足量的NaHCO3溶液反应的离子方程式:
(6)碳酸氢钠的电离方程式:
(7)氢氧化铜的电离方程式:
(8)Na与水反应的离子方程式:
(9)Na2O2与二氧化碳反应的化学方程式:
(10)Na2CO3溶液与少量盐酸反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】有如下反应:
请回答:
(1)上述反应中有电子转移的是___ (填序号),因此该类反应属于__ 反应。
(2)反应⑤的离子方程式是__ 。
(3)上述反应中属于复分解反应的是__ (填序号)。复分解反应发生的条件是i.生成沉淀,ii.放出气体,iii.生成水等难电离物质,若要由反应印证i、ii、iii,则除了这几个反应外,请补充反应:_ (写一个符合条件的化学方程式或离子方程式)。
(4)由反应①及所学知识判断:在该反应发生的条件下,NO3-、H+、Cu2+的氧化性由大到小的顺序是___ 。
| ①3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O | ②H++OH-=H2O |
③2Fe+3Cl2 2FeCl3 2FeCl3 | ④NaHCO3+NaOH=Na2CO3+H2O |
| ⑤CuSO4+2NaOH=Cu(OH)2↓+Na2SO4 | ⑥NaClO+CO2+H2O=HClO+NaHCO3 |
| ⑦2Al+2NaOH+2H2O=2NaAlO2+3H2↑ | ⑧CO2+H2O=H2CO3 |
(1)上述反应中有电子转移的是
(2)反应⑤的离子方程式是
(3)上述反应中属于复分解反应的是
(4)由反应①及所学知识判断:在该反应发生的条件下,NO3-、H+、Cu2+的氧化性由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】常温下,有 0.1 mol/L 的四种溶液:①HCl ②CH3COOH ③NaOH ④Na2CO3
(1)用化学用语解释溶液①呈酸性的原因:_________ 。
(2)溶液③的 pH=_________ 。
(3)溶液①、②分别与等量的溶液③恰好完全反应,消耗的体积:①_________ ②(填“>”、“<”或“=”)。
(4)溶液④加热后碱性增强,结合化学用语解释原因:_________ 。
(5)常温下,下列关于溶液②的判断正确的是_________ 。
a.c(CH3COO−) = 0.1 mol/L
b.溶液中c(H+) > c(CH3COO−) > c(OH −)
c.加入CH3COONa(s),c(H+)不变
d.滴入 NaOH 浓溶液,溶液导电性增强
(1)用化学用语解释溶液①呈酸性的原因:
(2)溶液③的 pH=
(3)溶液①、②分别与等量的溶液③恰好完全反应,消耗的体积:①
(4)溶液④加热后碱性增强,结合化学用语解释原因:
(5)常温下,下列关于溶液②的判断正确的是
a.c(CH3COO−) = 0.1 mol/L
b.溶液中c(H+) > c(CH3COO−) > c(OH −)
c.加入CH3COONa(s),c(H+)不变
d.滴入 NaOH 浓溶液,溶液导电性增强
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在不同温度下的水溶液中,c(H+)和c(OH-)的关系如图所示:

(1)A点水的离子积为_____________ ,C点水的离子积为_____________ ,对纯水由25℃升高温度至100℃时水的离子积__________ (填“增大”、“减小”或“不变”),各离子浓度由______ 点(填A、B、C、D)变为______ 点(填A、B、C、D)。
(2)100 ℃时,若向B点溶液中滴加硫酸,体系将由B点移向_____ 点(填C或D),为什么_____________________________________ 。
(3)25 ℃时,0.001mol/L的盐酸溶液pH=_______ ;0.001mol/L的氢氧化钠溶液pH=_________ ;若将二者温度都升高至100 ℃,________________ (填“盐酸”、“氢氧化钠”或“盐酸和氢氧化钠”)的pH会改变。

(1)A点水的离子积为
(2)100 ℃时,若向B点溶液中滴加硫酸,体系将由B点移向
(3)25 ℃时,0.001mol/L的盐酸溶液pH=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】室温下有5种稀溶液:①HCl、②H2SO4、③CH3COOH、④氨水、⑤NaOH,回答下列问题:
(1)若溶液①②③④⑤浓度均为0.01mol/L,pH由大到小的顺序是___________ 。(用序号填写,下同)
(2)中和等体积、pH相同的①②③溶液消耗NaOH最多的是___________ 。
(3)pH相同的④⑤溶液,则溶液的离子总浓度④___________ ⑤(填“>,<或=”)。
(4)常温下,pH=3的②溶液中水电离出的 ___________mol/L。
___________mol/L。
(1)若溶液①②③④⑤浓度均为0.01mol/L,pH由大到小的顺序是
(2)中和等体积、pH相同的①②③溶液消耗NaOH最多的是
(3)pH相同的④⑤溶液,则溶液的离子总浓度④
(4)常温下,pH=3的②溶液中水电离出的
 ___________mol/L。
___________mol/L。A.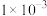 | B.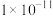 | C. | D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】I.根据表中数据(常温下),完成下列填空。
(1)常温下,NaCN溶液呈____ (填“酸”、“碱”或“中”)性,其原因是____ (用离子方程式表示)。
(2)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CH3COONa溶液,②NaCN溶液,③NaHCO3溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是____ (填序号)。
(3)常温下,向NaClO溶液中通入少量CO2,发生反应的离子方程式为____ 。
(4)常温下,Na2SO3溶液中c(OH-)−c(H+)=c(HSO )+
)+____ 。
II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10−12,Ksp(CdS)=8.0×10−27;回答下列问题:
(5)向某含镉废水中加入Na2S,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为____ mol∙L−1,此时是否符合生活饮用水卫生标准?____ (填“是”或“否”)。
(6)室温下,反应CdCO3(s)+S2−(aq) CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=____ (结果保留两位有效数字)
| 物质 | CH3COOH | NH3∙H2O | HCN | HClO | H2CO3 | H2SO3 |
| 电离常数(Ka) | 1.7×10−5 | 1.7×10−5 | 4.9×10−10 | 3×10−8 | Ka1=4.3×10−7 Ka2=5.6×10−11 | Ka1=1.5×10−2 Ka2=1.0×10−7 |
(2)常温下,浓度均为0.1 mol∙L−1的下列4种溶液:①CH3COONa溶液,②NaCN溶液,③NaHCO3溶液,④NaClO溶液;这4种溶液pH由大到小的顺序是
(3)常温下,向NaClO溶液中通入少量CO2,发生反应的离子方程式为
(4)常温下,Na2SO3溶液中c(OH-)−c(H+)=c(HSO
 )+
)+II.我国《生活饮用水卫生标准》中规定生活用水中镉的排放量不超过0.005mg∙L−1。处理含镉废水可采用化学沉淀法。Ksp(CdCO3)=4.0×10−12,Ksp(CdS)=8.0×10−27;回答下列问题:
(5)向某含镉废水中加入Na2S,当S2−浓度达到8.0×10−8 mol∙L−1时,废水中Cd2+的浓度为
(6)室温下,反应CdCO3(s)+S2−(aq)
 CdS(s)+CO
CdS(s)+CO (aq)达到平衡,该反应的平衡常数K=
(aq)达到平衡,该反应的平衡常数K=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请用离子方程式表示下列事实或者现象发生的原因:
①MgO可溶于NH4Cl溶液中的原理:__________ 。
②KCN溶液显碱性的原因是________ 。
③对于易溶于水的正盐MnRm溶液,若pH>7,其原因是______ ;若pH<7,其原因是_______ 。
①MgO可溶于NH4Cl溶液中的原理:
②KCN溶液显碱性的原因是
③对于易溶于水的正盐MnRm溶液,若pH>7,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题:
(1)水的离子积常数Kw与温度t(℃)的关系如图所示:
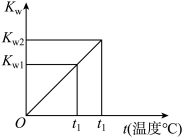
若t1=25℃,则Kw1=_______ ;若t2=100℃时,Kw2=10-12,则此时0.05mol·L-1的Ba(OH)2溶液的pH=_______ 。
(2)常温下用NaOH、氨水、CH3COOH、HCl、NH4HSO4五种溶液进行下列实验:
①浓度均为0.1mol/L的HCl和CH3COOH的pH:HCl_______ CH3COOH(填“<”“>”或“=”)。
②将xL0.01mol/L氨水与yL0.01mol/LHCl溶液充分反应至溶液呈中性,x、y大小关系为:x_______ y(填“<”“>”或“=”)。
③浓度均为0.1mol/L的NH4HSO4与NaOH等体积混合,反应的离子方程式为_______ ;此时溶液呈_______ 性(填“酸性”碱性”或“中性”)。
④用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是_______ (填写序号)。
① ②
② ③c
③c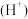 和c
和c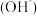 的乘积 ④
的乘积 ④ 的物质的量
的物质的量
(1)水的离子积常数Kw与温度t(℃)的关系如图所示:

若t1=25℃,则Kw1=
(2)常温下用NaOH、氨水、CH3COOH、HCl、NH4HSO4五种溶液进行下列实验:
①浓度均为0.1mol/L的HCl和CH3COOH的pH:HCl
②将xL0.01mol/L氨水与yL0.01mol/LHCl溶液充分反应至溶液呈中性,x、y大小关系为:x
③浓度均为0.1mol/L的NH4HSO4与NaOH等体积混合,反应的离子方程式为
④用水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是
①
 ②
② ③c
③c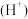 和c
和c 的乘积 ④
的乘积 ④ 的物质的量
的物质的量
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据下图,回答下列问题:
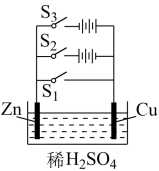
(1)若闭合S1,装置属于___________ ,锌极作___________ 。
(2)若闭合S2,装置属于___________ ,锌极上的反应为___________ 。
(3)若闭合S3,装置属于___________ ,总反应为___________ 。

(1)若闭合S1,装置属于
(2)若闭合S2,装置属于
(3)若闭合S3,装置属于
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】如图在A、B、C三只烧杯中各盛放稀硫酸、氯化钠溶液和硝酸银溶液

(1)图中A池是_________ (填“原电池” “电解池”或“电镀池”)。
(2)石墨1电极的名称是________ ,检验该电极反应产物的方法是_________
(3)写出以下电极的电极反应式
B池:石墨1电极_______ 石墨2电极__________
C池:Ag电极__________ Cu电极________
(4)写出B池中反应的离子方程式_______________

(1)图中A池是
(2)石墨1电极的名称是
(3)写出以下电极的电极反应式
B池:石墨1电极
C池:Ag电极
(4)写出B池中反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。请回答下列问题:

(1)甲池为_______ (填“原电池”“电解池”或“电镀池”),通入CH3OH电极的反应式为_______ 。
(2)乙池中A(石墨)电极的名称为_______ (填“正极”“负极”“阴极”或“阳极”),总反应式为_______ 。
(3)当乙池中B极质量增加21.6g时,甲池中理论上消耗O2的体积为_______ L(标准状况下),丙池中D极析出_______ g铜。
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将_______ (填“增大”“减小”或“不变”)。

(1)甲池为
(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加21.6g时,甲池中理论上消耗O2的体积为
(4)若丙中电极不变,将其溶液换成NaCl溶液,电键闭合一段时间后,甲中溶液的pH将
您最近一年使用:0次