Ⅰ. 醋酸是一种常见的弱酸,在0.1 mol·L-1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:(填“正向”、“逆向”或“不移动”,“增大”、“减小”或“不变”,填“>”、“<”或“=”)
(1)向醋酸中加入醋酸钠固体,电离平衡向_____________ 移动,pH_____________ 。
(2)向醋酸中加入碳酸钙固体,电离平衡向_____________ 移动;
(3)向醋酸中加入大量的水,c(OH-)_____________ ,导电能力_____________ 。
(1)向醋酸中加入醋酸钠固体,电离平衡向
(2)向醋酸中加入碳酸钙固体,电离平衡向
(3)向醋酸中加入大量的水,c(OH-)
更新时间:2020-11-26 21:26:36
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】25℃时0.1mol/L的醋酸溶液的pH约为3,当向其中加入醋酸钠晶体,等晶体溶解后发现溶液的pH增大。对上述现象有两种不同的解释:甲同学认为醋酸钠水解呈碱性,c(OH-)增大了,因而溶液的pH增大;乙同学认为醋酸钠溶于水电离出大量醋酸根离子,抑制了醋酸的电离,使c(H+)减小,因此溶液的pH增大。
(1)为了验证上述哪种解释正确,继续做如下实验:向0.1mol/L的醋酸溶液中加入少量下列物质中的___________ (填写编号),然后测定溶液的pH(已知25℃时,CH3COONH4溶液呈中性)。
A.固体CH3COOK B.固体CH3COONH4
C.气体NH3 D.固体NaHCO3
(2)若___________ 的解释正确(填“甲”或“乙”),(1)中溶液的pH应___________ (填“增大”、“减小”或“不变”)。
(3)常温下将0.010mol CH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液,判断:
①溶液中共有___________ 种粒子。
②其中有两种粒子的物质的量之和一定等于0.010mol,它们是___________ 和___________ 。
③溶液中n(CH3COO-)+n(OH-)-n(H+)=___________ mol
(1)为了验证上述哪种解释正确,继续做如下实验:向0.1mol/L的醋酸溶液中加入少量下列物质中的
A.固体CH3COOK B.固体CH3COONH4
C.气体NH3 D.固体NaHCO3
(2)若
(3)常温下将0.010mol CH3COONa和0.004molHCl溶于水,配制成0.5L混合溶液,判断:
①溶液中共有
②其中有两种粒子的物质的量之和一定等于0.010mol,它们是
③溶液中n(CH3COO-)+n(OH-)-n(H+)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】判断正误,错误的写出正确的关系式。
(1)0.1 mol·L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(HCO )+c(CO
)+c(CO )+c(OH-)。
)+c(OH-)。_______
(2)在Na2SO3溶液中:c(Na+)=2c(SO )+c(HSO
)+c(HSO )+c(OH-)。
)+c(OH-)。_______
(3)0.1 mol·L-1 NH4HS溶液中:c( )<c(HS-)+c(H2S)+c(S2-)。
)<c(HS-)+c(H2S)+c(S2-)。_______
(4)0.2 mol·L-1 NH4HCO3溶液(pH>7):c( )>c(H2CO3)>c(HCO
)>c(H2CO3)>c(HCO )>c(NH3·H2O) 。
)>c(NH3·H2O) 。_______
(5)室温下,0.1 mol·L-1 NH4Fe(SO4)2溶液中存在:c( )+3c(Fe3+)>2c(SO
)+3c(Fe3+)>2c(SO )。
)。_______
(1)0.1 mol·L-1 Na2CO3溶液中:c(Na+)+c(H+)=c(HCO
 )+c(CO
)+c(CO )+c(OH-)。
)+c(OH-)。(2)在Na2SO3溶液中:c(Na+)=2c(SO
 )+c(HSO
)+c(HSO )+c(OH-)。
)+c(OH-)。(3)0.1 mol·L-1 NH4HS溶液中:c(
 )<c(HS-)+c(H2S)+c(S2-)。
)<c(HS-)+c(H2S)+c(S2-)。(4)0.2 mol·L-1 NH4HCO3溶液(pH>7):c(
 )>c(H2CO3)>c(HCO
)>c(H2CO3)>c(HCO )>c(NH3·H2O) 。
)>c(NH3·H2O) 。(5)室温下,0.1 mol·L-1 NH4Fe(SO4)2溶液中存在:c(
 )+3c(Fe3+)>2c(SO
)+3c(Fe3+)>2c(SO )。
)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】人类食用醋的历史已有10000多年,有关醋的文字记载也至少有3000年,醋和食盐一样属于最古老的调味品。
Ⅰ.某兴趣小组为确定 是弱电解质并分析其中的变化,设计如下实验方案。
是弱电解质并分析其中的变化,设计如下实验方案。
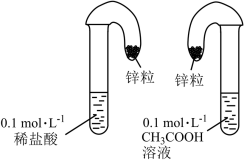
方案一:如图所示,取纯度、质量、大小相同的锌粒于两只相同气球中,同时将锌粒分别加入盛有10mL 溶液和稀盐酸的试管中,充分反应。
溶液和稀盐酸的试管中,充分反应。
方案二:用pH计测定浓度为0.1 的
的 溶液的pH。
溶液的pH。
方案三:配制pH=3的 溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
回答下列问题:
(1)方案一中,说明 是弱电解质的实验现象是
是弱电解质的实验现象是___________ (填字母)。
a.两个试管上方的气球同时鼓起,且体积一样大
b.装有盐酸的试管上方的气球鼓起慢
c.装有 的试管上方的气球鼓起慢
的试管上方的气球鼓起慢
d.装有 的试管上方的气球鼓起体积小
的试管上方的气球鼓起体积小
(2)方案二中,测得0.1 的
的 溶液的pH
溶液的pH___________ 1(填“>”“<”或“=”)。
(3)方案三中,所得醋酸溶液与pH=5的盐酸溶液,比较c(CH3COO-)___________ c(Cl-)(填“>”“<”或“=”)。
Ⅱ.完成下列问题
(4)根据 在溶液中的电离平衡移动的原理分析,为使
在溶液中的电离平衡移动的原理分析,为使 的电离程度和
的电离程度和 都减小,
都减小,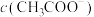 增加,可向0.1
增加,可向0.1 的
的 溶液中,选择加入的试剂是
溶液中,选择加入的试剂是___________ (填化学式)。
(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是___________ (填选项字母,下同)。
A.c(H+) B.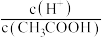 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
若该溶液升高温度,上述5种表达式的数据一定增大的是___________ 。
(6)25℃时,将amolL-1的醋酸溶液与bmolL-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,则溶液中c(Na+)___________ c(CH3COO-)(填写“>”、“=”或“<”)。
Ⅰ.某兴趣小组为确定
 是弱电解质并分析其中的变化,设计如下实验方案。
是弱电解质并分析其中的变化,设计如下实验方案。方案一:如图所示,取纯度、质量、大小相同的锌粒于两只相同气球中,同时将锌粒分别加入盛有10mL
 溶液和稀盐酸的试管中,充分反应。
溶液和稀盐酸的试管中,充分反应。
方案二:用pH计测定浓度为0.1
 的
的 溶液的pH。
溶液的pH。方案三:配制pH=3的
 溶液250mL,取5mL稀释至500mL,再用pH计测其pH。
溶液250mL,取5mL稀释至500mL,再用pH计测其pH。回答下列问题:
(1)方案一中,说明
 是弱电解质的实验现象是
是弱电解质的实验现象是a.两个试管上方的气球同时鼓起,且体积一样大
b.装有盐酸的试管上方的气球鼓起慢
c.装有
 的试管上方的气球鼓起慢
的试管上方的气球鼓起慢d.装有
 的试管上方的气球鼓起体积小
的试管上方的气球鼓起体积小(2)方案二中,测得0.1
 的
的 溶液的pH
溶液的pH(3)方案三中,所得醋酸溶液与pH=5的盐酸溶液,比较c(CH3COO-)
Ⅱ.完成下列问题
(4)根据
 在溶液中的电离平衡移动的原理分析,为使
在溶液中的电离平衡移动的原理分析,为使 的电离程度和
的电离程度和 都减小,
都减小,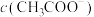 增加,可向0.1
增加,可向0.1 的
的 溶液中,选择加入的试剂是
溶液中,选择加入的试剂是(5)常温下0.1mol•L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H+) B.
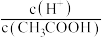 C.c(H+)∙c(OH-) D.
C.c(H+)∙c(OH-) D. E.
E.
若该溶液升高温度,上述5种表达式的数据一定增大的是
(6)25℃时,将amolL-1的醋酸溶液与bmolL-1氢氧化钠溶液等体积混合,反应后溶液恰好显中性,则溶液中c(Na+)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】化学平衡移动原理同样也适用于其他平衡,已知在氨水中存在下列平衡:
NH3+H2O NH3·H2O
NH3·H2O NH4++OH-
NH4++OH-
(1)向氨水中加入MgCl2固体时,平衡向______________ 移动,OH-的浓度_______ , NH4+的浓度_______ 。
(2)向氨水中加入浓盐酸,此时溶液中浓度减小的微粒有_______ 、_______ 、_______ 。
(3)向浓氨水中加入少量的NaOH固体,平衡向_______ 移动,此时发生的现象是____________________________ 。
NH3+H2O
 NH3·H2O
NH3·H2O NH4++OH-
NH4++OH-(1)向氨水中加入MgCl2固体时,平衡向
(2)向氨水中加入浓盐酸,此时溶液中浓度减小的微粒有
(3)向浓氨水中加入少量的NaOH固体,平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】外部因素:
电离平衡的移动符合勒夏特列原理,在分析影响电离平衡的因素的问题时,关键是要正确运用化学平衡移动的知识,既要考虑平衡移动的方向,又要考虑各物质的量的变化。注意平衡正向移动时,生成物离子浓度不一定增大,还要考虑引起平衡移动的原因。
现以0.1 mol·L-1 的CH3COOH溶液为例,分析影响电离平衡的因素及平衡移动结果。
电离方程式为CH3COOH CH3COO-+H+。
CH3COO-+H+。
电离平衡的移动符合勒夏特列原理,在分析影响电离平衡的因素的问题时,关键是要正确运用化学平衡移动的知识,既要考虑平衡移动的方向,又要考虑各物质的量的变化。注意平衡正向移动时,生成物离子浓度不一定增大,还要考虑引起平衡移动的原因。
现以0.1 mol·L-1 的CH3COOH溶液为例,分析影响电离平衡的因素及平衡移动结果。
电离方程式为CH3COOH
 CH3COO-+H+。
CH3COO-+H+。| 影响因素 | 平衡移动方向 | n(H+) | c(H+) | c(CH3COO-) | pH | 导电能力 |
| 升温(不考虑挥发) | ||||||
| 加冰醋酸 | ||||||
| 加水稀释 | ||||||
| 加CH3COONa固体 | ||||||
| 通HCl气体 | ||||||
| 加NaOH固体 | ||||||
| 加金属Zn |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】醋酸、盐酸是生活中常见的物质。
(1)25℃时,浓度均为0.1mol·L-1的盐酸和醋酸溶液,下列说法正确的是___ 。
a.两溶液的pH相同
b.两溶液的导电能力相同
c.两溶液中由水电离出的c(OH-)相同
d.中和等物质的量的NaOH,消耗两溶液的体积相同
(2)25℃时,pH均等于4的醋酸溶液和盐酸溶液,醋酸溶液中水电离出的H+浓度与盐酸溶液中水电离出的H+浓度之比是___ 。
(3)醋酸溶液中存在电离平衡:CH3COOH CH3COO-+H+,下列叙述不正确的是
CH3COO-+H+,下列叙述不正确的是___ 。
a.CH3COOH溶液中离子浓度关系满足:c(H+)=c(OH-)+c(CH3COO‾)
b.0.1mol·L-1的CH3COOH溶液加水稀释,溶液中c(OHˉ)减小
c.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动
d.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后溶液的pH>7
e.室温下pH=3的醋酸溶液加水稀释,溶液中 不变
不变
(4)常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
a.加水稀释10倍后,醋酸溶液中的c(H+)__ (填“>”“=”或“<”)盐酸溶液中的c(H+)。
b.加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸__ (填“>”“=”或“<”)盐酸。
c.使温度都升高20℃,溶液中c(H+):醋酸__ (填“>”“=”或“<”)盐酸。
d.分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是__ (填字母)。(①表示盐酸,②表示醋酸)

(5)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是__ (填字母)。
a.电离程度增大
b.溶液中离子总数增多
c.溶液导电性增强
d.溶液中醋酸分子增多
(1)25℃时,浓度均为0.1mol·L-1的盐酸和醋酸溶液,下列说法正确的是
a.两溶液的pH相同
b.两溶液的导电能力相同
c.两溶液中由水电离出的c(OH-)相同
d.中和等物质的量的NaOH,消耗两溶液的体积相同
(2)25℃时,pH均等于4的醋酸溶液和盐酸溶液,醋酸溶液中水电离出的H+浓度与盐酸溶液中水电离出的H+浓度之比是
(3)醋酸溶液中存在电离平衡:CH3COOH
 CH3COO-+H+,下列叙述不正确的是
CH3COO-+H+,下列叙述不正确的是a.CH3COOH溶液中离子浓度关系满足:c(H+)=c(OH-)+c(CH3COO‾)
b.0.1mol·L-1的CH3COOH溶液加水稀释,溶液中c(OHˉ)减小
c.CH3COOH溶液中加入少量CH3COONa固体,平衡逆向移动
d.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后溶液的pH>7
e.室温下pH=3的醋酸溶液加水稀释,溶液中
 不变
不变(4)常温下,有pH相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
a.加水稀释10倍后,醋酸溶液中的c(H+)
b.加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸
c.使温度都升高20℃,溶液中c(H+):醋酸
d.分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

(5)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是
a.电离程度增大
b.溶液中离子总数增多
c.溶液导电性增强
d.溶液中醋酸分子增多
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如右图所示。请回答:
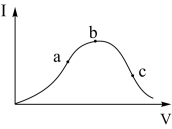
(1)a、b、c三点溶液中c(H+)由大到小的顺序为_____________ ;
(2)a、b、c三点中醋酸电离度最大的是_____________ ;
(3)若使C点溶液的c(CH3COO-)提高,在如下措施中可采取_____ (填标号)
A.通HCl气体
B.加Zn粒
C.加入固体KOH
D.加水
E.加固体CH3COONa

(1)a、b、c三点溶液中c(H+)由大到小的顺序为
(2)a、b、c三点中醋酸电离度最大的是
(3)若使C点溶液的c(CH3COO-)提高,在如下措施中可采取
A.通HCl气体
B.加Zn粒
C.加入固体KOH
D.加水
E.加固体CH3COONa
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列问题。
(1)某浓度的氨水中存在平衡:NH3·H2O⇌ +OH-。如想增大
+OH-。如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___________ (填字母)。
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
(1)某浓度的氨水中存在平衡:NH3·H2O⇌
 +OH-。如想增大
+OH-。如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】25℃时,50mL0.1mol/L醋酸中存在下述平衡:_______________________ 。若分别作如下改变,对上述平衡有何影响?
⑴加入少量冰醋酸,平衡将__________ ,溶液中c(H+)将__________ (增大、减小、不变);
⑵加入一定量蒸馏水,平衡将__________ ,溶液中c(H+)将__________ (增大、减小、不变)
⑶加入少量0.1mol/L盐酸,平衡将__________ ,溶液中c(H+)将__________ (增大、减小、不变)
⑷加入20mL0.10mol/LNaCl,平衡将__________ ,溶液中c(H+)将__________ (增大、减小、不变)
⑴加入少量冰醋酸,平衡将
⑵加入一定量蒸馏水,平衡将
⑶加入少量0.1mol/L盐酸,平衡将
⑷加入20mL0.10mol/LNaCl,平衡将
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,冰醋酸加水稀释过程中溶液的导电能力如图所示,请回答:
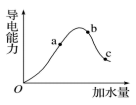
(1)a、b、c三点溶液酸性由强到弱的顺序为___________ 。
(2)若使c点溶液中的 c(CH3COO−) 提高,在如下措施中,不可选择的是______ (填字母,下同)。A.加热 B.加很稀的 NaOH 溶液 C.加固体 KOH D.加水 E.加固体 CH3COONa F.加 Zn 粒
(3)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________。

(1)a、b、c三点溶液酸性由强到弱的顺序为
(2)若使c点溶液中的 c(CH3COO−) 提高,在如下措施中,不可选择的是
(3)在稀释过程中,随着醋酸浓度的降低,下列始终保持增大趋势的量是___________。
A. |
B. 个数 个数 |
C. 分子数 分子数 |
D. |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)  Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=_______ 。
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______ c(Ur−) (填“>”、“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______ 。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
 Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程
(5)对于尿酸偏高的人群,下列建议正确的是
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
您最近一年使用:0次

 的氨水和
的氨水和 溶液加水稀释时的
溶液加水稀释时的
 点所在曲线对应的是
点所在曲线对应的是 两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。 、
、

