人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s)  Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为_______
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=_______ 。
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)_______ c(Ur−) (填“>”、“<”或“=”)。
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程_______
(5)对于尿酸偏高的人群,下列建议正确的是_______ 。
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
 Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq) ∆H >0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:①37℃时,Ka(HUr) = 4×10−6,Kw = 2.4×10−14,Ksp(NaUr) = 6.4×10−5
②37℃时,模拟关节滑液pH =7.4,c(Ur-) =4.6×10−4 mol∙L−1
(1)尿酸电离方程式为
(2)Kh为盐的水解常数,37℃时,Kh(Ur−)=
(3)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液中c(Na+)
(4)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+) = 0.2 mol∙L−1时,通过计算判断是否有NaUr晶体析出,请写出判断过程
(5)对于尿酸偏高的人群,下列建议正确的是
a.加强锻炼,注意关节保暖 b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂 d.减少摄入易代谢出尿酸的食物
2020·海南海口·模拟预测 查看更多[7]
海南省海口市2020届高三6月等级模拟试卷化学试题(已下线)第03章 物质在水溶液中的行为(A卷基础强化卷)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)海南省北京师范大学万宁附属中学2021届高三上学期第一次月考化学试题福建省福州一中2021届高三第五次模拟考试化学试题(已下线)第25讲 盐类水解(精练)-2022年高考化学一轮复习讲练测(已下线)第25讲 盐类水解(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第4讲 盐类的水解
更新时间:2021-05-27 21:32:19
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】依据醋酸的性质,请回答下列问题(以下讨论均在常温时)。
(1)取0.1mol(冰醋酸)作导电性实验,稀释过程中溶液的导电能力变化如下图所示。
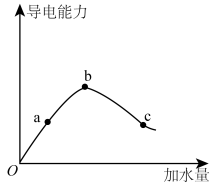
①CH3COOH的电离方程式是___________ 。
②a、b、c三点中pH最小的是___________ 。
③在稀释过程中,
___________
(2)向相同的两密闭容器中加入0.05g镁条,分别注入2mL 2mol/L盐酸、2mL 2mol/L醋酸,测得容器内压强随时间变化如下图所示。
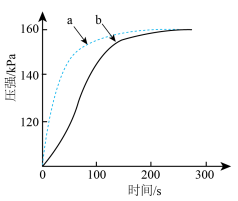
反应为醋酸的曲线是___________ (填字母)。
(1)取0.1mol(冰醋酸)作导电性实验,稀释过程中溶液的导电能力变化如下图所示。

①CH3COOH的电离方程式是
②a、b、c三点中pH最小的是
③在稀释过程中,

(2)向相同的两密闭容器中加入0.05g镁条,分别注入2mL 2mol/L盐酸、2mL 2mol/L醋酸,测得容器内压强随时间变化如下图所示。

反应为醋酸的曲线是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】常温下有浓度均为0.5mol/L的四种溶液:①Na2CO3、②NaOH、③HCl、④NH3·H2O
(1)上述溶液中,可发生水解的是___ (填序号,下同)。
(2)向④中加入少量氯化铵固体,此时 的值
的值__ (填“增大”、“减小”或“不变”)。
(3)将③和④的溶液等体积混合后溶液呈__ (填“酸”、“碱”或“中”)性,原因是__ (用离子方程式解释)。
(4)取10mL溶液③,加水稀释到500mL,则此时溶液中由水电离出的c(H+)=__ mol/L。
(1)上述溶液中,可发生水解的是
(2)向④中加入少量氯化铵固体,此时
 的值
的值(3)将③和④的溶液等体积混合后溶液呈
(4)取10mL溶液③,加水稀释到500mL,则此时溶液中由水电离出的c(H+)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
I.列出了几组物质,请将物质的合适组号填写在空格上。
(1)其中互为同分异构体的是___________ ,(CH3)2CHCH2CH3的核磁共振氢谱有___________ 组峰。
①金刚石与“足球烯”C60; ②D与T; ③16O、17O和18O; ④氧气(O2)与臭氧(O3); ⑤CH4和CH3CH2CH3; ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑦ 和(CH3)2CHCH2CH3⑧
和(CH3)2CHCH2CH3⑧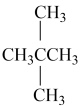 和(CH3)2CHCH2CH3
和(CH3)2CHCH2CH3
II.常温下,浓度均为0.1 mol·L-1的四种溶液:
①Na2CO3溶液 ②NaHCO3溶液 ③盐酸 ④氨水。试回答下列问题:
(2)上述溶液中有水解反应发生的是___________ (填编号,下同),溶液中溶质存在电离平衡的是___________
(3)比较等浓度的①、②溶液,pH较大的是___________
(4)在溶液④中加入少量NH4Cl固体,此时 的值将
的值将___________ (填“变小”“变大”或“不变)
I.列出了几组物质,请将物质的合适组号填写在空格上。
(1)其中互为同分异构体的是
①金刚石与“足球烯”C60; ②D与T; ③16O、17O和18O; ④氧气(O2)与臭氧(O3); ⑤CH4和CH3CH2CH3; ⑥乙醇(CH3CH2OH)和甲醚(CH3OCH3);⑦
 和(CH3)2CHCH2CH3⑧
和(CH3)2CHCH2CH3⑧ 和(CH3)2CHCH2CH3
和(CH3)2CHCH2CH3II.常温下,浓度均为0.1 mol·L-1的四种溶液:
①Na2CO3溶液 ②NaHCO3溶液 ③盐酸 ④氨水。试回答下列问题:
(2)上述溶液中有水解反应发生的是
(3)比较等浓度的①、②溶液,pH较大的是
(4)在溶液④中加入少量NH4Cl固体,此时
 的值将
的值将
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】完成下列问题。
(1)某浓度的氨水中存在平衡:NH3·H2O⇌ +OH-。如想增大
+OH-。如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___________ (填字母)。
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
(1)某浓度的氨水中存在平衡:NH3·H2O⇌
 +OH-。如想增大
+OH-。如想增大 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是a.适当升高温度 b.加入NH4Cl固体 c.通入NH3 d.加入少量浓盐酸
(2)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是
a.电离程度增大 b.溶液中离子总数增多
c.溶液导电性增强 d.溶液中醋酸分子增多
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)浓度均为0.1mol/L的CH3COOH、H2CO3、HC1O溶液,H+浓度最大的是_______ ,H3PO3的二级电离方程式为_______ ,Na2HPO3是_____ (填“正盐”或“酸式盐”)。
(2)写出下列反应的离子方程式。
①向HClO溶液中滴加少量Na2CO3溶液:__________ 。
②向NaClO溶液中通入过量CO2:_________ 。
(3)为了增大氯水的漂白性可加入_____ 。
A.NaOH B.HCl C. D.
D. E. CaCO3
E. CaCO3
(4)常温下,下列方法可以使0.1 mol·L-1 CH3COOH的电离程度增大的是_______。
(5)25 ℃时,向NaHCO3溶液中加入一定量的氨水,所得混合液的pH=8,则混合液中c( ):c(H2CO3)=
):c(H2CO3)=_______ (填数值)。
(6)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中,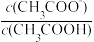 =
=_____ (填数值)。
(7)将一定浓度的氢氧化钠溶液加热,pH_____ (填“变大”“变小”或“不变”)。
(8)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是__ (填字母)。
A.c(H+) B. C.c(H+)∙c(OH﹣) D.
C.c(H+)∙c(OH﹣) D.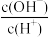 E.
E.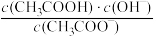
| 化学式 | CH3COOH | H2CO3 | HClO | H3PO3 |
| 电离平衡常数 | 1.7×10﹣5 | K1=4×10-7 K2=5×10﹣11 | 3.0×10﹣8 | K1=8×10-3 K2=5×10﹣6 |
(1)浓度均为0.1mol/L的CH3COOH、H2CO3、HC1O溶液,H+浓度最大的是
(2)写出下列反应的离子方程式。
①向HClO溶液中滴加少量Na2CO3溶液:
②向NaClO溶液中通入过量CO2:
(3)为了增大氯水的漂白性可加入
A.NaOH B.HCl C.
 D.
D. E. CaCO3
E. CaCO3(4)常温下,下列方法可以使0.1 mol·L-1 CH3COOH的电离程度增大的是_______。
| A.加入少量的稀盐酸 | B.加热溶液 | C.加水稀释 | D.加入少量冰醋酸 |
(5)25 ℃时,向NaHCO3溶液中加入一定量的氨水,所得混合液的pH=8,则混合液中c(
 ):c(H2CO3)=
):c(H2CO3)=(6)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中,
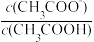 =
=(7)将一定浓度的氢氧化钠溶液加热,pH
(8)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.c(H+) B.
 C.c(H+)∙c(OH﹣) D.
C.c(H+)∙c(OH﹣) D.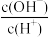 E.
E.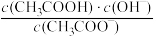
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】25℃ 时,硫氢化钾溶液里存在下列平衡:a. HS-+H2O OH-+H2S b.HS-
OH-+H2S b.HS- H++S2-
H++S2-
(1)平衡a 是__________ 平衡;平衡b是________ 平衡。(填“电 离”或“水 解”)
(2)向KHS溶液中加入氢氧化钠固体时,c(S2-)将________ (填“增 大”“ 减小”或“不 变”, 下同);向KHS溶液中通入HCl时,c(HS-)将______________ 。
(3)向KHS溶液中加入硫酸铜溶液时,有黑色沉淀(CuS)产生,则平衡a_________ (填“正向” “逆向”或“不”,下 同 )移动, 平 衡b___________ 移 动。
 OH-+H2S b.HS-
OH-+H2S b.HS- H++S2-
H++S2-(1)平衡a 是
(2)向KHS溶液中加入氢氧化钠固体时,c(S2-)将
(3)向KHS溶液中加入硫酸铜溶液时,有黑色沉淀(CuS)产生,则平衡a
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在稀氨水中存在平衡:NH3+H2O NH4++OH-,如进行下列操作,则NH3、NH4+、H+、OH-浓度及pH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3)
NH4++OH-,如进行下列操作,则NH3、NH4+、H+、OH-浓度及pH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3)____________ ,c(H+)_________ ,pH值__________ 。
(2加入少量NaOH固体时,c(NH4+)________ ,c(OH-)_______ ,PH值____ 。
(3)加入NH4Cl晶体时,c(NH4+)____________ ,c(OH-)____________ 。
 NH4++OH-,如进行下列操作,则NH3、NH4+、H+、OH-浓度及pH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3)
NH4++OH-,如进行下列操作,则NH3、NH4+、H+、OH-浓度及pH值如何变化?(试用“增大”“减小”“不变”填写。)(1)通适量HCl气体时,c(NH3)(2加入少量NaOH固体时,c(NH4+)
(3)加入NH4Cl晶体时,c(NH4+)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】写出下列反应的化学方程式。
(1)AlCl3水解溶液呈酸性________
(2)将TiCl4加入热水中生成TiO2.xH2O________
(3)向Na2S2O3溶液中加入稀硫酸__________
(4)在Mg(OH)2悬浊液中加入NH4Cl溶液,沉淀溶解___________
(1)AlCl3水解溶液呈酸性
(2)将TiCl4加入热水中生成TiO2.xH2O
(3)向Na2S2O3溶液中加入稀硫酸
(4)在Mg(OH)2悬浊液中加入NH4Cl溶液,沉淀溶解
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】【实验探究】
【实验1】在小烧杯中加入20 mL 0.1 mol·L-1 Fe(NO3)3溶液,用pH计测量该溶液的pH。
实验现象:溶液的pH___________ 7。实验结论与解释______________________ 。
【实验2】在另一只小烧杯中加入5 mL 0.1 mol·L-1 Fe(NO3)3溶液,加水稀释到50 mL,用pH计测量该溶液的pH。
实验现象:溶液的pH比稀释前___________ 。
实验结论与解释:稀释的过程中虽然FeCl3的水解平衡向正反应方向移动,但稀释对H+浓度的变化占主要优势,所以pH比稀释前大。
【实验3】在A、B、C三支试管中加入等体积0.1 mol·L-1Fe(NO3)3溶液。将A试管在酒精灯火焰上加热到溶液沸腾,向B试管中加入3滴6 mol·L-1 HNO3溶液。观察A、B试管中溶液的颜色,并与C试管中溶液的颜色比较。用化学平衡移动的原理解释上述实验现象。
实验现象:A与C比较颜色___________ ;B与C比较颜色___________ 。
实验结论与解释:加热时A中Fe(NO3)3的水解平衡向___________ 方向移动,Fe3+浓度___________ ,颜色___________ ;向B中加HNO3时,Fe(NO3)3的水解平衡向___________ 方向移动,Fe3+浓度___________ ,颜色___________ 。
【实验1】在小烧杯中加入20 mL 0.1 mol·L-1 Fe(NO3)3溶液,用pH计测量该溶液的pH。
实验现象:溶液的pH
【实验2】在另一只小烧杯中加入5 mL 0.1 mol·L-1 Fe(NO3)3溶液,加水稀释到50 mL,用pH计测量该溶液的pH。
实验现象:溶液的pH比稀释前
实验结论与解释:稀释的过程中虽然FeCl3的水解平衡向正反应方向移动,但稀释对H+浓度的变化占主要优势,所以pH比稀释前大。
【实验3】在A、B、C三支试管中加入等体积0.1 mol·L-1Fe(NO3)3溶液。将A试管在酒精灯火焰上加热到溶液沸腾,向B试管中加入3滴6 mol·L-1 HNO3溶液。观察A、B试管中溶液的颜色,并与C试管中溶液的颜色比较。用化学平衡移动的原理解释上述实验现象。
实验现象:A与C比较颜色
实验结论与解释:加热时A中Fe(NO3)3的水解平衡向
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下图所示三个烧瓶中分别装入含酚酞的0.01 mol·L-1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质。
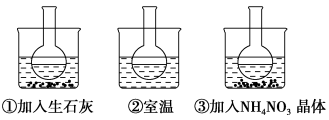
(1)含酚酞的0.01 mol·L-1 CH3COONa溶液显浅红色的原因为__________________ (用离子方程式和必要文字解释)。
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是________ (填字母序号)。
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01 mol·L-1 CH3COONa溶液中分别加入NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO-水解平衡移动的方向分别为__________ 、____________ 、____________ (填“左”、“右”或“不移动”)。

(1)含酚酞的0.01 mol·L-1 CH3COONa溶液显浅红色的原因为
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是
A.水解反应为放热反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向0.01 mol·L-1 CH3COONa溶液中分别加入NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO-水解平衡移动的方向分别为
您最近一年使用:0次



