室温下,相同体积、相同 的氨水和
的氨水和 溶液加水稀释时的
溶液加水稀释时的 变化曲线如图所示:
变化曲线如图所示:

(1) 点所在曲线对应的是
点所在曲线对应的是___________ 。(填溶液名称)
(2) 、
、 两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
___________  (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
(3) 、
、 、
、 三点溶液导电能力由大到小排序
三点溶液导电能力由大到小排序___________ 。
 的氨水和
的氨水和 溶液加水稀释时的
溶液加水稀释时的 变化曲线如图所示:
变化曲线如图所示:
(1)
 点所在曲线对应的是
点所在曲线对应的是(2)
 、
、 两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
两点溶液与同一浓度的盐酸完全反应时,消耗盐酸体积:
 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。(3)
 、
、 、
、 三点溶液导电能力由大到小排序
三点溶液导电能力由大到小排序
更新时间:2023-06-05 09:06:34
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】规律的普遍性和客观性原理
规律是事物运动过程中固有的,本质的,必然的,稳定的关系。规律是客观的不以人的意志为转移。规律既不能被创造,也不能被消灭。知道了规律的普遍性和客观性原理后,以指导我们的实践。化学的学习也要遵循规律,例如电离规律、物质的分类等都有规律可循。
(1)下列属于非电解质的是__________。
(2)下列物质中,属于弱电解质的是__________。
(3)下列物质中,属于电解质并在此状态下能导电的是__________。
(4)下列电离方程式错误的是__________。
(5)写出实验室制备氯气的离子方程式__________ 。
(6)工业上制备漂粉精的一个重要反应为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。请写出漂粉精失效原理__________ 。(化学方程式)
规律是事物运动过程中固有的,本质的,必然的,稳定的关系。规律是客观的不以人的意志为转移。规律既不能被创造,也不能被消灭。知道了规律的普遍性和客观性原理后,以指导我们的实践。化学的学习也要遵循规律,例如电离规律、物质的分类等都有规律可循。
(1)下列属于非电解质的是__________。
| A.铜 | B.盐酸 | C.氢氧化钠 | D.蔗糖 |
| A.蔗糖 | B.纯碱 | C.氢碘酸(HI)、 | D.一水合氨 |
| A.胆矾 | B.铁棒 | C.熔融的氯化铁 | D.饱和食盐水 |
| A.NaClO2=Na++Cl-+O2 |
| B.AlCl3=Al3++3Cl- |
| C. Ba(OH)2=Ba2++2OH- |
D. |
(6)工业上制备漂粉精的一个重要反应为:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。请写出漂粉精失效原理
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】某学生进行了以下四个实验并测试了溶液导电性的变化,请将实验序号和导电性图对应。

①氢氧化钠溶液中通入氯化氢气体
②氢氧化钡溶液中滴加稀硫酸
③稀氨水中滴加醋酸溶液
④蒸馏水中添加氢氧化钠固体
(1)___________
(2)___________

①氢氧化钠溶液中通入氯化氢气体
②氢氧化钡溶液中滴加稀硫酸
③稀氨水中滴加醋酸溶液
④蒸馏水中添加氢氧化钠固体
(1)
(2)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】有下列物质:①石墨;②稀硫酸;③NH3;④氨水;⑤K2S;⑥NaHSO4;⑦CH3COOH;⑧液态HCl;⑨C2H5OH
(1)下列属于强电解质的是___________ ;下列属于非电解质的是___________ 。
(2)写出⑤⑥在相应条件下的电离或水解方程式:
⑤(水溶液)___________ ;⑥(熔融) ___________ 。
(3)当②⑦⑧三种酸溶液的物质的量浓度相同时,c(H+)由大到小的顺序是___________ (填序号,下同);若②⑦⑧三种酸溶液的pH相等,则中和等体积等物质的量浓度的氢氧化钠溶液,所需酸溶液的体积由大到小的顺序是___________ 。
(1)下列属于强电解质的是
(2)写出⑤⑥在相应条件下的电离或水解方程式:
⑤(水溶液)
(3)当②⑦⑧三种酸溶液的物质的量浓度相同时,c(H+)由大到小的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】甲、乙两位同学设计用实验确定某酸HA是弱电解质,存在电离平衡,且改变条件平衡发生移动。实验方案如图:
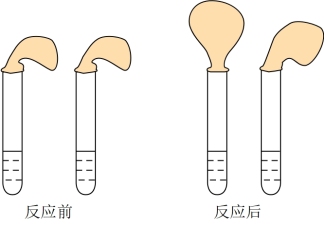
甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol∙L−1的HA、HCl溶液各10mL,按图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1 mol∙L−1HA和HCl溶液的pH;
②再取0.1 mol∙L−1的HA和HCl溶液各2滴(1滴约为 mL)分别稀释至100mL,再用pH计测其pH变化。
mL)分别稀释至100mL,再用pH计测其pH变化。
(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol∙L−1的HA溶pH____ 1(填“>”、“<”或“=”);甲方案中,说明HA是弱电解质的实验现象是:____ 。
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第____ 步,能证明改变条件弱电解质平衡发生移动。甲同学为了进一步证明弱电解质电离平衡移动的情况,设计如下实验:
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1 mol∙L−1的HA溶液中,选择加入____ 试剂(选填“A”“B’“C”“D”下同)。
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol∙L−1的HA溶液中,选择加入____ 试剂。
A.NaA固体(可完全溶于水) B.1 mol∙L−1NaOH溶液
C.1 mol∙L−1H2SO4 D.2 mol∙L−1HA

甲:取纯度相同,质量、大小相等的锌粒于两支试管中,同时加入0.1 mol∙L−1的HA、HCl溶液各10mL,按图装好,观察现象。
乙:①用pH计测定物质的量浓度均为0.1 mol∙L−1HA和HCl溶液的pH;
②再取0.1 mol∙L−1的HA和HCl溶液各2滴(1滴约为
 mL)分别稀释至100mL,再用pH计测其pH变化。
mL)分别稀释至100mL,再用pH计测其pH变化。(1)乙方案中说明HA是弱电解质的理由是:测得0.1 mol∙L−1的HA溶pH
A.加入HCl溶液后,试管上方的气球鼓起快
B.加入HA溶液后,试管上方的气球鼓起慢
C.加入两种稀酸后,两个试管上方的气球同时鼓起,且一样大
(2)乙同学设计的实验第
①使HA的电离程度和c(H+)都减小,c(A-)增大,可在0.1 mol∙L−1的HA溶液中,选择加入
②使HA的电离程度减小,c(H+)和c(A-)都增大,可在0.1 mol∙L−1的HA溶液中,选择加入
A.NaA固体(可完全溶于水) B.1 mol∙L−1NaOH溶液
C.1 mol∙L−1H2SO4 D.2 mol∙L−1HA
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】现有浓度均为0.01 mol/L的盐酸、硫酸、醋酸三种溶液,回答下列问题:
(1)分别用以上三种酸中和一定量(且等量)的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、 V3,其大小关系为______________ 。
(2)分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为_____________ 。
(3)将以上三种酸溶液稀释100倍后,pH分别变成a、b、c,其大小关系为__________ 。
(4)将上述盐酸稀释106倍后,c(H+):c(Cl-)=__________ 。
(5)常温下,某浓度的盐酸和NaOH溶液的pH之和为16,当它们按一定体积比混合时, 溶液的pH恰好等于7,则盐酸与氢氧化钠溶液的体积比是______________ 。
(1)分别用以上三种酸中和一定量(且等量)的NaOH溶液生成正盐,若需要酸的体积分别为V1、V2、 V3,其大小关系为
(2)分别与Zn反应,开始时生成H2的速率为v1、v2、v3,其大小关系为
(3)将以上三种酸溶液稀释100倍后,pH分别变成a、b、c,其大小关系为
(4)将上述盐酸稀释106倍后,c(H+):c(Cl-)=
(5)常温下,某浓度的盐酸和NaOH溶液的pH之和为16,当它们按一定体积比混合时, 溶液的pH恰好等于7,则盐酸与氢氧化钠溶液的体积比是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如右图所示。请回答:
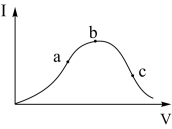
(1)a、b、c三点溶液中c(H+)由大到小的顺序为_____________ ;
(2)a、b、c三点中醋酸电离度最大的是_____________ ;
(3)若使C点溶液的c(CH3COO-)提高,在如下措施中可采取_____ (填标号)
A.通HCl气体
B.加Zn粒
C.加入固体KOH
D.加水
E.加固体CH3COONa

(1)a、b、c三点溶液中c(H+)由大到小的顺序为
(2)a、b、c三点中醋酸电离度最大的是
(3)若使C点溶液的c(CH3COO-)提高,在如下措施中可采取
A.通HCl气体
B.加Zn粒
C.加入固体KOH
D.加水
E.加固体CH3COONa
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】蚊虫、蚂蚁等叮咬人时,常向人体血液(存在平衡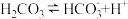 )中注入一种含有蚁酸(即甲酸,分子式为
)中注入一种含有蚁酸(即甲酸,分子式为 )的液体。
)的液体。
(1) 同
同 一样是一种有机弱酸,则
一样是一种有机弱酸,则 在溶液中的电离方程式为
在溶液中的电离方程式为______ 。
(2)当人受到蚂蚁叮咬时,皮肤上会起小疱,即使不治疗,过一段时间小疱也能痊愈,其原因是_________ 。有同学认为,受到蚂蚁叮咬时及时涂抹稀氨水或肥皂水能起到治疗作用,这一观点_______ (填“正确”或“不正确”)。
(3)已知:25℃时, 的电离平衡常数
的电离平衡常数 ,
, 的电离平衡常数
的电离平衡常数 ,
,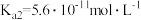 。下列说法正确的是
。下列说法正确的是________ (填标号)。
A 向 溶液中加入甲酸无明显现象
溶液中加入甲酸无明显现象
B 25℃时,向甲酸溶液中加入 溶液,
溶液, 的电离程度和
的电离程度和 均增大
均增大
C 向 甲酸溶液中加入蒸馏水,
甲酸溶液中加入蒸馏水, 增大
增大
D 向碳酸溶液中加入 固体,
固体, 减小
减小
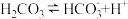 )中注入一种含有蚁酸(即甲酸,分子式为
)中注入一种含有蚁酸(即甲酸,分子式为 )的液体。
)的液体。(1)
 同
同 一样是一种有机弱酸,则
一样是一种有机弱酸,则 在溶液中的电离方程式为
在溶液中的电离方程式为(2)当人受到蚂蚁叮咬时,皮肤上会起小疱,即使不治疗,过一段时间小疱也能痊愈,其原因是
(3)已知:25℃时,
 的电离平衡常数
的电离平衡常数 ,
, 的电离平衡常数
的电离平衡常数 ,
,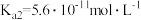 。下列说法正确的是
。下列说法正确的是A 向
 溶液中加入甲酸无明显现象
溶液中加入甲酸无明显现象B 25℃时,向甲酸溶液中加入
 溶液,
溶液, 的电离程度和
的电离程度和 均增大
均增大C 向
 甲酸溶液中加入蒸馏水,
甲酸溶液中加入蒸馏水, 增大
增大D 向碳酸溶液中加入
 固体,
固体, 减小
减小
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)浓度均为0.1mol/L的CH3COOH、H2CO3、HC1O溶液,H+浓度最大的是_______ ,H3PO3的二级电离方程式为_______ ,Na2HPO3是_____ (填“正盐”或“酸式盐”)。
(2)写出下列反应的离子方程式。
①向HClO溶液中滴加少量Na2CO3溶液:__________ 。
②向NaClO溶液中通入过量CO2:_________ 。
(3)为了增大氯水的漂白性可加入_____ 。
A.NaOH B.HCl C. D.
D. E. CaCO3
E. CaCO3
(4)常温下,下列方法可以使0.1 mol·L-1 CH3COOH的电离程度增大的是_______。
(5)25 ℃时,向NaHCO3溶液中加入一定量的氨水,所得混合液的pH=8,则混合液中c( ):c(H2CO3)=
):c(H2CO3)=_______ (填数值)。
(6)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中,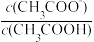 =
=_____ (填数值)。
(7)将一定浓度的氢氧化钠溶液加热,pH_____ (填“变大”“变小”或“不变”)。
(8)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是__ (填字母)。
A.c(H+) B. C.c(H+)∙c(OH﹣) D.
C.c(H+)∙c(OH﹣) D.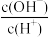 E.
E.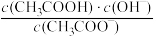
| 化学式 | CH3COOH | H2CO3 | HClO | H3PO3 |
| 电离平衡常数 | 1.7×10﹣5 | K1=4×10-7 K2=5×10﹣11 | 3.0×10﹣8 | K1=8×10-3 K2=5×10﹣6 |
(1)浓度均为0.1mol/L的CH3COOH、H2CO3、HC1O溶液,H+浓度最大的是
(2)写出下列反应的离子方程式。
①向HClO溶液中滴加少量Na2CO3溶液:
②向NaClO溶液中通入过量CO2:
(3)为了增大氯水的漂白性可加入
A.NaOH B.HCl C.
 D.
D. E. CaCO3
E. CaCO3(4)常温下,下列方法可以使0.1 mol·L-1 CH3COOH的电离程度增大的是_______。
| A.加入少量的稀盐酸 | B.加热溶液 | C.加水稀释 | D.加入少量冰醋酸 |
(5)25 ℃时,向NaHCO3溶液中加入一定量的氨水,所得混合液的pH=8,则混合液中c(
 ):c(H2CO3)=
):c(H2CO3)=(6)25℃时,CH3COOH与CH3COONa的混合溶液,若测得pH=6,则溶液中,
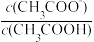 =
=(7)将一定浓度的氢氧化钠溶液加热,pH
(8)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.c(H+) B.
 C.c(H+)∙c(OH﹣) D.
C.c(H+)∙c(OH﹣) D.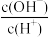 E.
E.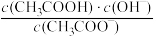
您最近一年使用:0次



