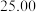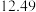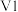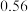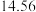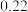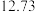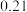弱电解质的电离平衡、盐类的水解平衡和难溶物的溶解平衡均属于化学平衡.根据要求回答问题
(1)生活中明矾常作净水剂,其净水的原理是___________ (用离子方程式表示).
(2)物质的量浓度相同的CH3COOH 溶液和NaOH 溶液混合后,溶液中c(CH3COO‾)=c(Na+),则CH3COOH 溶液的体积_____ NaOH 溶液的体积.(填“大于”、“小于”或“等于”.)
(3)常温下,取0.2mol•L﹣1 HCl溶液与0.2mol•L﹣1 MOH溶液等体积混合,测得混合溶液后的pH=5.写出MOH的电离方程式:_______________________ .
(4)含 的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的
的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的 .为了使废水的排放达标,进行如下处理:
.为了使废水的排放达标,进行如下处理:
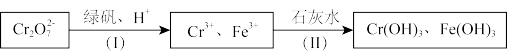
①绿矾为FeSO4•7H2O.反应(I)中Cr2O72﹣与FeSO4的物质的量之比为_____ .
②常温下若处理后的废水中c(Cr3+)=6.0×10﹣7 mol•L﹣1,则处理后的废水的pH=_____ (Ksp[Cr(OH)3]=6.0×10﹣31)
(1)生活中明矾常作净水剂,其净水的原理是
(2)物质的量浓度相同的CH3COOH 溶液和NaOH 溶液混合后,溶液中c(CH3COO‾)=c(Na+),则CH3COOH 溶液的体积
(3)常温下,取0.2mol•L﹣1 HCl溶液与0.2mol•L﹣1 MOH溶液等体积混合,测得混合溶液后的pH=5.写出MOH的电离方程式:
(4)含
 的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的
的废水毒性较大,某工厂废水中含5.0×10﹣3 mol•L﹣1的 .为了使废水的排放达标,进行如下处理:
.为了使废水的排放达标,进行如下处理: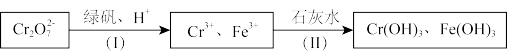
①绿矾为FeSO4•7H2O.反应(I)中Cr2O72﹣与FeSO4的物质的量之比为
②常温下若处理后的废水中c(Cr3+)=6.0×10﹣7 mol•L﹣1,则处理后的废水的pH=
更新时间:2019-12-31 10:51:38
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】按要求写出下列方程式
①已知C(s)+1/2O2(g)=CO(g)△H=-110.5kJ/mol;CO(s)+1/2O2(g)=CO2(g)△H=-283kJ/mol请写出碳完全燃烧的热化学方程式_______
②NH3・H2O电离方程式_________
③CH3COOH电离方程式_______
④NaHCO3电离方程式_______________
⑤Al(OH)3电离方程式_______
①已知C(s)+1/2O2(g)=CO(g)△H=-110.5kJ/mol;CO(s)+1/2O2(g)=CO2(g)△H=-283kJ/mol请写出碳完全燃烧的热化学方程式
②NH3・H2O电离方程式
③CH3COOH电离方程式
④NaHCO3电离方程式
⑤Al(OH)3电离方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】写出下列物质的电离方程式
A.NaHSO4________ B.NaHCO3________ C.HClO________ D.H2S________
A.NaHSO4
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】某锂电池的反应式为FePO4+Li LiFePO4,回答下列问题:
LiFePO4,回答下列问题:
(1)该蓄电池放电过程中发生还原反应的物质是___________ (写化学式),充电时外电路中转移了 电子,则阴极产物的质量为
电子,则阴极产物的质量为___________ g。
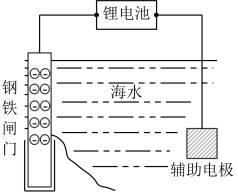
(2)为防止水体中的钢铁制品发生化学腐蚀,可采用外加电源的阴极保护法,下图是以海水中的钢铁闸门为例的保护图示,则锂电池___________ (填“正极”或“负极”)接钢铁闸门。
(3)若以该锂电池为电源,电解 稀溶液,制备
稀溶液,制备 和
和 ,则阴极的电极反应式为
,则阴极的电极反应式为___________ 。
(4)若利用该电源精炼铜。粗铜精炼过程中,因阳极杂质逐渐溶解,电解质溶液中 、
、 的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
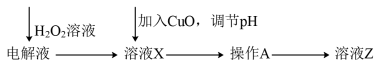
已知有关氢氧化输沉淀的pH如下表:
加入H2O2溶液时发生反应的离子方程式为___________ ;调节pH=5.0时,则沉淀的离子主要是___________ (填离子符号);操作A的名称是___________ 。该同学的方案中未除去的杂质金属阳离子是___________ 。
 LiFePO4,回答下列问题:
LiFePO4,回答下列问题:(1)该蓄电池放电过程中发生还原反应的物质是
 电子,则阴极产物的质量为
电子,则阴极产物的质量为(2)为防止水体中的钢铁制品发生化学腐蚀,可采用外加电源的阴极保护法,下图是以海水中的钢铁闸门为例的保护图示,则锂电池

(3)若以该锂电池为电源,电解
 稀溶液,制备
稀溶液,制备 和
和 ,则阴极的电极反应式为
,则阴极的电极反应式为(4)若利用该电源精炼铜。粗铜精炼过程中,因阳极杂质逐渐溶解,电解质溶液中
 、
、 的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
的浓度会逐渐增大,而这些杂质离子则会影响后续精炼。某同学设计下图所示的除杂方案:
已知有关氢氧化输沉淀的pH如下表:
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Fe(OH)2 |
| 开始沉淀时的pH | 2.3 | 5.6 | 6.2 | 7.5 |
| 完全沉淀时的pH | 3.9 | 6.4 | 8.0 | 9.7 |
加入H2O2溶液时发生反应的离子方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】现有电解质溶液:①Na2CO3②NaHCO3③NaAlO2④CH3COONa ⑤NaOH
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是______ (填编号,下同)
(2)将上述物质的量浓度均为0.1 mol/L 的五种溶液,稀释相同倍数时,其pH变化最大的是______
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,无气体产生的是______
(1)当五种溶液的pH相同时,其物质的量浓度由大到小的顺序是
(2)将上述物质的量浓度均为0.1 mol/L 的五种溶液,稀释相同倍数时,其pH变化最大的是
(3)在上述五种电解质溶液中,分别加入AlCl3溶液,无气体产生的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)实验室在配制Cu(NO3)2的溶液时,常将Cu(NO3)2固体先溶于较浓的硝酸中,再用蒸馏水稀释到所需的浓度,其目的是_______ ;
(2)已知草酸是二元弱酸,常温下测得0.1mol/L的KHC2O4的pH为4.8,则此KHC2O4溶液中c( )
)_______ c(H2C2O4)(填“<”“>”或“=”)。
(3)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是_______ (请用反应的离子方程式表示)。
(4)粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质最好选用的是_______ 。
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液至pH=4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用下列中的_______ 。
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
(2)已知草酸是二元弱酸,常温下测得0.1mol/L的KHC2O4的pH为4.8,则此KHC2O4溶液中c(
 )
)(3)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是
(4)粗制CuSO4·5H2O晶体中常含有杂质Fe2+。
①在提纯时为了除去Fe2+,常加入合适氧化剂,使Fe2+氧化为Fe3+,下列物质最好选用的是
A.KMnO4 B.H2O2 C.氯水 D.HNO3
②然后再加入适当物质调整溶液至pH=4,使Fe3+转化为Fe(OH)3,调整溶液pH可选用下列中的
A.NaOH B.NH3·H2O C.CuO D.Cu(OH)2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)HCOOH、 、HCN的酸性由强到弱的顺序为
、HCN的酸性由强到弱的顺序为______ 。
(2)向 溶液中加入足量HCN,反应的离子方程式为
溶液中加入足量HCN,反应的离子方程式为______ 。
(3)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.000mol/L的NaOH标准溶液滴定:
①用NaOH固体配制100mL,1.000mol/L的NaOH溶液,需要用到的仪器 除天平,药匙,烧杯,玻璃棒,胶头滴管,还需要______ 。实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;用标准NaOH溶液进行滴定,滴定过程中,眼睛应注视______ 。
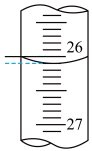
②连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为______ mL。
依据上表数据计算该HCOOH溶液的物质的量浓度为______ mol/L(计算结果保留四位有效数字)。
④下列操作中可能使所测HCOOH溶液的浓度数值偏低的是______ (填字母)。
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
(4)滴定法是一种常见的定量实验分析法,常见的滴定有酸碱中和滴定、氧化还原滴定、沉淀滴定等。
①如据反应 ,可以用碘水滴定
,可以用碘水滴定 溶液,可以选
溶液,可以选______ 作指示剂;
②用 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点,当溶液中的
反应生成砖红色沉淀指示滴定终点,当溶液中的 恰好沉淀完全(浓度为
恰好沉淀完全(浓度为 )时,溶液中的
)时,溶液中的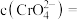
______  。(已知25℃时,
。(已知25℃时, 和AgCl的
和AgCl的 分别为
分别为 和
和 。)
。)
化学式 |
|
|
|
电离平衡常数 |
|
|
|
(1)HCOOH、
 、HCN的酸性由强到弱的顺序为
、HCN的酸性由强到弱的顺序为(2)向
 溶液中加入足量HCN,反应的离子方程式为
溶液中加入足量HCN,反应的离子方程式为(3)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.000mol/L的NaOH标准溶液滴定:
①用NaOH固体配制100mL,1.000mol/L的NaOH溶液,需要用到的
②连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为
实验序号 | 待测 |
| ||
滴定前刻度 | 滴定后刻度 | 溶液的体积 | ||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
④下列操作中可能使所测HCOOH溶液的浓度数值偏低的是
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
(4)滴定法是一种常见的定量实验分析法,常见的滴定有酸碱中和滴定、氧化还原滴定、沉淀滴定等。
①如据反应
 ,可以用碘水滴定
,可以用碘水滴定 溶液,可以选
溶液,可以选②用
 标准溶液滴定溶液中的
标准溶液滴定溶液中的 时,采用
时,采用 为指示剂,利用
为指示剂,利用 与
与 反应生成砖红色沉淀指示滴定终点,当溶液中的
反应生成砖红色沉淀指示滴定终点,当溶液中的 恰好沉淀完全(浓度为
恰好沉淀完全(浓度为 )时,溶液中的
)时,溶液中的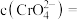
 。(已知25℃时,
。(已知25℃时, 和AgCl的
和AgCl的 分别为
分别为 和
和 。)
。)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】我国锰矿资源主要为贫碳酸锰矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。 ,
,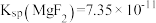 。
。
“除钙镁”后的滤液中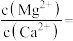
___________ 。
 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。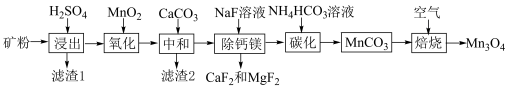
 ,
,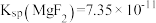 。
。“除钙镁”后的滤液中
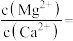
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】填空题(共12分)
(1)室温下,将等体积的氨水与盐酸溶液混合后,若混合溶液中c( )=c(Cl-),则溶液中的pH值
)=c(Cl-),则溶液中的pH值____ 7(填“>”、“<”或“=”,下同),混合前c(NH3·H2O)_____ c(HCl)
(2)等浓度的NH4Cl和氨水溶液中,水电离出的H+浓度,前者______ 后者。
(3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______ 。
(4)在配制硫化钠溶液时,为了抑制水解,可以加入少量的________ 。
(5)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10−1),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液浓度为2×10−1 mol∙L−1,则生成沉淀所需CaCl2溶液的最小浓度为________ 。
(1)室温下,将等体积的氨水与盐酸溶液混合后,若混合溶液中c(
 )=c(Cl-),则溶液中的pH值
)=c(Cl-),则溶液中的pH值(2)等浓度的NH4Cl和氨水溶液中,水电离出的H+浓度,前者
(3)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是
(4)在配制硫化钠溶液时,为了抑制水解,可以加入少量的
(5)Na2SO3溶液与CaCl2溶液混合会生成难溶的CaSO3(Ksp=3.1×10−1),现将等体积的CaCl2溶液与Na2SO3溶液混合,若混合前Na2SO3溶液浓度为2×10−1 mol∙L−1,则生成沉淀所需CaCl2溶液的最小浓度为
您最近一年使用:0次

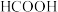

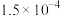
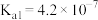
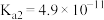

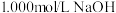 的体积
的体积