按要求科学表达下列化学用语:
(1)含20.0gNaOH的稀溶液与稀硫酸反应,放出28.7kJ的热量,表示该反应中和热的热化学反应方程式:___ 。
(2)碱性锌锰电池总反应为:2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2,写出负极电板反应__ 。
(3)氨在催化剂作用下与氧气反应生成一氧化氮,写出其化学反应方程式___ 。
(4)根据下表提供的数据,写出往NaClO溶液中通入少量CO2的离子方程式__ 。
(1)含20.0gNaOH的稀溶液与稀硫酸反应,放出28.7kJ的热量,表示该反应中和热的热化学反应方程式:
(2)碱性锌锰电池总反应为:2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2,写出负极电板反应
(3)氨在催化剂作用下与氧气反应生成一氧化氮,写出其化学反应方程式
(4)根据下表提供的数据,写出往NaClO溶液中通入少量CO2的离子方程式
| 化学式 | 电离常数 |
| HClO | K1=3×10-8 |
| H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
21-22高二上·浙江·期中 查看更多[1]
(已下线)【浙江新东方】【2021.4.27】【宁波】【高二上】【高中化学】【00136】
更新时间:2021-04-28 22:25:19
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】Ⅰ.硫元素是动植物生长不可缺少的元素,下图是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。
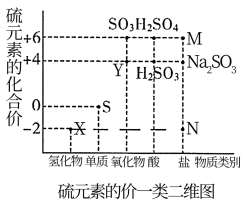
(1)图中X对应的物质是___________ ,将X气体通入 溶液中会出现淡黄色沉淀,反应物
溶液中会出现淡黄色沉淀,反应物 作
作___________ 剂(填“氧化”或“还原”)。
(2)空气中易造成硫酸酸雨的主要气体是___________ (填化学式);
(3)请写出铜和浓硫酸反应的化学方程式___________ 。
Ⅱ.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:
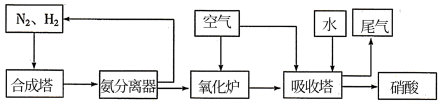
(1)氧化炉中, 转化为NO的化学方程式为
转化为NO的化学方程式为___________ 。
(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的___________ 性质。
(3)写出硝酸的电离方程式___________ 。
(4)吸收塔中出来的尾气可用 溶液吸收,主要反应为:
溶液吸收,主要反应为:
a.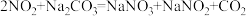
b.
根据反应b,每产生11.2L(标准状况下) ,吸收液质量将增加
,吸收液质量将增加___________ g。

(1)图中X对应的物质是
 溶液中会出现淡黄色沉淀,反应物
溶液中会出现淡黄色沉淀,反应物 作
作(2)空气中易造成硫酸酸雨的主要气体是
(3)请写出铜和浓硫酸反应的化学方程式
Ⅱ.氨和硝酸是重要的工业产品,如图是工业合成氨及制备硝酸的流程示意图:

(1)氧化炉中,
 转化为NO的化学方程式为
转化为NO的化学方程式为(2)氨分离器中压强约为15MPa,温度约为-20℃,分离氨应用了氨的
(3)写出硝酸的电离方程式
(4)吸收塔中出来的尾气可用
 溶液吸收,主要反应为:
溶液吸收,主要反应为:a.
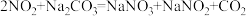
b.

根据反应b,每产生11.2L(标准状况下)
 ,吸收液质量将增加
,吸收液质量将增加
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】请写出下列反应的化学方程式:
(1)氨气的催化氧化___________ 。
(2)氯化铁溶液制作铜制印刷电路板___________ 。
(3)铜与浓硝酸反应___________ 。
(4)铝与二氧化锰反应冶炼金属锰___________ 。
(1)氨气的催化氧化
(2)氯化铁溶液制作铜制印刷电路板
(3)铜与浓硝酸反应
(4)铝与二氧化锰反应冶炼金属锰
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】氮在自然界中的转化是一个复杂的过程,如图所示的氮循环是生态系统物质循环的重要组成部分。
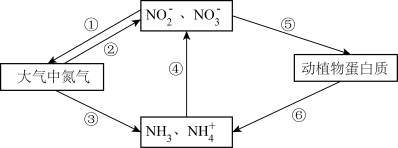
(1)循环图中能够说明含氮有机物可以转化为无机物的是___________ (填转化序号)。
(2)循环图中转化④的反应之一可表示为N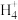 +2O2
+2O2 X+2H++H2O,写出X的化学式:
X+2H++H2O,写出X的化学式:_______ 。
(3)下列有关氮循环说法正确的是___________ 。
a. 图中转化②③④都属于氮的固定
b. 雷雨天气容易发生转化②的过程
c. 动植物蛋白质中一定含有氮元素
(4)氨气与二氧化氮在一定条件下可以发生反应,生成参与大气循环的物质,写出反应的化学方程式:______ 。

(1)循环图中能够说明含氮有机物可以转化为无机物的是
(2)循环图中转化④的反应之一可表示为N
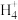 +2O2
+2O2 X+2H++H2O,写出X的化学式:
X+2H++H2O,写出X的化学式:(3)下列有关氮循环说法正确的是
a. 图中转化②③④都属于氮的固定
b. 雷雨天气容易发生转化②的过程
c. 动植物蛋白质中一定含有氮元素
(4)氨气与二氧化氮在一定条件下可以发生反应,生成参与大气循环的物质,写出反应的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】肼( )是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。 ,放出
,放出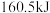 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为_______ ,消耗 液态肼放出的热量为
液态肼放出的热量为_______ 。
(2)已知: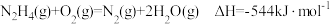 ,键能数据如下表:
,键能数据如下表:
则氮氮三键的键能为_______ ;若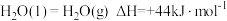 ,则
,则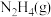 的燃烧热为
的燃烧热为_______ 。
(3)已知: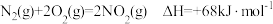 ,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为_______ 。
 )是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
)是一种良好的火箭推进剂,其与适当的氧化剂(如过氧化氢、氧气等)配合,可组成比冲最高的可贮存液体推进剂。
 ,放出
,放出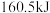 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为 液态肼放出的热量为
液态肼放出的热量为(2)已知:
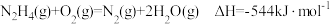 ,键能数据如下表:
,键能数据如下表:化学键 |
|
|
|
|
键能/( | 193 | 391 | 497 | 463 |
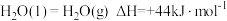 ,则
,则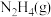 的燃烧热为
的燃烧热为(3)已知:
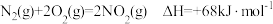 ,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
,则肼(g)和二氧化氮(g)反应生成氮气和水蒸气的热化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】家用液化气的主要成分之一是丁烷,当10kg丁烷完全燃烧并生成二氧化碳和液态水时,放出热量为5×105kJ,试写出表示丁烷燃烧的热化学方程式:_________________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)Zn﹣MnO2干电池应用广泛,其电解质溶液是ZnCl2﹣NH4Cl混合溶液。该电池的负极材料是______ .电池工作时,电子流向______ (填“正极”或“负极”)。
若ZnCl2﹣NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的反应.其主要原因是_________________ 。
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。该电池总反应式为:
Pb+PbO2+2H2SO4 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
该蓄电池放电时,电解质溶液中阴离子移向_____________ (填“正极”或“负极”);正极附近溶液的酸性_______ (填“增强”、“减弱”或“不变”)放电时,负极的电极反应式为:________________ 。
(3)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为_________________________________ 。该电池工作时,外电路每流过2 mole-,消耗标况下氧气____________ L。
(1)Zn﹣MnO2干电池应用广泛,其电解质溶液是ZnCl2﹣NH4Cl混合溶液。该电池的负极材料是
若ZnCl2﹣NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的反应.其主要原因是
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。该电池总反应式为:
Pb+PbO2+2H2SO4
 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:该蓄电池放电时,电解质溶液中阴离子移向
(3)氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】锌锰电池(俗称干电池)在生活中的用量很大。两种锌锰电池的构造如图所示。回答下列问题:
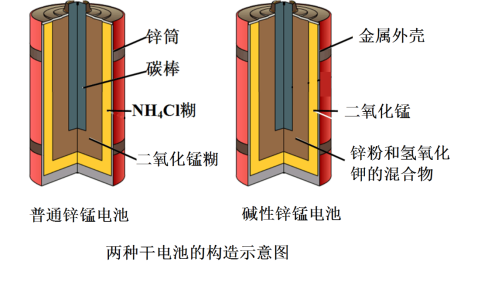
(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,该电池中,负极材料主要是______________ ,电解质的主要成分是________ ,正极发生的主要反应是________________________ 。
(2)与普通锌锰电池相比,碱性锌锰电池的优点及其理由是____________________________ 。。

(1)普通锌锰电池放电时发生的主要反应为:Zn+2NH4Cl+2MnO2=Zn(NH3)2Cl2+2MnOOH,该电池中,负极材料主要是
(2)与普通锌锰电池相比,碱性锌锰电池的优点及其理由是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】
(1)锌锰(Zn—MnO2)干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
①该电池的负极材料是_________ 。电池工作时,电子流向_____________ (填“正极”或“负极”)。
②若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是________________________ 。
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。该电池总反应式为:Pb+PbO2+2H2SO4 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:
①该蓄电池放电时,电解质溶液中阴离子移向_____________ (填“正极”或“负极”);正极附近溶液的酸性_____________ (填“增强”、“减弱”或“不变”)放电时,负极的电极反应式为:_____________________________ (用离子方程式表示)。(已知:硫酸铅为不溶于水的白色沉淀,生成时附着在电极上)
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050 mol Cl2,这时电池内消耗的H2SO4的物质的量至少是________________ 。氢氧燃料电池具有启动快、效率高等优点,其能量密度高于铅蓄电池。若电解质为KOH溶液,则氢氧燃料电池的负极反应式为___________________ 。该电池工作时,外电路每流过2 mol e-,消耗标况下氧气_________ L。
(1)锌锰(Zn—MnO2)干电池应用广泛,其电解质溶液是ZnCl2—NH4Cl混合溶液。
①该电池的负极材料是
②若ZnCl2—NH4Cl混合溶液中含有杂质Cu2+,会加速某电极的腐蚀,其主要原因是
(2)铅蓄电池是常用的化学电源,其电极材料分别是Pb和PbO2,电解液为硫酸。该电池总反应式为:Pb+PbO2+2H2SO4
 2PbSO4+2H2O。请根据上述情况判断:
2PbSO4+2H2O。请根据上述情况判断:①该蓄电池放电时,电解质溶液中阴离子移向
②实验室用铅蓄电池作电源电解饱和食盐水制取氯气,今若制得0.050 mol Cl2,这时电池内消耗的H2SO4的物质的量至少是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】弱电解质的研究是重要课题。
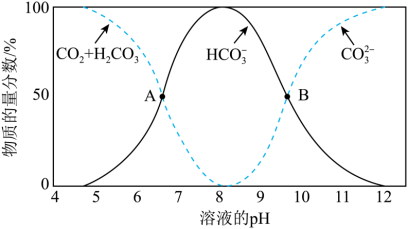
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不正确的是_______ 。
A.pH=8时,溶液中含碳元素的微粒主要是HCO
B.A点,溶液中H2CO3和HCO 浓度相同
浓度相同
C.当c(HCO )=c(CO
)=c(CO )时,c(H+)>c(OH-)
)时,c(H+)>c(OH-)
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是_______ 。
(2)H2CO3以及其它部分弱酸的电离平衡常数如下表。
按要求回答下列问题:
①H2S、H2CO3、HClO的酸性由强到弱的顺序为_______ 。
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:_______ 。
③取等体积等pH的醋酸和次氯酸两种溶液,分别用等浓度的NaOH稀溶液恰好完全中和时,消耗NaOH溶液的体积分别为V1,V2,则大小关系为:V1_______ V2 (填“>”、“<”或“=”)。
(1)①已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不正确的是

A.pH=8时,溶液中含碳元素的微粒主要是HCO

B.A点,溶液中H2CO3和HCO
 浓度相同
浓度相同C.当c(HCO
 )=c(CO
)=c(CO )时,c(H+)>c(OH-)
)时,c(H+)>c(OH-)②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是
(2)H2CO3以及其它部分弱酸的电离平衡常数如下表。
| 弱酸 | H2S | H2CO3 | HClO | CH3COOH |
| 电离平衡常数(25℃) | K1=1.3×10﹣7 K2=7.1×10﹣15 | K1=4.4×10﹣7 K2=4.7×10﹣11 | K=3.0×10﹣8 | Ka=1.8x10-5 |
按要求回答下列问题:
①H2S、H2CO3、HClO的酸性由强到弱的顺序为
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:
③取等体积等pH的醋酸和次氯酸两种溶液,分别用等浓度的NaOH稀溶液恰好完全中和时,消耗NaOH溶液的体积分别为V1,V2,则大小关系为:V1
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在-50 ℃时液氨中存在着下列平衡:2NH3⇌NH +NH
+NH ,两种离子的平衡浓度均为1.0×10-15mol·L-1。
,两种离子的平衡浓度均为1.0×10-15mol·L-1。
(1)液氨中离子积为_______ ;
(2)向液氨中加入氨基钠(NaNH2),液氨的离子积_______ ;向液氨中加入NH4Cl,c(NH )增大,离子积的数值
)增大,离子积的数值_______ 。
 +NH
+NH ,两种离子的平衡浓度均为1.0×10-15mol·L-1。
,两种离子的平衡浓度均为1.0×10-15mol·L-1。(1)液氨中离子积为
(2)向液氨中加入氨基钠(NaNH2),液氨的离子积
 )增大,离子积的数值
)增大,离子积的数值
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】25℃时,醋酸、次氯酸、碳酸和亚硫酸电离平衡常数分别为:醋酸K=1.75×10-5;次氯酸K=2.95×10-8;碳酸K1=4.30×10-7,K2=5.61×10-11;亚硫酸K1=1.54×10-2,K2=1.02×10-7
(1)写出碳酸的第一级电离平衡常数表达式K1=___________ 。
(2)在相同条件下,等浓度的CH3COO-、ClO-、CO32-和SO32-溶液中结合H+能力最强的是___________ 。
(3)已知下面三个数据:6.3×10-4、5.6×10-4、6.2×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2;NaNO2+HF=HNO2+NaF.由此可判断下列叙述不正确的是___________
(1)写出碳酸的第一级电离平衡常数表达式K1=
(2)在相同条件下,等浓度的CH3COO-、ClO-、CO32-和SO32-溶液中结合H+能力最强的是
(3)已知下面三个数据:6.3×10-4、5.6×10-4、6.2×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2;NaNO2+HF=HNO2+NaF.由此可判断下列叙述不正确的是___________
| A.Ka(HF)=6.3×10-4 |
| B.Ka(HNO2)=6.2×10-10 |
| C.三种酸的强弱顺序为HF>HNO2>HCN |
| D.Ka(HCN)<Ka(HNO2)<Ka(HF) |
您最近一年使用:0次





 )
)

