含物质的量相同的CH3COOH和CH3COONa混合溶液中:
(1)写出所有电离、水解离子方程式:_______ 。
(2)粒子浓度由大到小顺序为_______ 。
(3)电荷守恒:_______ 。
(4)物料守恒:_______ 。
(1)写出所有电离、水解离子方程式:
(2)粒子浓度由大到小顺序为
(3)电荷守恒:
(4)物料守恒:
更新时间:2023-09-17 19:25:17
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)H3PO2是一元中强酸,写出其电离方程式_______________________________ 。NaH2PO2为__________ (填“正盐”或“酸式盐”),其溶液显__________ (填“弱酸性”、“中性”或“弱碱性”)
(2)下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
经某一工艺处理后的废水pH=8,常温下,该废水中Zn2+的浓度为__________ mg·L-1(常温下, Ksp[Zn(OH)2]=1.2×10-17),__________ (填“符合”或“不符合”)国家环保标准。
(2)下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
| 冷轧含锌废水水质 | 经处理后的水国家环保标准值 | |
| Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
| pH | 1~5 | 6~9 |
| SO42-浓度/(mg·L-1) | ≤23 000 | ≤150 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式:_______________________ 。
②n越大,直链聚磷酸铵的水溶性越_______________ (填“大”或“小”)。
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。

______________________________________
(3)由工业白磷 (含少量砷、铁、镁等) 制备高纯白磷 ( 熔点44℃,沸点280℃),主要生产流程如下:
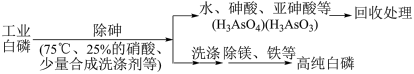
①除砷过程在75 ℃下进行,其合理的原因是__________ (填字母)。
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是_________________________________ 。
③除砷过程中,合成洗涤剂起到________________ 作用。
④硝酸氧化除砷时被还原为NO,写出砷转化为砷酸的化学方程式:_______________ 。
氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越______ (填“多”或“少”)。
⑤某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是_______ 。

(1)直链聚磷酸是由n个磷酸分子通过分子间脱水形成的,常用于制取阻燃剂聚磷酸铵。
①写出磷酸主要的电离方程式:
②n越大,直链聚磷酸铵的水溶性越
(2)在碱性条件下,次磷酸盐可用于化学镀银,完成其反应的离子方程式。

(3)由工业白磷 (含少量砷、铁、镁等) 制备高纯白磷 ( 熔点44℃,沸点280℃),主要生产流程如下:
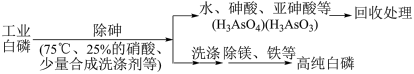
①除砷过程在75 ℃下进行,其合理的原因是
a.使白磷熔化,提高反应活性
b.降低白磷的毒性
c.温度不宜过高,防止硝酸分解
d.适当提高温度,增大反应速率
②生产过程在高纯氮气保护下进行,其目的是
③除砷过程中,合成洗涤剂起到
④硝酸氧化除砷时被还原为NO,写出砷转化为砷酸的化学方程式:
氧化相同质量的砷,当转化为亚砷酸的量越多,消耗硝酸的量越
⑤某条件下,用一定量的硝酸处理一定量的工业白磷,砷的脱除率及磷的产率随硝酸质量分数的变化如图,砷的脱除率从a点到b点降低的原因是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】常温下,将0.01 mol NH4Cl和 0.002 mol NaOH 溶于水配成1 L混合溶液,
(1)该溶液中存在的三个平衡体系是:______________________________ 、
_______________________________ 、_______________________________ 。
(2)溶液中共有_______ 种不同的粒子。
(3)这些粒子中浓度为0.01 mol/L 的是_________ ,浓度为0.002 mol/L 的是_________ 。
(4)物质的量之和为0.01 mol的两种粒子是:___________ 和______________ 。
(5)_______ 和_______ 两种离子数量之和比OH-多0.008mol。
(1)该溶液中存在的三个平衡体系是:
(2)溶液中共有
(3)这些粒子中浓度为0.01 mol/L 的是
(4)物质的量之和为0.01 mol的两种粒子是:
(5)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】为探究 溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
(1)配制:50 mL 1.0 mol⋅L-1的 溶液,测其pH约为0.7,即
溶液,测其pH约为0.7,即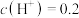 mol⋅L-1。用离子方程式解释
mol⋅L-1。用离子方程式解释 溶液呈酸性的原因:
溶液呈酸性的原因:___________ 。
(2)小组同学利用上述 溶液探究其与足量锌粉的反应。实验操作及现象如表:
溶液探究其与足量锌粉的反应。实验操作及现象如表:
已知:Zn的性质与Al相似,能发生反应:
①红褐色沉淀是:___________ (填化学式),结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:___________ 。
②反应后溶液为浅绿色,写出相关反应的离子方程式:___________ 。
③分离出黑色固体,经下列实验证实了其中含有的主要物质。
ⅰ.黑色固体可以被磁铁吸引;
ⅱ.向黑色固体中加入足量的NaOH溶液,产生气泡;
ⅲ.将ⅱ中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
ⅳ.向ⅲ反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是___________ 。
b.小组同学认为上述实验无法确定黑色固体中是否含有 ,理由是
,理由是___________ 。
(3)为进一步探究上述1.0 mol⋅L-1 溶液中
溶液中 和
和 氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
小组同学得出结论:在1.0 mol⋅L-1  溶液中,
溶液中, 的氧化性比
的氧化性比 更强。
更强。
 溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
溶液中的离子平衡和离子反应,某小组同学进行了如下实验。(1)配制:50 mL 1.0 mol⋅L-1的
 溶液,测其pH约为0.7,即
溶液,测其pH约为0.7,即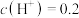 mol⋅L-1。用离子方程式解释
mol⋅L-1。用离子方程式解释 溶液呈酸性的原因:
溶液呈酸性的原因:(2)小组同学利用上述
 溶液探究其与足量锌粉的反应。实验操作及现象如表:
溶液探究其与足量锌粉的反应。实验操作及现象如表:| 操作 | 现象 |
向反应瓶中加入6.5 g锌粉,然后加入50 mL 1.0 mol·L 的 的 溶液,搅拌 溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |

①红褐色沉淀是:
②反应后溶液为浅绿色,写出相关反应的离子方程式:
③分离出黑色固体,经下列实验证实了其中含有的主要物质。
ⅰ.黑色固体可以被磁铁吸引;
ⅱ.向黑色固体中加入足量的NaOH溶液,产生气泡;
ⅲ.将ⅱ中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
ⅳ.向ⅲ反应后的溶液中滴加KSCN溶液,无变化。
a.黑色固体中一定含有的物质是
b.小组同学认为上述实验无法确定黑色固体中是否含有
 ,理由是
,理由是(3)为进一步探究上述1.0 mol⋅L-1
 溶液中
溶液中 和
和 氧化性的相对强弱,继续实验并观察到反应开始时现象如表:
氧化性的相对强弱,继续实验并观察到反应开始时现象如表:| 操作 | 现象 |
将5 mL 1.0 mol⋅L-1的 溶液与0.65 g锌粉混合 溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将 | 溶液中立即产生大量气泡 |
 溶液中,
溶液中, 的氧化性比
的氧化性比 更强。
更强。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】弱电解质的电离平衡、盐类的水解平衡均属于化学平衡。根据要求回答问题
(1)生活中明矾常作净水剂,其净水的原理是_______ (结合方程式说明)。
(2)常温下,取 盐酸与
盐酸与 碱MOH溶液等体积混合,测得混合溶液后的
碱MOH溶液等体积混合,测得混合溶液后的 ,写出MOH的电离方程式
,写出MOH的电离方程式_______ 。
(3)室温下, 的NaHA溶液中,测得溶液显碱性。则
的NaHA溶液中,测得溶液显碱性。则
①该溶液中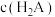
_______ 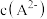 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②作出上述判断的依据是_______ (用文字解释)。
(4)常温下向含有1mol溶质的稀盐酸中缓慢通入1mol (溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是
(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是_______ ;在通入 的过程中溶液的导电能力
的过程中溶液的导电能力_______ (选填“变大”、“变小”或“几乎不变”)。
(5) 溶液与NaOH溶液混合至中性,则
溶液与NaOH溶液混合至中性,则
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)生活中明矾常作净水剂,其净水的原理是
(2)常温下,取
 盐酸与
盐酸与 碱MOH溶液等体积混合,测得混合溶液后的
碱MOH溶液等体积混合,测得混合溶液后的 ,写出MOH的电离方程式
,写出MOH的电离方程式(3)室温下,
 的NaHA溶液中,测得溶液显碱性。则
的NaHA溶液中,测得溶液显碱性。则①该溶液中
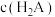
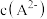 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②作出上述判断的依据是
(4)常温下向含有1mol溶质的稀盐酸中缓慢通入1mol
 (溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是
(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是 的过程中溶液的导电能力
的过程中溶液的导电能力(5)
 溶液与NaOH溶液混合至中性,则
溶液与NaOH溶液混合至中性,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Na2S又称臭碱、硫化碱,是应用广泛的化工原料,也常用于吸收工业废气中的SO2。完成下列填空:
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因___ 。
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式___ 。结合你所学习过的其它离子反应分析,离子互换反应进行的方向是___ 。
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐___ (填“变大”、“变小”),生成的沉淀是___ ;
(4)关于反应后得到的溶液,下列离子浓度关系正确的是___ 。
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
(1)用离子方程式说明Na2S又称臭碱、硫化碱的原因
(2)向AgCl悬浊液中滴加Na2S溶液,生成黑色沉淀,写出反应的离子方程式
向Na2S溶液中不断通入SO2,直至不再能吸收。其间看到溶液变浑浊,停止反应后溶液中含硫微粒为:S2O32-、HSO3-、H2SO3、HS-。
(3)反应过程中,溶液的pH逐渐
(4)关于反应后得到的溶液,下列离子浓度关系正确的是
a.c(Na+)=c(S2O32-) +2c(HSO3-)+2c(H2SO3) + 2c(HS-)
b.c(Na+)+c(H+)=2c(S2O32-)+c(HSO3-) +c(HS-) +c(OH-)
c.c(Na+)=2c(HS-)
d.c(Na+)=2c(HS-)+2c(S2O32-)+c(HSO3-)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】常温下,NaOH和CH3COOH等浓度按1∶2体积比混合后pH<7
(1)溶液中粒子浓度的大小关系:_______ (水分子除外)。
(2)电荷守恒:_______ 。
(3)元素质量守恒:_______ 。
(4)质子守恒:_______ 。
(1)溶液中粒子浓度的大小关系:
(2)电荷守恒:
(3)元素质量守恒:
(4)质子守恒:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在含有弱电解质的溶液中,往往有多个平衡共存。
(1)常温下,将 的某一元酸
的某一元酸 溶液和
溶液和 的
的 溶液等体积混合后溶液的
溶液等体积混合后溶液的 大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是
大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是___________ (填字母)。
A.
B.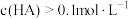
C.
(2)常温下,向 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳元素的各种微粒(
溶液,溶液中含碳元素的各种微粒( 因逸出未画出)的物质的量分数(纵轴)随溶液的
因逸出未画出)的物质的量分数(纵轴)随溶液的 变化的部分情况如图所示。
变化的部分情况如图所示。

①在同一溶液中,
___________ (填“能”或“不能”)大量共存。
②当 时,溶液中
时,溶液中
___________ (填“>”、“<”或“=”)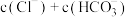 。
。
③ 时,
时, 水解反应的平衡常数
水解反应的平衡常数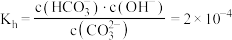 ,当溶液中
,当溶液中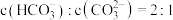 时,溶液的
时,溶液的
___________ 。
(3) 虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比
虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。
① 在溶液中分三步水解:
在溶液中分三步水解:


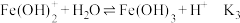
上述水解反应的平衡常数 由大到小的顺序是
由大到小的顺序是___________ 。
②通过控制条件,上述水獬产物聚合,生成聚合氯化铁,其离子方程式为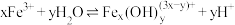 ,欲使平衡正向移动可采用的措施是
,欲使平衡正向移动可采用的措施是___________ (填字母)。
a.加水稀释 b.降温 c.加入
(1)常温下,将
 的某一元酸
的某一元酸 溶液和
溶液和 的
的 溶液等体积混合后溶液的
溶液等体积混合后溶液的 大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是
大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是A.

B.
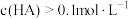
C.

(2)常温下,向
 溶液中逐滴加入
溶液中逐滴加入 溶液,溶液中含碳元素的各种微粒(
溶液,溶液中含碳元素的各种微粒( 因逸出未画出)的物质的量分数(纵轴)随溶液的
因逸出未画出)的物质的量分数(纵轴)随溶液的 变化的部分情况如图所示。
变化的部分情况如图所示。
①在同一溶液中,

②当
 时,溶液中
时,溶液中
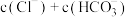 。
。③
 时,
时, 水解反应的平衡常数
水解反应的平衡常数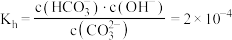 ,当溶液中
,当溶液中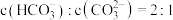 时,溶液的
时,溶液的
(3)
 虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比
虽然具有净水作用,但是会腐蚀设备。聚合氯化铁是一种新型的絮凝剂,处理污水比 高效,且腐蚀性小。
高效,且腐蚀性小。①
 在溶液中分三步水解:
在溶液中分三步水解:

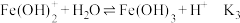
上述水解反应的平衡常数
 由大到小的顺序是
由大到小的顺序是②通过控制条件,上述水獬产物聚合,生成聚合氯化铁,其离子方程式为
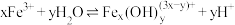 ,欲使平衡正向移动可采用的措施是
,欲使平衡正向移动可采用的措施是a.加水稀释 b.降温 c.加入

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)25℃时,浓度为0.1 mol·L-1的6种溶液:①HCl,②CH3COOH ③Ba(OH)2④Na2CO3⑤KCl ⑥NH4Cl溶液pH由小到大的顺序为_______________ (填写编号)
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=_______ mol·L-1(保留到小数点后一位)。
(3)25℃时,pH=3 的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈________ (填“酸性”,“中性”或“碱性”),请写出溶液中离子浓度间的一个等式:________________________________ 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH= 7,则溶液中c (CH3COO-)+c(CH3COOH)=_____________ ,m与n的大小关系是m_____ n (填“>”“=”或“<”)。
(5)当300mL 1 mol·L-1的NaOH 溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为_________________________________________ 。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=
(3)25℃时,pH=3 的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH= 7,则溶液中c (CH3COO-)+c(CH3COOH)=
(5)当300mL 1 mol·L-1的NaOH 溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】探究金属钠与水或盐酸的反应,记录如下:
(1)由实验现象可推断:金属钠与水或盐酸的反应,反应的共同特征是___________ (写出两点)。
(2)研究实验I
①实验前水中
___________ ;
②实验结束后所得溶液显碱性,原因可能是___________ (填序号)。
a.生成的氢氧化钠属于碱
b.氢氧化钠在水中能电离出
c.氢氧化钠抑制了水的电离,导致由水电离产生的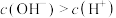
d.钠与 反应,促进水的电离,导致
反应,促进水的电离,导致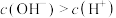
(3)研究实验II:实验结束后,溶液中离子浓度由大到小的顺序是___________ 。
| 实验序号 | 实验内容 | 实验现象 |
| I | 室温下,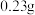 钠与 钠与 蒸馏水 蒸馏水 | 钠浮在水面上,熔成小球四处游动,发出嘶嘶响声, 后钠块消失 后钠块消失 |
| II | 室温下,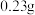 钠与 钠与  盐酸 盐酸 | 钠浮在水面上,熔成小球四处游动,发出嘶嘶响声,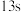 后钠块消失 后钠块消失 |
(2)研究实验I
①实验前水中

②实验结束后所得溶液显碱性,原因可能是
a.生成的氢氧化钠属于碱
b.氢氧化钠在水中能电离出

c.氢氧化钠抑制了水的电离,导致由水电离产生的
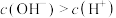
d.钠与
 反应,促进水的电离,导致
反应,促进水的电离,导致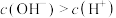
(3)研究实验II:实验结束后,溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】现有常温下甲、乙、丙三种溶液,甲为0.1mol•L-1的NaOH溶液,乙为0.1mol•L-1的HCl溶液,丙为0.1mol•L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的c(H+)=______ ,pH=______ 。
(2)丙溶液中存在的两个电离平衡为______ (用电离平衡方程式表示)。
(3)常温下,用水稀释0.1mol•L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是______ (填序号)。
①n(H+) ②c(H+) ③ ④c(OH-)
④c(OH-)
(4)乙、丙两种溶液中水电离程度大小顺序为______ 。
(5)将等体积的甲、丙溶液混合,充分反应后,得到的溶液中离子浓度由大到小为______ ;溶液中电荷守恒______ (用粒子浓度形式表示)。
(1)甲溶液的c(H+)=
(2)丙溶液中存在的两个电离平衡为
(3)常温下,用水稀释0.1mol•L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是
①n(H+) ②c(H+) ③
 ④c(OH-)
④c(OH-)(4)乙、丙两种溶液中水电离程度大小顺序为
(5)将等体积的甲、丙溶液混合,充分反应后,得到的溶液中离子浓度由大到小为
您最近一年使用:0次

 溶液中
溶液中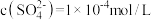 ,则该溶液中
,则该溶液中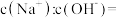
 的
的 ,该温度下,纯水的
,该温度下,纯水的
 的
的 与
与 的
的 溶液
溶液 混合,所得混合液为中性,则
混合,所得混合液为中性,则
 溶液
溶液 ,
,
 ;
;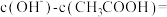
 的
的 和
和 的混合液中逐渐加入
的混合液中逐渐加入 粉末,当溶液中
粉末,当溶液中 浓度下降到
浓度下降到 时,
时, 开始沉淀。已知:
开始沉淀。已知: 时,
时,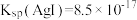 ;
;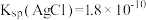 。
。


