(1)H3PO2是一元中强酸,写出其电离方程式_______________________________ 。NaH2PO2为__________ (填“正盐”或“酸式盐”),其溶液显__________ (填“弱酸性”、“中性”或“弱碱性”)
(2)下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
经某一工艺处理后的废水pH=8,常温下,该废水中Zn2+的浓度为__________ mg·L-1(常温下, Ksp[Zn(OH)2]=1.2×10-17),__________ (填“符合”或“不符合”)国家环保标准。
(2)下表列出了某冷轧厂排放的废水中各成分的含量及国家环保标准值的有关数据:
| 冷轧含锌废水水质 | 经处理后的水国家环保标准值 | |
| Zn2+浓度/(mg·L-1) | ≤800 | ≤3.9 |
| pH | 1~5 | 6~9 |
| SO42-浓度/(mg·L-1) | ≤23 000 | ≤150 |
更新时间:2018-03-18 19:06:19
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有下列六种物质:①铝 ②CH3COOH ③CO2 ④液态HCl ⑤NaOH溶液 ⑥红褐色的氢氧化铁胶体
(1)上述物质中属于电解质的有_______ (填序号,下同),能导电的是_______ 。
(2)写出②④在水中的电离方程式:_______ 、_______ 。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为H++OH-=H2O,则该反应的化学方程式为_______ 。
(1)上述物质中属于电解质的有
(2)写出②④在水中的电离方程式:
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为H++OH-=H2O,则该反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知25℃时,CH3COOH和NH3·H2O的电离平衡常数分别为Ka(CH3COOH)=l.7×10-5mol/L,Kb(NH3·H2O)=1.7×l0-5mol/L。现有常温下1 mol/L的醋酸溶液和l mol/L的氨水,且知醋酸溶液的pH=a,试回答下列问题:
(1)醋酸溶液中存在的电离平衡用电离方程式表示为_______ ,
(2)将上述两种溶液等体积混合,所得溶液的pH=_______ 。
(3)饱和氯化铵溶液显酸性,原因是(用离子方程式表示)_______ ;向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解。甲、乙两位同学分别提出了不同的解释:
甲同学:由于NH4+水解呈酸性,其H+结合Mg(OH)2电离的OH-,使Mg(OH)2溶解
乙同学:由于Mg(OH)2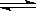 Mg2++2OH-,NH4++OH-
Mg2++2OH-,NH4++OH-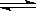 NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释
NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释__________ 。
(1)醋酸溶液中存在的电离平衡用电离方程式表示为
(2)将上述两种溶液等体积混合,所得溶液的pH=
(3)饱和氯化铵溶液显酸性,原因是(用离子方程式表示)
甲同学:由于NH4+水解呈酸性,其H+结合Mg(OH)2电离的OH-,使Mg(OH)2溶解
乙同学:由于Mg(OH)2
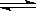 Mg2++2OH-,NH4++OH-
Mg2++2OH-,NH4++OH-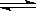 NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释
NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】已知25℃时有关弱酸的电离常数如表:
(1)25℃时,将20mL0.1mol·L-1CH3COOH溶液和20mL0.1mol·L-1HSCN溶液分别与20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示。
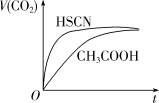
反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是___ 。
(2)若保持温度不变,在醋酸溶液中通入一定量氨,下列量会变小的是___ (填字母)。
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸的电离常数
| 弱酸 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
(1)25℃时,将20mL0.1mol·L-1CH3COOH溶液和20mL0.1mol·L-1HSCN溶液分别与20mL0.1mol·L-1NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图所示。

反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是
(2)若保持温度不变,在醋酸溶液中通入一定量氨,下列量会变小的是
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸的电离常数
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.已知:在相同条件下醋酸与氨水电离程度相同,现有浓度均为0.1mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵、⑧氨水。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是 填序号
填序号
____ 。
(2)若④、⑤、⑥、⑦、⑧五种溶液中NH 浓度相等,则五种溶液的物质的量浓度由大到小的顺序是
浓度相等,则五种溶液的物质的量浓度由大到小的顺序是 填序号
填序号
___ 。
Ⅱ 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(3)pH相等的下列溶液,它们的物质的量浓度由大到小排列的顺序是____ (用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:____ 。
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=____ (填准确数值 。
。
(6)25℃时,将amol•L-1的醋酸与bmol•L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____ 。
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是
 填序号
填序号
(2)若④、⑤、⑥、⑦、⑧五种溶液中NH
 浓度相等,则五种溶液的物质的量浓度由大到小的顺序是
浓度相等,则五种溶液的物质的量浓度由大到小的顺序是 填序号
填序号
Ⅱ
 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1.8×10-5 | Ka1=4,.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(4)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(5)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)=
 。
。(6)25℃时,将amol•L-1的醋酸与bmol•L-1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】常温下,几种酸的电离常数如表所示:
(1)常温下,CH3COOH、HClO、H2CO3的酸性由强到弱的顺序为______ 。
(2)HCO 的电离平衡常数表达式为K=
的电离平衡常数表达式为K=______ 。
(3)常温下,实验测得某人血液中c(HCO )=2.3×10-2mol·L-1,c(H2CO3)=2.3×10-3mol·L-1,则该人血液呈
)=2.3×10-2mol·L-1,c(H2CO3)=2.3×10-3mol·L-1,则该人血液呈______ (填“酸性”“中性”或“碱性”)。
(4)常温下,pH=10的Na2CO3溶液中,由水电离的c(OH-)=______ 。
(5)常温下,等浓度的CH3COONa、NaClO、Na2CO3溶液的pH由大到小的顺序为______ (用溶质的化学式表示)。
(6)某温度下,向CH3COOH溶液中滴加NaOH溶液c(CH3COOH)、c(CH3COO-)与pH的关系如图所示,则该温度下Ka(CH3COOH)=______ 。

| 弱酸 | CH3COOH | HClO | H2CO3 |
| 电离平衡常数 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.5×10-7 Ka2=4.7×10-11 |
(2)HCO
 的电离平衡常数表达式为K=
的电离平衡常数表达式为K=(3)常温下,实验测得某人血液中c(HCO
 )=2.3×10-2mol·L-1,c(H2CO3)=2.3×10-3mol·L-1,则该人血液呈
)=2.3×10-2mol·L-1,c(H2CO3)=2.3×10-3mol·L-1,则该人血液呈(4)常温下,pH=10的Na2CO3溶液中,由水电离的c(OH-)=
(5)常温下,等浓度的CH3COONa、NaClO、Na2CO3溶液的pH由大到小的顺序为
(6)某温度下,向CH3COOH溶液中滴加NaOH溶液c(CH3COOH)、c(CH3COO-)与pH的关系如图所示,则该温度下Ka(CH3COOH)=

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】已知某溶液中只存在OH-、H+、CH3COO-、Na+四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+) ②c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
③c(CH3COO-)=c(Na+)>c(H+)=c(OH-) ④c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
(1)若溶液中只溶解了一种溶质,则该溶质是________ (填物质名称),上述四种离子浓度的大小顺序为________________________________ (填编号)。
(2)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好反应,则混合前两溶液的物质的量浓度大小关系为c(NaOH)________ c(CH3COOH)(填“大于”“小于”或“等于”,下同),混合前酸中c(H+)和碱中c(OH-)的关系是c(H+)________ c(OH-)。
(3)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好呈中性,则混合前两溶液的物质的量浓度大小关系为c(NaOH)________ c(CH3COOH)(填“大于”“小于”或“等于”),混合后溶液中的各离子浓度的大小关系_________________________________ 。
①c(Na+)>c(CH3COO-)>c(OH-)>c(H+) ②c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
③c(CH3COO-)=c(Na+)>c(H+)=c(OH-) ④c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好反应,则混合前两溶液的物质的量浓度大小关系为c(NaOH)
(3)若该溶液是由体积相等的氢氧化钠溶液和醋酸溶液混合而成,且恰好呈中性,则混合前两溶液的物质的量浓度大小关系为c(NaOH)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知难溶于水的盐在水中存在溶解平衡,例如氯化银在水中的溶解平衡为AgCl(s) Ag+(aq)+ Cl-(aq)在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp = c(Ag+)·c(Cl-)= 1.8 × 10-10,现把氯化银(足量)分别放入:①100mL蒸馏水中;②100mL 0.1mol·L-1的盐酸溶液中;③1000mL 0.1 mol·L-l的氯化铝溶液中;④100mL0.1 mol·L-1的氯化镁溶液中。
Ag+(aq)+ Cl-(aq)在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp = c(Ag+)·c(Cl-)= 1.8 × 10-10,现把氯化银(足量)分别放入:①100mL蒸馏水中;②100mL 0.1mol·L-1的盐酸溶液中;③1000mL 0.1 mol·L-l的氯化铝溶液中;④100mL0.1 mol·L-1的氯化镁溶液中。
(1)充分搅拌后相同温度下,银离子浓度由大到小顺序是_____________ (填序号)
(2)0.1mol·L-l氯化铝溶液中,银离子的物质的量浓度最大可达到______________ mol·L-1。
(3)向氯化银的饱和溶液中滴加硫化钾溶液,可观察到的现象是_______________ ,产生此现象涉及的离子方程式为___________________ 。
 Ag+(aq)+ Cl-(aq)在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp = c(Ag+)·c(Cl-)= 1.8 × 10-10,现把氯化银(足量)分别放入:①100mL蒸馏水中;②100mL 0.1mol·L-1的盐酸溶液中;③1000mL 0.1 mol·L-l的氯化铝溶液中;④100mL0.1 mol·L-1的氯化镁溶液中。
Ag+(aq)+ Cl-(aq)在一定温度下,水溶液中银离子(Ag+)和氯离子(Cl-)的物质的量浓度的乘积为一常数,可用Ksp表示:Ksp = c(Ag+)·c(Cl-)= 1.8 × 10-10,现把氯化银(足量)分别放入:①100mL蒸馏水中;②100mL 0.1mol·L-1的盐酸溶液中;③1000mL 0.1 mol·L-l的氯化铝溶液中;④100mL0.1 mol·L-1的氯化镁溶液中。(1)充分搅拌后相同温度下,银离子浓度由大到小顺序是
(2)0.1mol·L-l氯化铝溶液中,银离子的物质的量浓度最大可达到
(3)向氯化银的饱和溶液中滴加硫化钾溶液,可观察到的现象是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】高铁酸钾是绿色、环保型水处理剂。
(1)已知: 常温下,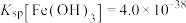 。高铁酸钾的净水能力与废水的pH 有关,当溶液 pH=2时, 废水中
。高铁酸钾的净水能力与废水的pH 有关,当溶液 pH=2时, 废水中
________ mol∙L−1。
(2)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:

pH=2.6时,溶液中主要含铁形体浓度的大小关系为___________ 。
(3)已知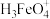 电离常数分别为:
电离常数分别为:  ,
,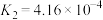 ,
,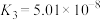 ,当 pH=4 时, 溶液中
,当 pH=4 时, 溶液中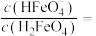
________ 。
(1)已知: 常温下,
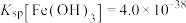 。高铁酸钾的净水能力与废水的pH 有关,当溶液 pH=2时, 废水中
。高铁酸钾的净水能力与废水的pH 有关,当溶液 pH=2时, 废水中
(2)高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:

pH=2.6时,溶液中主要含铁形体浓度的大小关系为
(3)已知
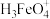 电离常数分别为:
电离常数分别为:  ,
,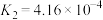 ,
,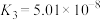 ,当 pH=4 时, 溶液中
,当 pH=4 时, 溶液中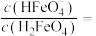
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】二水合磷酸二氢锰具有广泛用途,被用作防锈剂。某化工厂拟用软锰矿(含MnO2及少量FeO、Al2O3和SiO2)为原料生产Mn(H2PO4)2·2H2O,其工艺流程如下所示:
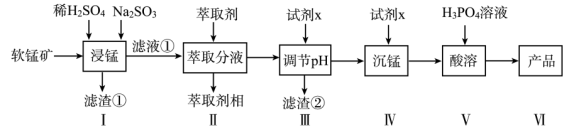
试回答下列问题:试剂x为某种钠的正盐,从环保、经济角度,x最好为___________ (写化学式);若c(Mn2+)=1.0 mol·L-1,调节pH范围应为___________ (该条件下,Ksp[Al(OH)3]=1.0×10-33,Ksp[Mn(OH)2]=1.0×10-14)。

试回答下列问题:试剂x为某种钠的正盐,从环保、经济角度,x最好为
您最近一年使用:0次



