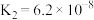常温下,将0.01 mol NH4Cl和 0.002 mol NaOH 溶于水配成1 L混合溶液,
(1)该溶液中存在的三个平衡体系是:______________________________ 、
_______________________________ 、_______________________________ 。
(2)溶液中共有_______ 种不同的粒子。
(3)这些粒子中浓度为0.01 mol/L 的是_________ ,浓度为0.002 mol/L 的是_________ 。
(4)物质的量之和为0.01 mol的两种粒子是:___________ 和______________ 。
(5)_______ 和_______ 两种离子数量之和比OH-多0.008mol。
(1)该溶液中存在的三个平衡体系是:
(2)溶液中共有
(3)这些粒子中浓度为0.01 mol/L 的是
(4)物质的量之和为0.01 mol的两种粒子是:
(5)
10-11高二上·重庆·期中 查看更多[1]
(已下线)2010年重庆市西南师大附中高二上学期期中考试化学试卷
更新时间:2010-12-08 15:50:46
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】计算下列各题在常温下的数值(lg2=0.3、lg3=0.477、lg5=0.7)。
(1)0.005mol/L的氢氧化钡溶液的PH=____ 。
(2)0.1mol/L的醋酸的PH=_____ (电离度=1%)。
(3)pH=12的NaOH溶液加水稀释到原来的10倍,则溶液的pH=_____ 。
(4)pH=12氨水加水稀释到原来100倍,溶液的pH值范围___________ 。
(5)PH=1和PH=3的硫酸等体积混合后溶液的PH=______ ,c(H+)水=_____ 。
(6)pH=13 的强碱与 pH=2 的强酸溶液混合,所得混合液的 pH=11,则强碱与强酸的体积比为___ 。
(1)0.005mol/L的氢氧化钡溶液的PH=
(2)0.1mol/L的醋酸的PH=
(3)pH=12的NaOH溶液加水稀释到原来的10倍,则溶液的pH=
(4)pH=12氨水加水稀释到原来100倍,溶液的pH值范围
(5)PH=1和PH=3的硫酸等体积混合后溶液的PH=
(6)pH=13 的强碱与 pH=2 的强酸溶液混合,所得混合液的 pH=11,则强碱与强酸的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】 时,四种酸的电离平衡常数如下:
时,四种酸的电离平衡常数如下:
回答下列问题:
(1) 时,
时,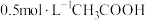 溶液的
溶液的 约为
约为__________ (已知 );向该
);向该 溶液中加入水稀释后,下列说法正确的是
溶液中加入水稀释后,下列说法正确的是__________ (填代号).
a.水的电离平衡正向移动 b.醋酸的电离程度增大, 也增大
也增大
c.溶液中导电粒子的数目减少 d.溶液中 不变
不变
(2) 时,将
时,将 通入氨水中,当
通入氨水中,当 降至
降至 时,溶液中的
时,溶液中的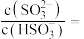
__________ .
(3)体积和 相同的①
相同的① ;②
;② ;③
;③ 三份酸溶液分别与同一浓度的
三份酸溶液分别与同一浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液体积由大到小的顺序是
溶液体积由大到小的顺序是__________ (填序号).
(4)向 溶液中通入少量
溶液中通入少量 时,发生反应的离子方程式为
时,发生反应的离子方程式为__________ .
 时,四种酸的电离平衡常数如下:
时,四种酸的电离平衡常数如下:化学式 |
|
|
|
|
电离常数 |
|
|
|
|
(1)
 时,
时,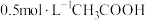 溶液的
溶液的 约为
约为 );向该
);向该 溶液中加入水稀释后,下列说法正确的是
溶液中加入水稀释后,下列说法正确的是a.水的电离平衡正向移动 b.醋酸的电离程度增大,
 也增大
也增大c.溶液中导电粒子的数目减少 d.溶液中
 不变
不变(2)
 时,将
时,将 通入氨水中,当
通入氨水中,当 降至
降至 时,溶液中的
时,溶液中的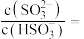
(3)体积和
 相同的①
相同的① ;②
;② ;③
;③ 三份酸溶液分别与同一浓度的
三份酸溶液分别与同一浓度的 溶液完全中和,消耗
溶液完全中和,消耗 溶液体积由大到小的顺序是
溶液体积由大到小的顺序是(4)向
 溶液中通入少量
溶液中通入少量 时,发生反应的离子方程式为
时,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)某温度(t ℃)时,水的Kw=1×10-12,则该温度____ (填“>”“<”或“=”)25 ℃,其理由是____ 。
(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈____ (填“酸性”“碱性”或“中性”);若该溶液中只存在NaOH溶质,则由H2O电离出来的c(OH-)=____ mol·L-1。
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡____ (填“向左”“向右”或“不”,下同)移动。在新制氯水中加入少量NaCl固体,水的电离平衡____ 移动。
(4)25 ℃时,0.1 mol·L-1下列物质的溶液,水电离出的c(H+)由大到小的关系是____ (填序号)。
①HCl ②H2SO4 ③CH3COOH(Ka=1.7×10-5) ④NH3·H2O(Kb=1.7×10-5) ⑤NaOH ⑥Ba(OH)2
(5)25 ℃时,pH=4的盐酸中水的电离程度____ pH=10的Ba(OH)2溶液中水的电离程度。
(6)下列曲线中,可以描述0.1 mol·L-1乙酸(甲,Ka=1.8×10-5)和0.1 mol·L-1氯乙酸(乙,Ka=1.4×10-3)的水溶液中,水电离出的c(H+)与加入水体积V的关系的是____ (填字母)。

(2)该温度下,c(H+)=1×10-7 mol·L-1的溶液呈
(3)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡
(4)25 ℃时,0.1 mol·L-1下列物质的溶液,水电离出的c(H+)由大到小的关系是
①HCl ②H2SO4 ③CH3COOH(Ka=1.7×10-5) ④NH3·H2O(Kb=1.7×10-5) ⑤NaOH ⑥Ba(OH)2
(5)25 ℃时,pH=4的盐酸中水的电离程度
(6)下列曲线中,可以描述0.1 mol·L-1乙酸(甲,Ka=1.8×10-5)和0.1 mol·L-1氯乙酸(乙,Ka=1.4×10-3)的水溶液中,水电离出的c(H+)与加入水体积V的关系的是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】已知某溶液中存在OH-、H+、NH4+、Cl-四种离子,某同学推测其离子浓度大小顺序有如下四种关系:
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是________ ,上述四种离子浓度的大小顺序为________ (选填序号)。
(2)若上述关系中③是正确的,则溶液中的溶质为________ ;若上述关系中④是正确的,则溶液中的溶质为________ 。
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________ c(NH3·H2O)(填“大于”“小于”或“等于”,下同),混合前酸中c (H+)和碱中c(OH-)的关系为c(H+)________ c(OH-)。
①c(Cl-)>c(NH4+)>c(H+)>c(OH-) ②c(Cl-)>c(NH4+)>c(OH-)>c(H+)
③c(NH4+)>c(Cl-)>c(OH-)>c(H+) ④c(Cl-)>c(H+)>c(NH4+)>c(OH-)
填写下列空白:
(1)若溶液中只溶解了一种溶质,则该溶质是
(2)若上述关系中③是正确的,则溶液中的溶质为
(3)若该溶液是由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题
(1)已知:25℃时NH3·H2O的Kb=1.0×10-5。
①求0.10mol·L-1的NH3·H2O溶液中c(OH-)=___________ mol·L-1。
②25℃时,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,若混合后所得溶液的pH=7,用含a的代数式表示的电离常数Kb=___________ 。
(2)25℃时,H2SO3 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=___________ ,若向NaHSO3溶液中加入少量的Cl2,则溶液中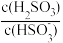 将
将___________ (填“增大”“减小”或“不变”)。
(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH___________ NaOH溶液的pH(填“>”“=”或“<”)。
(4)常温时,取0.1mol·L-1HX溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1mol·L-1NaOH溶液中由水电离出的c(OH-)之比为___________ 。
②已知NH4X溶液呈中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH___________ 7(填“>”“<”或“=”)。
(1)已知:25℃时NH3·H2O的Kb=1.0×10-5。
①求0.10mol·L-1的NH3·H2O溶液中c(OH-)=
②25℃时,将amol·L-1的氨水与0.01mol·L-1的盐酸等体积混合,若混合后所得溶液的pH=7,用含a的代数式表示的电离常数Kb=
(2)25℃时,H2SO3
 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=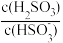 将
将(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH
(4)常温时,取0.1mol·L-1HX溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1mol·L-1NaOH溶液中由水电离出的c(OH-)之比为
②已知NH4X溶液呈中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】利用所学化学反应原理知识,解决以下问题:
(1)25℃时, 溶液呈碱性的原因是
溶液呈碱性的原因是___________ (用离子方程式表示);把 溶液蒸干并灼烧得到的产物是
溶液蒸干并灼烧得到的产物是___________ 。
(2)在日常生活中经常用 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:___________ 。
(3)相同物质的量浓度的五种溶液:① 、②氨水、③
、②氨水、③ 、④
、④ ⑤
⑤ ,
, 由大到小顺序是
由大到小顺序是___________ (用序号表示)。
(4)实验室中常用NaOH溶液来进行洗气和提纯,当用150mL 1mol/L的NaOH溶液吸收标准状况下2.24L 时,所得溶液中各离子浓度由大到小的顺序为
时,所得溶液中各离子浓度由大到小的顺序为___________ 。
(5)某酸 在水中的电离方程式是:
在水中的电离方程式是: ,
, ,回答下列问题:
,回答下列问题:
①在 的
的 溶液中,下列微粒浓度关系式正确的是
溶液中,下列微粒浓度关系式正确的是___________ 。
A.
B.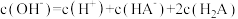
C.
D.
②常温下,已知 NaHA溶液的
NaHA溶液的 ,则
,则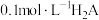 溶液中
溶液中 可能
可能___________ (填“>”、“<”或“=”) 。
。
(1)25℃时,
 溶液呈碱性的原因是
溶液呈碱性的原因是 溶液蒸干并灼烧得到的产物是
溶液蒸干并灼烧得到的产物是(2)在日常生活中经常用
 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:(3)相同物质的量浓度的五种溶液:①
 、②氨水、③
、②氨水、③ 、④
、④ ⑤
⑤ ,
, 由大到小顺序是
由大到小顺序是(4)实验室中常用NaOH溶液来进行洗气和提纯,当用150mL 1mol/L的NaOH溶液吸收标准状况下2.24L
 时,所得溶液中各离子浓度由大到小的顺序为
时,所得溶液中各离子浓度由大到小的顺序为(5)某酸
 在水中的电离方程式是:
在水中的电离方程式是: ,
, ,回答下列问题:
,回答下列问题:①在
 的
的 溶液中,下列微粒浓度关系式正确的是
溶液中,下列微粒浓度关系式正确的是A.

B.
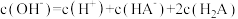
C.

D.

②常温下,已知
 NaHA溶液的
NaHA溶液的 ,则
,则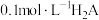 溶液中
溶液中 可能
可能 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】草酸即乙二酸,是一种有机二元酸,在工业上有重要的应用。草酸在100℃时开始升华,157℃时大量升华,并开始分解。常温下,相关数据如表所示:
(1)常温下,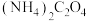 ,溶液的pH
,溶液的pH__________ 7(填“>”“<”或“=”)。
(2)用惰性电极电解饱和草酸溶液可制得乙醛酸( ),阴极的电极反应式为
),阴极的电极反应式为_______ 。
(3)草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸 草酸钠晶体
草酸钠晶体
①75%酒精的作用是____________________________________ 。
②将草酸与碳酸钠按物质的量之比为2∶1充分溶解在足量的水中,所得溶液的 。请将所得溶液中离子浓度按由大到小的顺序排列:
。请将所得溶液中离子浓度按由大到小的顺序排列:____________________________________________ 。
(4)已知某温度下 的
的 为
为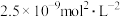 。将
。将 的
的 溶液和
溶液和 的
的 溶液等体积混合后,所得溶液中
溶液等体积混合后,所得溶液中 的物质的量浓度为
的物质的量浓度为__________ 。
| 电离方程式 | 电离常数 |
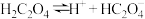 |  |
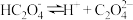 | 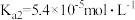 |
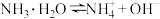 | 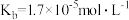 |
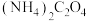 ,溶液的pH
,溶液的pH(2)用惰性电极电解饱和草酸溶液可制得乙醛酸(
 ),阴极的电极反应式为
),阴极的电极反应式为(3)草酸钠是一种重要的还原剂。合成草酸钠的操作如下:草酸
 草酸钠晶体
草酸钠晶体①75%酒精的作用是
②将草酸与碳酸钠按物质的量之比为2∶1充分溶解在足量的水中,所得溶液的
 。请将所得溶液中离子浓度按由大到小的顺序排列:
。请将所得溶液中离子浓度按由大到小的顺序排列:(4)已知某温度下
 的
的 为
为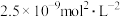 。将
。将 的
的 溶液和
溶液和 的
的 溶液等体积混合后,所得溶液中
溶液等体积混合后,所得溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)25℃时,将pH=12的NaOH溶液aL与pH=l的HCl溶液bL混合,若所得混合液为中性,则a:b=____ 。
(2)25℃时,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液pH>7,则溶液中c(Na+)____ c(CH3COO-)(填“>”、“<”或“=”)。
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液显____ 性(填“酸”、“中”或“碱”)。
(4)已知T℃时:CH3COOH CH3COO-+H+Ka=m
CH3COO-+H+Ka=m
H2O=H++OH-Kw=n
则: =
=____ 。
(5)电离常数(25℃):CH3COOH:Ka=1.8 10-5H2SO3:Ka1=1.3
10-5H2SO3:Ka1=1.3 10-2、Ka2=6.0
10-2、Ka2=6.0 10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:____ 。
(1)25℃时,将pH=12的NaOH溶液aL与pH=l的HCl溶液bL混合,若所得混合液为中性,则a:b=
(2)25℃时,将等体积等物质的量浓度的醋酸和氢氧化钠溶液混合,溶液pH>7,则溶液中c(Na+)
(3)25℃时,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液显
(4)已知T℃时:CH3COOH
 CH3COO-+H+Ka=m
CH3COO-+H+Ka=mH2O=H++OH-Kw=n
则:
 =
=(5)电离常数(25℃):CH3COOH:Ka=1.8
 10-5H2SO3:Ka1=1.3
10-5H2SO3:Ka1=1.3 10-2、Ka2=6.0
10-2、Ka2=6.0 10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
10-8。请写出在CH3COONa溶液中通入少量SO2的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
现将0.04mol∙L-1HA溶液和0.02mol∙L-1NaOH溶液等体积混合,得到缓冲溶液。
a.若HA为HCN,该溶液显碱性,则溶液中c(Na+)_______ c(CN-) (填“<”、“=”或“>”)。
b.若HA为CH3COOH,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是_______ 。
(2)常温下,向100mL0.01mol∙L-1HCl溶液中逐滴加入0.02mol∙L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
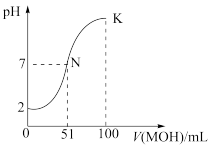
①常温下一定浓度的MCl稀溶液的pH_______ (填“>”“<”或“=”)7,用离子方程式表示其原因_______ 。
②K点对应的溶液中,c(M+)+c(MOH)_______ (填“>”“<”或“=”) 2c(Cl-)。
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
现将0.04mol∙L-1HA溶液和0.02mol∙L-1NaOH溶液等体积混合,得到缓冲溶液。
a.若HA为HCN,该溶液显碱性,则溶液中c(Na+)
b.若HA为CH3COOH,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
(2)常温下,向100mL0.01mol∙L-1HCl溶液中逐滴加入0.02mol∙L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

①常温下一定浓度的MCl稀溶液的pH
②K点对应的溶液中,c(M+)+c(MOH)
您最近一年使用:0次






 ,
,
 ,
,