计算下列各题在常温下的数值(lg2=0.3、lg3=0.477、lg5=0.7)。
(1)0.005mol/L的氢氧化钡溶液的PH=____ 。
(2)0.1mol/L的醋酸的PH=_____ (电离度=1%)。
(3)pH=12的NaOH溶液加水稀释到原来的10倍,则溶液的pH=_____ 。
(4)pH=12氨水加水稀释到原来100倍,溶液的pH值范围___________ 。
(5)PH=1和PH=3的硫酸等体积混合后溶液的PH=______ ,c(H+)水=_____ 。
(6)pH=13 的强碱与 pH=2 的强酸溶液混合,所得混合液的 pH=11,则强碱与强酸的体积比为___ 。
(1)0.005mol/L的氢氧化钡溶液的PH=
(2)0.1mol/L的醋酸的PH=
(3)pH=12的NaOH溶液加水稀释到原来的10倍,则溶液的pH=
(4)pH=12氨水加水稀释到原来100倍,溶液的pH值范围
(5)PH=1和PH=3的硫酸等体积混合后溶液的PH=
(6)pH=13 的强碱与 pH=2 的强酸溶液混合,所得混合液的 pH=11,则强碱与强酸的体积比为
更新时间:2019-11-11 23:18:17
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】将pH=4的盐酸与pH=10的氨水等体积混合
(1)混合后溶液中的溶质是___________ ,呈___________ 性。
(2)溶液中离子浓度由大到小的顺序是___________ 。
(1)混合后溶液中的溶质是
(2)溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空:
(1)25℃,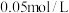 硫酸溶液中,酸电离出的
硫酸溶液中,酸电离出的 约为水电离出的
约为水电离出的 的
的______ 倍。
(2)25℃时,将 的稀硫酸
的稀硫酸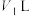 与
与 的苛性钠溶液
的苛性钠溶液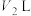 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则
___________ 。
(3)常温下,向 的乙酸溶液中加入少量蒸馏水稀释,则溶液中
的乙酸溶液中加入少量蒸馏水稀释,则溶液中 的数目将
的数目将________ , 将
将_________ (填“变大”、“变小”或“不变”)。
(4)室温时,碳酸的电离常数为 、
、 ,则当某溶液
,则当某溶液 时,
时,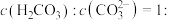
___________ ;已知次氯酸的电离平衡常数 和碳酸的电离平衡常数关系为
和碳酸的电离平衡常数关系为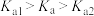 ,请写出向
,请写出向 溶液中通入少量
溶液中通入少量 的离子反应方程式
的离子反应方程式___________ 。
(5) 俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式
俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式___________ 。
(1)25℃,
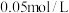 硫酸溶液中,酸电离出的
硫酸溶液中,酸电离出的 约为水电离出的
约为水电离出的 的
的(2)25℃时,将
 的稀硫酸
的稀硫酸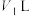 与
与 的苛性钠溶液
的苛性钠溶液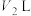 混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的
混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的 ,则
,则
(3)常温下,向
 的乙酸溶液中加入少量蒸馏水稀释,则溶液中
的乙酸溶液中加入少量蒸馏水稀释,则溶液中 的数目将
的数目将 将
将(4)室温时,碳酸的电离常数为
 、
、 ,则当某溶液
,则当某溶液 时,
时,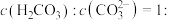
 和碳酸的电离平衡常数关系为
和碳酸的电离平衡常数关系为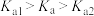 ,请写出向
,请写出向 溶液中通入少量
溶液中通入少量 的离子反应方程式
的离子反应方程式(5)
 俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式
俗称大苏打,在与稀硫酸溶液混合时会产生沉淀及易溶于水的气体,该反应可用来探究化学反应速率的影响因素,请写出该化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有室温下溶质浓度均为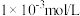 的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
的几种溶液:①盐酸、②硫酸、③醋酸、④硫酸铵、⑤氨水、⑥氢氧化钠溶液,回答下列问题:
(1)在④溶液中,各离子浓度大小顺序为:
(2)将③、⑥混合后,若溶液呈现中性,则消耗两溶液的体积为③
(3)在常温下,将100mL的②与100mL的⑥溶液混合后(假设混合后溶液的体积为混合前溶液的体积之和),溶液的pH=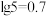 )
)
(4)在常温下,六种液体的pH由大到小的顺序是
(5)常温下将③溶液加水稀释过程中,下列表达式的数据一定变大的是
A、 B、
B、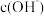 C、
C、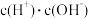 D、
D、
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求填写下面的空。
(1)温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4④NH4NO3⑤NaClO ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是________
A.③①④②⑥⑤ B.③①④②⑤⑥ C.③②①⑥④⑤ D.⑤⑥②④①③
(2)25℃时,利用pH试纸测得0.1mol•L-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为_______ ;向10mL此溶液中加水稀释。pH值将_____ (填“增大”、“减小”或“无法确定”)
(3)25 ℃时,pH=3的NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=______ (取近似值)
(4)pH=2的盐酸和CH3COOH溶液各1mL,分别加水至pH再次相等,则加入水的体积V(HCl)__________ V(CH3COOH)(填“>”、“<”或“=”,下同)
(5)浓度均为0.1mol/L的盐酸和CH3COOH溶液各1mL,加入等体积的水稀释后pH(HCl)_____ pH(CH3COOH)
(1)温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4④NH4NO3⑤NaClO ⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
A.③①④②⑥⑤ B.③①④②⑤⑥ C.③②①⑥④⑤ D.⑤⑥②④①③
(2)25℃时,利用pH试纸测得0.1mol•L-1醋酸溶液的pH约为3,则可以估算出醋酸的电离常数约为
(3)25 ℃时,pH=3的NH4Al(SO4)2中2c(SO42-)-c(NH4+)-3c(Al3+)=
(4)pH=2的盐酸和CH3COOH溶液各1mL,分别加水至pH再次相等,则加入水的体积V(HCl)
(5)浓度均为0.1mol/L的盐酸和CH3COOH溶液各1mL,加入等体积的水稀释后pH(HCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】运用相关原理,回答下列各小题:
(1)某 溶液的浓度是
溶液的浓度是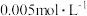 :
:
①此溶液的 为
为_______ ;
②用水稀释到原来体积的100倍, 为
为_______ ;
③再继续稀释 倍,
倍, 为
为_______ 。
(2)室温下、某水溶液中存在的离子有 、
、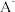 、
、 、
、 。根据题意,回答下列问题:
。根据题意,回答下列问题:
①若由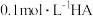 溶液与
溶液与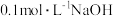 溶液等体积混合而得,则溶液的
溶液等体积混合而得,则溶液的
_______ 7(填大小关系)。
②若溶液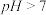 ,则
,则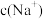
_______ 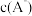 ,理由是
,理由是_______
③若溶液由 的HA溶液
的HA溶液 与
与 的
的 溶液
溶液 混合而得,则下列说法中正确的是
混合而得,则下列说法中正确的是_______ (填选项代号)。
A.若反应后溶液呈中性,则
B.若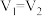 反应后溶液的
反应后溶液的 一定等于7
一定等于7
C.若反应后溶液呈酸性,则 一定大于
一定大于
D.若反应后溶液呈碱性,则 一定小于
一定小于
(1)某
 溶液的浓度是
溶液的浓度是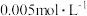 :
:①此溶液的
 为
为②用水稀释到原来体积的100倍,
 为
为③再继续稀释
 倍,
倍, 为
为(2)室温下、某水溶液中存在的离子有
 、
、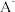 、
、 、
、 。根据题意,回答下列问题:
。根据题意,回答下列问题:①若由
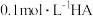 溶液与
溶液与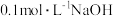 溶液等体积混合而得,则溶液的
溶液等体积混合而得,则溶液的
②若溶液
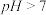 ,则
,则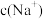
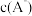 ,理由是
,理由是③若溶液由
 的HA溶液
的HA溶液 与
与 的
的 溶液
溶液 混合而得,则下列说法中正确的是
混合而得,则下列说法中正确的是A.若反应后溶液呈中性,则

B.若
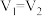 反应后溶液的
反应后溶液的 一定等于7
一定等于7C.若反应后溶液呈酸性,则
 一定大于
一定大于
D.若反应后溶液呈碱性,则
 一定小于
一定小于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列填空:
(一)常温下,计算下列溶液的pH,并将计算结果填在横线上:
(1)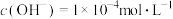 的溶液pH=
的溶液pH=___________ 。
(2)将pH=2的H2SO4溶液与pH=11的 溶液以体积比
溶液以体积比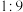 混合,充分反应后恢复至常温(溶液体积的变化忽略不计)时pH=
混合,充分反应后恢复至常温(溶液体积的变化忽略不计)时pH=___________ 。
(二)现有常温下五份溶液:
①0.01mol∙L-1CH3COOH溶液②0.01mol∙L-1盐酸③pH=12的氨水④pH=12的NaOH溶液
⑤0.01mol∙L-1盐酸与pH=12的NaOH溶液等体积混合后所得溶液
(3)其中水电离程度最大的是________ (填序号,下同),水的电离程度相同的是________ 。
(4)将五份溶液同等稀释10倍后,溶液的pH:①___________ ②,③___________ ⑤(填“>”、“=”或“<”)。
(一)常温下,计算下列溶液的pH,并将计算结果填在横线上:
(1)
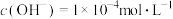 的溶液pH=
的溶液pH=(2)将pH=2的H2SO4溶液与pH=11的
 溶液以体积比
溶液以体积比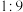 混合,充分反应后恢复至常温(溶液体积的变化忽略不计)时pH=
混合,充分反应后恢复至常温(溶液体积的变化忽略不计)时pH=(二)现有常温下五份溶液:
①0.01mol∙L-1CH3COOH溶液②0.01mol∙L-1盐酸③pH=12的氨水④pH=12的NaOH溶液
⑤0.01mol∙L-1盐酸与pH=12的NaOH溶液等体积混合后所得溶液
(3)其中水电离程度最大的是
(4)将五份溶液同等稀释10倍后,溶液的pH:①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】水的电离平衡曲线如图所示:
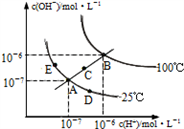
(1)在25℃时,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。如果加入蒸馏水,就加入_______ mL;如果加入pH = 10的NaOH溶液,应加入_______ mL(忽略溶液混合后体积的微小变化);
(2)当温度升高到B点时,水的离子积为________ ;加酸_______ (填能或不能)使水的离子积由E点变到B点;
(3)在100℃下,将pH=8的氢氧化钠溶液与pH=5的盐酸溶液混合并保持100℃,欲使溶液的pH=7,则氢氧化钠溶液与盐酸的体积比为_________ (忽略溶液混合后体积的微小变化)。

(1)在25℃时,有一pH = 12的NaOH溶液100 mL ,欲使它的pH降为11。如果加入蒸馏水,就加入
(2)当温度升高到B点时,水的离子积为
(3)在100℃下,将pH=8的氢氧化钠溶液与pH=5的盐酸溶液混合并保持100℃,欲使溶液的pH=7,则氢氧化钠溶液与盐酸的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】Ⅰ.已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH 溶液中存在电离平衡:CH3COOH ⇌ CH3COO-+H+ ΔH>0。
(1)常温下,在 pH = 5 的稀醋酸溶液中,c(CH3COO-)=_____ (不必化简)。下列方法中,可以使 0.10 mol·L-1 CH3COOH 的电离程度增大的是_____ 。
a.加入少量 0.10 mol·L-1 的稀盐酸 b.加热 CH3COOH 溶液
c.加水稀释至 0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量 0.10 mol·L-1 的 NaOH 溶液
(2)将等质量的锌投入等体积且 pH 均等于 3 的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)_____ V(醋酸),反应的最初速率为:υ(盐酸)_____ υ(醋酸)。(填写“>”、“<”或“=”)
(3)已知:90℃时,水的离子积常数为 Kw=3.8×10-13,在此温度下,将 pH=3 的盐酸和 pH=11 的氢氧化钠溶液等体积混合,则混合溶液中的 c(H+)=_____ mol/L(保留三位有效数字)。
Ⅱ.(1)常温下,已知 0.1 mol·L-1 一元酸HA 溶液中c(OH-)/c(H+)=1×10-8。常温下,0.1mol·L-1 HA溶液的 pH=_____ ;
(2)常温下,向 pH=a 的氨水中加入等体积盐酸时,溶液呈中性,则此盐酸的 pH_____ (14-a)(填写“>”、“<”或“=”)。
(1)常温下,在 pH = 5 的稀醋酸溶液中,c(CH3COO-)=
a.加入少量 0.10 mol·L-1 的稀盐酸 b.加热 CH3COOH 溶液
c.加水稀释至 0.010 mol·L-1 d.加入少量冰醋酸
e.加入少量氯化钠固体 f.加入少量 0.10 mol·L-1 的 NaOH 溶液
(2)将等质量的锌投入等体积且 pH 均等于 3 的醋酸和盐酸溶液中,经过充分反应后,发现只在一种溶液中有锌粉剩余,则生成氢气的体积:V(盐酸)
(3)已知:90℃时,水的离子积常数为 Kw=3.8×10-13,在此温度下,将 pH=3 的盐酸和 pH=11 的氢氧化钠溶液等体积混合,则混合溶液中的 c(H+)=
Ⅱ.(1)常温下,已知 0.1 mol·L-1 一元酸HA 溶液中c(OH-)/c(H+)=1×10-8。常温下,0.1mol·L-1 HA溶液的 pH=
(2)常温下,向 pH=a 的氨水中加入等体积盐酸时,溶液呈中性,则此盐酸的 pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
(1)将1L pH=3的HCl溶液分别与0.001mol·L-1 V1L NH3·H2O溶液、0.001mol·L-1 V2L NaOH溶液充分反应至中性,则V1、V2大小关系为V1_______ V2(填“>”“<”或“=”下同);pH相同的HCl溶液和CH3COOH溶液,加水稀释同等倍数后pH大小关系为:HCl_______ CH3COOH。
(2)浓度均为0.1mol·L-1NH4HSO4与NaOH溶液等体积混合,溶液呈酸性的原因:_______ (用离子方程式表示)
(3)用水稀释0.1 mol·L-1NH3·H2O时,溶液中随着水量的增加而减小的是_______ (填写序号)。
①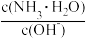 ②
② ③c(H+) ④ n(OH-) ⑤ c(H+)和c(OH-)的乘积
③c(H+) ④ n(OH-) ⑤ c(H+)和c(OH-)的乘积
(4)室温下,将pH=1的HCl溶液aL与pH=12的 NaOH溶液bL混合,所得混合液的pH=3,设混合溶液体积变化忽略不计,则a:b=_______ 。
(5)0.1 mol·L-1 NH4HSO4溶液中各种离子浓度由大到小的顺序是:_______ 。
(1)将1L pH=3的HCl溶液分别与0.001mol·L-1 V1L NH3·H2O溶液、0.001mol·L-1 V2L NaOH溶液充分反应至中性,则V1、V2大小关系为V1
(2)浓度均为0.1mol·L-1NH4HSO4与NaOH溶液等体积混合,溶液呈酸性的原因:
(3)用水稀释0.1 mol·L-1NH3·H2O时,溶液中随着水量的增加而减小的是
①
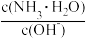 ②
② ③c(H+) ④ n(OH-) ⑤ c(H+)和c(OH-)的乘积
③c(H+) ④ n(OH-) ⑤ c(H+)和c(OH-)的乘积 (4)室温下,将pH=1的HCl溶液aL与pH=12的 NaOH溶液bL混合,所得混合液的pH=3,设混合溶液体积变化忽略不计,则a:b=
(5)0.1 mol·L-1 NH4HSO4溶液中各种离子浓度由大到小的顺序是:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】弱酸HA的电离常数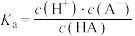 。25℃时,几种弱酸的电离常数如下:
。25℃时,几种弱酸的电离常数如下:
(1)根据上表数据填空:
①物质的量浓度相同的四种酸,其pH由大到小的顺序是___________ 。
②分别向等体积、相同pH的HCl溶液和CH3COOH溶液中加入足量的Zn粉,反应刚开始时产生H2的速率:v(HCl)___________ v(CH3COOH)(填“=”、“>”或“<”下同),反应完全后,所得氢气的质量:
___________  。
。
③将0.2mol/LHCN溶液与0.1mol/L Na2CO3溶液等体积混合,发生反应的离子方程式为_______ 。
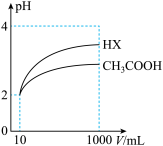
(2)体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中溶液pH变化如图所示。稀释后,HX溶液中水电离的c(H+)比醋酸溶液中水电离的c(H+)___________ ;电离常数
___________ 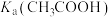 (填“>”、“=”或“<”),理由是
(填“>”、“=”或“<”),理由是_________ 。
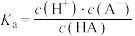 。25℃时,几种弱酸的电离常数如下:
。25℃时,几种弱酸的电离常数如下:| 弱酸化学式 |  |  | HCN |  |
| 电离常数 | 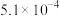 |  |  |   |
(1)根据上表数据填空:
①物质的量浓度相同的四种酸,其pH由大到小的顺序是
②分别向等体积、相同pH的HCl溶液和CH3COOH溶液中加入足量的Zn粉,反应刚开始时产生H2的速率:v(HCl)

 。
。③将0.2mol/LHCN溶液与0.1mol/L Na2CO3溶液等体积混合,发生反应的离子方程式为
(2)体积均为10mL、pH均为2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中溶液pH变化如图所示。稀释后,HX溶液中水电离的c(H+)比醋酸溶液中水电离的c(H+)

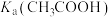 (填“>”、“=”或“<”),理由是
(填“>”、“=”或“<”),理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】已知:25℃时, 、HClO、
、HClO、 ,
, 的电离平衡常数如表所示,
的电离平衡常数如表所示, 。请回答下列问题。
。请回答下列问题。
(1)等浓度的四种酸溶液的酸性由强到弱的顺序是_________ 。
(2)写出HClO在水中的电离方程式:_________ 。
(3)将10 mL 0.1 mol⋅L
 溶液逐滴滴入50 mL 0.1 mol⋅L
溶液逐滴滴入50 mL 0.1 mol⋅L
 溶液中,现象为
溶液中,现象为_________ ,写出反应的离子方程式_________ 。
(4)若将少量的 气体通入NaClO溶液中,反应的离子方程式为
气体通入NaClO溶液中,反应的离子方程式为_________ 。
(5)25℃时,取50 mL 0.1 mol⋅L
 溶液,将其稀释100倍。
溶液,将其稀释100倍。
①稀释前 的电离度(
的电离度(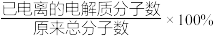 )约为
)约为_________ (保留三位有效数字)%。
②在稀释过程中,随着 浓度的降低,
浓度的降低, 逐渐
逐渐_________ (填“增大”、“减小”或“不变”)。
 、HClO、
、HClO、 ,
, 的电离平衡常数如表所示,
的电离平衡常数如表所示, 。请回答下列问题。
。请回答下列问题。| 物质 |  | HClO |  |  |
| 电离平衡常数 |  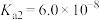 | 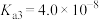 |   |  |
(2)写出HClO在水中的电离方程式:
(3)将10 mL 0.1 mol⋅L

 溶液逐滴滴入50 mL 0.1 mol⋅L
溶液逐滴滴入50 mL 0.1 mol⋅L
 溶液中,现象为
溶液中,现象为(4)若将少量的
 气体通入NaClO溶液中,反应的离子方程式为
气体通入NaClO溶液中,反应的离子方程式为(5)25℃时,取50 mL 0.1 mol⋅L

 溶液,将其稀释100倍。
溶液,将其稀释100倍。①稀释前
 的电离度(
的电离度(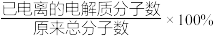 )约为
)约为②在稀释过程中,随着
 浓度的降低,
浓度的降低, 逐渐
逐渐
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)下列物质中,属于弱电解质的是(填序号,下同)______ ,属于非电解质是_____ 。
①硫酸氢钠固体 ②冰醋酸 ③蔗糖 ④氯化氢气体 ⑤硫酸钡 ⑥氨气 ⑦次氯酸钠
(2)写出下列物质在水中的电离方程式:醋酸:______ 。次氯酸钠:______ 。
(3)甲、乙两瓶氨水的浓度分别为1 mol•L-1、0.1 mol•L-1,则c(OH﹣)甲:c(OH﹣)乙________ 10(填“大于”、“等于”或“小于”)。
(4)现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol•L-1的NaOH溶液,乙为0.1 mol•L-1的HCl溶液,丙为0.1 mol•L-1的CH3COOH溶液,甲、乙、丙三种溶液中由水电离出的c(OH﹣)的大小关系为_____ 。
①硫酸氢钠固体 ②冰醋酸 ③蔗糖 ④氯化氢气体 ⑤硫酸钡 ⑥氨气 ⑦次氯酸钠
(2)写出下列物质在水中的电离方程式:醋酸:
(3)甲、乙两瓶氨水的浓度分别为1 mol•L-1、0.1 mol•L-1,则c(OH﹣)甲:c(OH﹣)乙
(4)现有常温条件下甲、乙、丙三种溶液,甲为0.1 mol•L-1的NaOH溶液,乙为0.1 mol•L-1的HCl溶液,丙为0.1 mol•L-1的CH3COOH溶液,甲、乙、丙三种溶液中由水电离出的c(OH﹣)的大小关系为
您最近一年使用:0次



