(1)25℃时,浓度为0.1 mol·L-1的6种溶液:①HCl,②CH3COOH ③Ba(OH)2④Na2CO3⑤KCl ⑥NH4Cl溶液pH由小到大的顺序为_______________ (填写编号)
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=_______ mol·L-1(保留到小数点后一位)。
(3)25℃时,pH=3 的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈________ (填“酸性”,“中性”或“碱性”),请写出溶液中离子浓度间的一个等式:________________________________ 。
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH= 7,则溶液中c (CH3COO-)+c(CH3COOH)=_____________ ,m与n的大小关系是m_____ n (填“>”“=”或“<”)。
(5)当300mL 1 mol·L-1的NaOH 溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为_________________________________________ 。
(2)25℃时,醋酸的电离常数Ka=1.7×10-5mol/L,则该温度下CH3COONa的水解平衡常数Kh=
(3)25℃时,pH=3 的醋酸和pH=11的氢氧化钠溶液等体积混合后,溶液呈
(4)25℃时,将m mol/L的醋酸和n mol/L的氢氧化钠溶液等体积混合后,溶液的pH= 7,则溶液中c (CH3COO-)+c(CH3COOH)=
(5)当300mL 1 mol·L-1的NaOH 溶液吸收标准状况下4.48LCO2时,所得溶液中各离子浓度由大到小的顺序为
更新时间:2017-12-28 10:18:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】盐酸、硫酸和醋酸是生产、生活和化学实验中常用的酸,请回答:
(1)人的胃液中含有盐酸,经测定某人胃液的pH=2,则其中的c(H+)=______ mol/L。
(2)食醋常用于食品调味,其主要成分为醋酸,已知醋酸酸性强于碳酸,写出碳酸钠溶液与足量醋酸反应的离子方程式:______ 。
(3)室温下,物质的量浓度相同、体积相同的盐酸(编号a)、硫酸(编号b)和醋酸(编号c),中和氢氧化钠的能力由大到小的顺序是______ 。(用相应编号表示);
(4)有pH均为3的盐酸、硫酸和醋酸,取同体积分别加蒸馏水稀释到pH=5,需水的体积依次为V1、V2、V3,则其关系是______ 。
(5)能证明醋酸是弱酸的实验事实是______ 。
a.室温时0.1mo/LCH3COONa溶液的pH大于7
b.可用食醋清除水壶内壁的水垢
c.与相同浓度的碳酸氢钠溶液反应,醋酸不如盐酸剧烈
d.将1mL pH=1的醋酸溶液稀释到100mL后,测其pH小于3
(6)向100mL0.1mo/L的盐酸中通入0.02mol氨气,充分吸收后测得溶液呈碱性。则该溶液中NH3·H2O、NH4+、Cl—三种微粒的物质的量浓度大小关系为______ 。
(1)人的胃液中含有盐酸,经测定某人胃液的pH=2,则其中的c(H+)=
(2)食醋常用于食品调味,其主要成分为醋酸,已知醋酸酸性强于碳酸,写出碳酸钠溶液与足量醋酸反应的离子方程式:
(3)室温下,物质的量浓度相同、体积相同的盐酸(编号a)、硫酸(编号b)和醋酸(编号c),中和氢氧化钠的能力由大到小的顺序是
(4)有pH均为3的盐酸、硫酸和醋酸,取同体积分别加蒸馏水稀释到pH=5,需水的体积依次为V1、V2、V3,则其关系是
(5)能证明醋酸是弱酸的实验事实是
a.室温时0.1mo/LCH3COONa溶液的pH大于7
b.可用食醋清除水壶内壁的水垢
c.与相同浓度的碳酸氢钠溶液反应,醋酸不如盐酸剧烈
d.将1mL pH=1的醋酸溶液稀释到100mL后,测其pH小于3
(6)向100mL0.1mo/L的盐酸中通入0.02mol氨气,充分吸收后测得溶液呈碱性。则该溶液中NH3·H2O、NH4+、Cl—三种微粒的物质的量浓度大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】硫的化合物应用广泛,研究其性质具有重要意义。回答下列问题:
(1)某小组测定
 ,溶液先升温后降温过程中的pH,数据如下表:
,溶液先升温后降温过程中的pH,数据如下表:
实验过程中,取 、
、 时刻的溶液,加入盐酸酸化的
时刻的溶液,加入盐酸酸化的 溶液做对比,
溶液做对比, 时刻产生的白色沉淀多。
时刻产生的白色沉淀多。
① 溶液呈碱性的原因是
溶液呈碱性的原因是_______ (用离子方程式表示)。
② 过程中,水的离子积常数
过程中,水的离子积常数
_______ (填“增大”、“减小”或“不确定”,下同); 水解程度
水解程度_______ 。
③与 相比,
相比, 溶液pH变小的原因是
溶液pH变小的原因是_______ 。
(2)室温时,向100mL
 溶液,溶液pH中滴加
溶液,溶液pH中滴加 NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。
NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。

①a点溶液pH_______ 1(填“>”、“<”或“=”)。
②b点到c点发生反应的离子方程式为_______ 。
③c点溶液中各离子浓度的大小关系是_______ 。
④d点和e点对应溶液中,水的电离程度d_______ e(填“>”、“<”或“=”)。
(1)某小组测定

 ,溶液先升温后降温过程中的pH,数据如下表:
,溶液先升温后降温过程中的pH,数据如下表:| 时刻 |  |  |  |  |
| 温度/℃ | 25 | 30 | 40 | 25 |
| pH | 9.66 | 9.52 | 9.37 | 9.25 |
 、
、 时刻的溶液,加入盐酸酸化的
时刻的溶液,加入盐酸酸化的 溶液做对比,
溶液做对比, 时刻产生的白色沉淀多。
时刻产生的白色沉淀多。①
 溶液呈碱性的原因是
溶液呈碱性的原因是②
 过程中,水的离子积常数
过程中,水的离子积常数
 水解程度
水解程度③与
 相比,
相比, 溶液pH变小的原因是
溶液pH变小的原因是(2)室温时,向100mL

 溶液,溶液pH中滴加
溶液,溶液pH中滴加 NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。
NaOH溶液,溶液pH与加入NaOH溶液体积的关系曲线如图所示。
①a点溶液pH
②b点到c点发生反应的离子方程式为
③c点溶液中各离子浓度的大小关系是
④d点和e点对应溶液中,水的电离程度d
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】NaOH溶液可用于多种气体的处理。
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO 水解而使其水溶液呈碱性,写出CO
水解而使其水溶液呈碱性,写出CO 第一步水解的离子方程式
第一步水解的离子方程式______ 。已知25℃时,CO 第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO
第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=20:1 时,溶液的pH=
)=20:1 时,溶液的pH=______ 。
②泡沫灭火器中通常装有NaHCO溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式______ 。
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmol•L﹣1CH3COONa溶液,则两份溶液中c(NO )、c(NO
)、c(NO )和c(CH3COO﹣)由大到小的顺序为
)和c(CH3COO﹣)由大到小的顺序为______ (已知HNO2的电离常数Ka=7.1×10﹣4mol•L﹣1,CH3COOH的电离常数Ka=1.7×10﹣5mol•L﹣1)。可使溶液A和溶液 B的 pH相等的方法是______ 。
A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收吸收SO2的过裎中,溶液中H2SO3、HSO 、SO
、SO 三者所占物质的量分数(a)随pH变化的关系如图所示:
三者所占物质的量分数(a)随pH变化的关系如图所示:
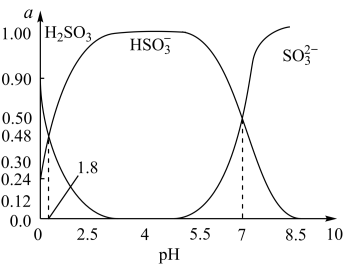
图中pH=7时,溶液中离子浓度关系正确的是______ 。
A.c(Na+)>2c(SO )>c(HSO
)>c(HSO )
)
B.c(Na+)=c(SO )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)
C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO )
)
D.c(Na+)>c(HSO )>c(SO
)>c(SO )>c(H+)=c(OH﹣)
)>c(H+)=c(OH﹣)
(1)CO2是温室气体,可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,因CO
 水解而使其水溶液呈碱性,写出CO
水解而使其水溶液呈碱性,写出CO 第一步水解的离子方程式
第一步水解的离子方程式 第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO
第一步水解的平衡常数Kh=2×10﹣4mol/L,当溶液中c(HCO ):c(CO
):c(CO )=20:1 时,溶液的pH=
)=20:1 时,溶液的pH=②泡沫灭火器中通常装有NaHCO溶液和Al2(SO4)3溶液,请写出这两种溶液混合时的离子反应方程式
(2)金属与浓硝酸反应产生的NO2可用NaOH溶液吸收,反应方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O。含0.2molNaOH的水溶液与0.2mol NO2恰好完全反应得1L溶液A,溶液B为0.lmol•L﹣1CH3COONa溶液,则两份溶液中c(NO
 )、c(NO
)、c(NO )和c(CH3COO﹣)由大到小的顺序为
)和c(CH3COO﹣)由大到小的顺序为A.向溶液A中加适量NaOH B.向溶液A中加适量水
C.向溶液B中加适量NaOH D.向溶液B中加适量水
(3)烟气中的SO2会引起酸雨,可利用氢氧化钠溶液吸收吸收SO2的过裎中,溶液中H2SO3、HSO
 、SO
、SO 三者所占物质的量分数(a)随pH变化的关系如图所示:
三者所占物质的量分数(a)随pH变化的关系如图所示:
图中pH=7时,溶液中离子浓度关系正确的是
A.c(Na+)>2c(SO
 )>c(HSO
)>c(HSO )
)B.c(Na+)=c(SO
 )+c(HSO
)+c(HSO )+c(H2SO3)
)+c(H2SO3)C.c(OH﹣)=c(H+)+c(H2SO3)+c(HSO
 )
)D.c(Na+)>c(HSO
 )>c(SO
)>c(SO )>c(H+)=c(OH﹣)
)>c(H+)=c(OH﹣)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常温下,浓度均为0.1mol·L-1的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液
(1)①中各离子浓度由大到小的顺序是___ 。
(2)④的水解平衡常数Kh=___ 。
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③___ ④(填“>”、“<"、“=”)
(4)向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:__ 。
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4×10-7;Ka2=5.6×10-11 | Ka=1.7×10-5 |
(1)①中各离子浓度由大到小的顺序是
(2)④的水解平衡常数Kh=
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
(4)向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知在常温下几种弱电解质的电离常数如下表:(已知pKi=-lgKi)
回答下列问题:
(1)在H3BO3(硼酸)、C6H5COOH(苯甲酸)、HN3(叠氮酸)三种物质中,酸性最弱的是___________ (填名称)。
(2)已知H3BO3在水中的电离方程式为H3BO3+H2O [B(OH)4]-+H+,则H3BO3是___________(填字母)。
[B(OH)4]-+H+,则H3BO3是___________(填字母)。
(3)(CH3)2NH·H2O在水中的电离类似一水合氨,写出(CH3)2NH·H2O的电离方程式:___________ 。
(4)NaN3溶液中离子浓度由大到小的顺序为___________ 。
(5)等物质的量浓度、等体积的C6H5COOH溶液和(CH3)2NH·H2O溶液反应,所得的混合溶液显___________ 性。
(6)常温下,C6H5COOK溶液的水解常数的数量级为___________ 。
| 化学式 | H3BO3 | C6H5COOH | HN3(叠氮酸) | (CH3)2NH·H2O |
| pKi | 9.14 | 4.19 | 4.7 | 3.7 |
回答下列问题:
(1)在H3BO3(硼酸)、C6H5COOH(苯甲酸)、HN3(叠氮酸)三种物质中,酸性最弱的是
(2)已知H3BO3在水中的电离方程式为H3BO3+H2O
 [B(OH)4]-+H+,则H3BO3是___________(填字母)。
[B(OH)4]-+H+,则H3BO3是___________(填字母)。| A.一元酸 | B.弱酸 | C.三元酸 | D.含氧酸 |
(4)NaN3溶液中离子浓度由大到小的顺序为
(5)等物质的量浓度、等体积的C6H5COOH溶液和(CH3)2NH·H2O溶液反应,所得的混合溶液显
(6)常温下,C6H5COOK溶液的水解常数的数量级为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】(1)已知:常温下浓度为0.1mol/L的下列溶液的pH如表
①等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:Cl-_________ ClO-,浓度相等的NaClO和CH3COOK溶液中:[c(Na+)-c(ClO-)]__________ [c(K+)-c(CH3COO-)](填“>”“<”或“=”)
②HCO3-的水解常数为__________ (填写具体数值),在相同温度下,同浓度的CH3COOH、H2CO3、HClO三种酸溶液的导电能力大小为__________
(2)常温下,向pH=a的醋酸中加入等体积NaOH时后呈中性,则此NaOH的pH_____ 14-a(>、<、=)
(3)常温下,已知0.1mol﹒L-1一元酸HA溶液中 =1×10-6。
=1×10-6。
①常温下,0.1mol﹒L-1HA溶液的pH=_____ ;
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是:_____ 。
(4)常温下,amol/L氨水与等体积0.1mol/LH2SO4溶液混合后溶液显中性,则NH3·H2O的电离平衡常数Kb=_____
| 溶质 | NaCl | CH3COOK | Na2CO3 | NaClO | NaHCO3 |
| pH | 7 | 8.1 | 11.6 | 9.7 | 8.3 |
①等体积等物质的量浓度的NaCl溶液与NaClO溶液中Cl-和ClO-离子个数:Cl-
②HCO3-的水解常数为
(2)常温下,向pH=a的醋酸中加入等体积NaOH时后呈中性,则此NaOH的pH
(3)常温下,已知0.1mol﹒L-1一元酸HA溶液中
 =1×10-6。
=1×10-6。①常温下,0.1mol﹒L-1HA溶液的pH=
②pH=3的HA与pH=11的NaOH溶液等体积混合后,溶液中4种离子物质的量浓度大小关系是:
(4)常温下,amol/L氨水与等体积0.1mol/LH2SO4溶液混合后溶液显中性,则NH3·H2O的电离平衡常数Kb=
您最近一年使用:0次



