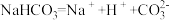名校
解题方法
1 . 下列事实中能说明HClO一定为弱电解质的是
| A.NaClO能与H2SO3反应 |
| B.用HClO溶液做导电实验时灯泡很暗 |
| C.常温下NaClO溶液的pH>7 |
| D.10mL1mol/LHClO溶液恰好与10mL1mol/L的NaOH溶液完全反应 |
您最近一年使用:0次
2023-01-13更新
|
54次组卷
|
4卷引用:第三章 本章复习提升3
21-22高二上·山东青岛·期末
名校
解题方法
2 . 肼(N2H4)又称联氨,为二元弱碱,在水中的电离与氨类似。已知常温下,N2H4第一步电离平衡
 。下列说法错误的是
。下列说法错误的是

 。下列说法错误的是
。下列说法错误的是A.N2H4的水溶液中存在: |
B.反应 的平衡常数 的平衡常数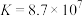 |
| C.联氨与硫酸形成酸式盐的化学式为N2H6(HSO4)2 |
D.向N2H4的水溶液中加水, 减小 减小 |
您最近一年使用:0次
2023-01-07更新
|
394次组卷
|
4卷引用:3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
(已下线)3.1.2 电离平衡常数-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)山东省青岛市黄岛区2021-2022学年高二上学期期末考试化学试题山东省青岛市4区县2021-2022学年高二上学期期末考试化学试题山东省菏泽市郓城第一中学2022-2023学年高二上学期期末考试化学试题
20-21高二上·广东江门·期中
名校
解题方法
3 . 在0.1 mol·L-1的CH3COOH溶液中存在如下电离平衡:CH3COOH CH3COO-+H+。对于该平衡,下列叙述正确的是
CH3COO-+H+。对于该平衡,下列叙述正确的是
 CH3COO-+H+。对于该平衡,下列叙述正确的是
CH3COO-+H+。对于该平衡,下列叙述正确的是| A.加入少量NaOH固体,平衡向正反应方向移动 |
| B.加水,平衡向逆反应方向移动 |
| C.滴加少量0.1 mol·L-1HCl溶液,溶液中c(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
您最近一年使用:0次
2022-12-19更新
|
742次组卷
|
24卷引用:3.1 电离平衡-同步学习必备知识
(已下线)3.1 电离平衡-同步学习必备知识黑龙江省哈尔滨市第一六二中学2021-2022学年高二上学期期末考试化学试题湖南省常德市石门县第一中学2021-2022学年高一下学期期中考试化学试题(已下线)第30练 电离平衡-2023年高考化学一轮复习小题多维练(全国通用)浙江省东阳中学2021-2022学年高二下学期期末考试化学试题新疆乌鲁木齐市第三十一中学2021-2022学年高二上学期期末考试化学试题 黑龙江省哈尔滨市第一六二中学校2022-2023学年高二上学期第一次月考化学试题(已下线)3.2.1 弱电解质的电离平衡-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)广东省兴宁市下堡中学2021-2022学年高二上学期期末质量检测化学试题广东省台山市华侨中学2020-2021学年高二上学期期中考试化学试题新疆维吾尔自治区呼图壁县第一中学2020-2021学年高二上学期期末考试化学试题四川省广安市武胜烈面中学校2020-2021学年高二下学期开学考试化学试题内蒙古集宁新世纪中学2020-2021学年高二下学期质量检测月考化学试题河北省张家口市第一中学2020-2021学年高二上学期10月月考(普实班) 化学试题(已下线)专题3.3.2 影响盐类水解的主要因素(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)浙江省温州新力量联盟2021-2022学年高二上学期期中联考化学试题黑龙江省大兴安岭实验中学(西校区)2021-2022学年高二上学期期中考试化学试题安徽省砀山县第四中学2021-2022学年高二学期12月月考化学试题山东省威海市文登新一中2021-2022学年高二上学期第一次阶段检测化学试题广东省潮州湘桥区南春中学2021-2022学年高二上学期期中考试化学试题(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)青海省海南藏族自治州高级中学2022-2023学年高二下学期期末考试化学试题黑龙江省海伦市第一中学2022-2023学年高三上学期1月期末考试化学试题内蒙古呼伦贝尔市满洲里远方中学2023-2024学年高二上学期期末考试化学试题
22-23高二上·全国·课时练习
解题方法
4 . A、B、C、D、E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
②浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是________ ,E是________ ;
(2)用水稀释0.1 mol·L-1B溶液时,溶液中随着水量的增加而减小的是________ (填写序号)。
a. b.
b. c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)
(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是________ (填写序号)。
a.反应所需要的时间E>A
b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E
d.E溶液里有镁粉剩余
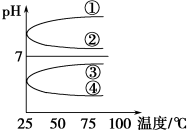
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中___ 曲线(填写序号)。
(5)室温下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为____________________ 。
①B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
②浓度均为0.1mol·L-1C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是
(2)用水稀释0.1 mol·L-1B溶液时,溶液中随着水量的增加而减小的是
a.
 b.
b. c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是
a.反应所需要的时间E>A
b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E
d.E溶液里有镁粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中

(5)室温下,向0.01mol·L-1 C溶液中滴加0.01mol·L-1 D溶液至中性,得到的溶液中所有离子的物质的量浓度由大到小的顺序为
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
5 . CO2可转化成有机物实现碳循环:CO2 CH3OH
CH3OH HCOOH……
HCOOH……
(1)用离子方程式表示HCOONa溶液呈碱性的原因___________ 。
(2)常温下,将0.2mol·L-1的HCOOH和0.1mol·L-1的NaOH溶液等体积混合,所得溶液的pH<7,说明HCOOH的电离程度___________ HCOONa的水解程度(填“大于”或“小于”)。该混合溶液中离子浓度由大到小的顺序是___________ 。
 CH3OH
CH3OH HCOOH……
HCOOH……(1)用离子方程式表示HCOONa溶液呈碱性的原因
(2)常温下,将0.2mol·L-1的HCOOH和0.1mol·L-1的NaOH溶液等体积混合,所得溶液的pH<7,说明HCOOH的电离程度
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
6 . HA与醋酸酸性相似,下列叙述错误的是
| A.HA水溶液中微粒浓度大小顺序:c(HA)>c(H+)>c(A-)>c(OH-) |
| B.HA与NH3作用生成的化合物是共价化合物 |
C.NaA水溶液中: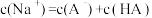 |
| D.稀释0.1mol·L-1 HA水溶液,其电离程度增大,pH也增大 |
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
7 . 向蒸馏水中滴入少量盐酸后,下列说法中错误的是
| A.c(H+)·c(OH-)不变 | B.pH增大了 |
| C.c(OH-)降低了 | D.水电离出的c(H+)减小了 |
您最近一年使用:0次
22-23高二上·全国·课时练习
解题方法
8 . 纯水在10 ℃和50 ℃时的氢离子浓度,前后两个量的大小关系为
| A.大于 | B.等于 | C.小于 | D.不能确定 |
您最近一年使用:0次
22-23高二上·全国·课时练习
9 . 有关电离平衡的理解不正确的是
| A.电解质在溶液中达到电离平衡时,分子浓度和离子的浓度相等 |
| B.电离平衡状态下溶液中各微粒的物质的量浓度和质量分数均保持不变 |
| C.电离平衡是动态平衡,弱电解质分子电离成离子和其离子结合成分子的过程均在进行 |
| D.改变条件时,电离平衡会发生移动,在新的条件下建立新的平衡 |
您最近一年使用:0次