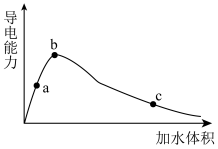
1 . 25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示。则下列说法不正确的是
A.醋酸的电离程度: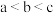 |
B.溶液中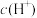 : : |
C.溶液中 : : |
D.从b点到c点,溶液中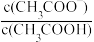 的比值增大 的比值增大 |
您最近半年使用:0次
2 . 在


 的
的 溶液中欲使
溶液中欲使 的电离度增大且
的电离度增大且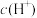 降低,可采用的方法是
降低,可采用的方法是
①加少量 的
的 溶液②加少量
溶液②加少量 的盐酸③加100
的盐酸③加100 水④加热
水④加热



 的
的 溶液中欲使
溶液中欲使 的电离度增大且
的电离度增大且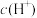 降低,可采用的方法是
降低,可采用的方法是①加少量
 的
的 溶液②加少量
溶液②加少量 的盐酸③加100
的盐酸③加100 水④加热
水④加热| A.①② | B.①③ | C.③④ | D.①④ |
您最近半年使用:0次
3 . 常温下,一种解释乙酰水杨酸(用HA表示, )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
 )药物在人体吸收模式如下:
)药物在人体吸收模式如下:
A.血浆中 大于胃中 大于胃中 | B.取胃中液体,加水稀释100倍后,pH=3.0 |
C.在血浆中,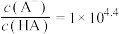 | D.在血浆和胃中,HA电离程度相同 |
您最近半年使用:0次
4 . 室温下,向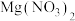 溶液、
溶液、 溶液、
溶液、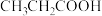 溶液中分别滴加
溶液中分别滴加 溶液,测得溶液
溶液,测得溶液 [
[ ,X代表
,X代表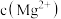 、
、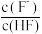 、
、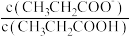 ]随溶液
]随溶液 的变化曲线如图所示。
的变化曲线如图所示。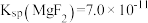 ,
, 的酸性比
的酸性比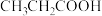 强。下列叙述正确的是
强。下列叙述正确的是
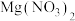 溶液、
溶液、 溶液、
溶液、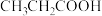 溶液中分别滴加
溶液中分别滴加 溶液,测得溶液
溶液,测得溶液 [
[ ,X代表
,X代表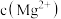 、
、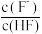 、
、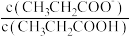 ]随溶液
]随溶液 的变化曲线如图所示。
的变化曲线如图所示。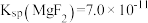 ,
, 的酸性比
的酸性比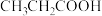 强。下列叙述正确的是
强。下列叙述正确的是
A. 代表 代表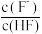 , ,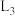 代表 代表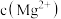 |
B.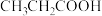 的 的 数量级为 数量级为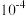 |
C.相同浓度的 、 、 混合溶液的 混合溶液的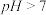 |
D.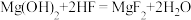 的 的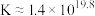 |
您最近半年使用:0次
5 . 常温下,向某浓度 溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与
溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与 、
、 、
、 变化如图所示。下列说法错误的是
变化如图所示。下列说法错误的是
 溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与
溶液中缓慢加入NaOH(s),保持溶液体积和温度不变,测得pH与 、
、 、
、 变化如图所示。下列说法错误的是
变化如图所示。下列说法错误的是
| A.a到b的滴定过程中水的电离程度逐渐增大 |
B.常温下, 电离平衡常数 电离平衡常数 为 为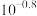 |
C.a点溶液中,存在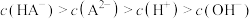 |
D.在NaHA溶液中,存在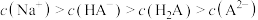 |
您最近半年使用:0次
6 . 完成下列问题。
(1)已知在25 ℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示。
①亚硫酸发生电离的方程式为______ 。
②碳酸和亚硫酸的第一步电离程度大于第二步电离程度的原因:______ 。
③在相同条件下,试比较H2CO3、 和
和 的酸性强弱:
的酸性强弱:____ >____ >____ 。
(2)在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,请回答:____ 。
②a、b、c三点溶液的pH由大到小的顺序为____ ,电离程度最大的是____ 。
③若使c点溶液中c(CH3COO-)增大,在如下措施中可选择____ (填字母)。
A.加热 B.加很稀的NaOH溶液 C.加固体KOH
D.加水 E.加CH3COONa(s) F.加锌粉
(3)向氨水中加入醋酸溶液,其导电能力(I)与加入醋酸溶液的体积(V)关系正确的是______。
(1)已知在25 ℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示。
| 酸 | 电离平衡常数 |
| 醋酸 | Ka=1.75×10-5 |
| 碳酸 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
| 亚硫酸 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
②碳酸和亚硫酸的第一步电离程度大于第二步电离程度的原因:
③在相同条件下,试比较H2CO3、
 和
和 的酸性强弱:
的酸性强弱:(2)在一定温度下,冰醋酸加水稀释的过程中,溶液的导电能力变化如图所示,请回答:
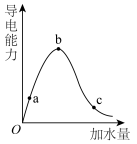
②a、b、c三点溶液的pH由大到小的顺序为
③若使c点溶液中c(CH3COO-)增大,在如下措施中可选择
A.加热 B.加很稀的NaOH溶液 C.加固体KOH
D.加水 E.加CH3COONa(s) F.加锌粉
(3)向氨水中加入醋酸溶液,其导电能力(I)与加入醋酸溶液的体积(V)关系正确的是______。
A.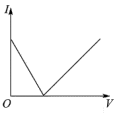 | B.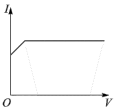 | C.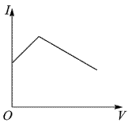 | D.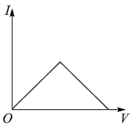 |
您最近半年使用:0次
解题方法
7 . 常温下,下列各组溶液的c(H+)一定等于1×10-7 mol/L的是
| A.pH=2和pH=12的两种溶液以等体积混合 |
| B.0.10 mol/L H2SO4溶液与0.10 mol/L NaOH溶液等体积混合 |
| C.将pH=5的CH3COOH溶液稀释100倍 |
| D.pH=1的H2SO4与c(OH-)=0.10 mol/L的Ba(OH)2溶液等体积混合 |
您最近半年使用:0次
解题方法
8 . 已知: 。精细化学品W是酸性条件下X与HCN反应的主产物,Y、Z是反应过程中的过渡态或中间体,X→W的反应过程可表示如下:
。精细化学品W是酸性条件下X与HCN反应的主产物,Y、Z是反应过程中的过渡态或中间体,X→W的反应过程可表示如下:
 。精细化学品W是酸性条件下X与HCN反应的主产物,Y、Z是反应过程中的过渡态或中间体,X→W的反应过程可表示如下:
。精细化学品W是酸性条件下X与HCN反应的主产物,Y、Z是反应过程中的过渡态或中间体,X→W的反应过程可表示如下:
| A.X的名称为2,3-环氧丙酮 | B.Z中碳原子的杂化方式为: |
| C.W存在对映异构体 | D.溶液的酸性越强,W的产率越高 |
您最近半年使用:0次
9 . 在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是___________ 。
(3)若三者PH相同时,物质的量浓度由大到小的顺序是___________ 。
(4)将PH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是___________ 。
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
(3)若三者PH相同时,物质的量浓度由大到小的顺序是
(4)将PH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是
您最近半年使用:0次
10 . 回答下列问题。
(1)溶液酸化时,K2MnO4转变为MnO2固体和KMnO4的离子方程式是___________ 。
(2)常温下,某种饮品pH=4,其中c(OH-)=___________ 。
(3)将0.025 mol·L-1的H2SO4溶液和0.075 mol·L-1的H2SO4溶液等体积混合,混合溶液的pH=___________ 。
(4)常温下,pH=13的氢氧化钡溶液,c[Ba(OH)2]=___________ 。
(5)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
纯碱溶液吸收少量H2S的离子方程式为___________ 。
(1)溶液酸化时,K2MnO4转变为MnO2固体和KMnO4的离子方程式是
(2)常温下,某种饮品pH=4,其中c(OH-)=
(3)将0.025 mol·L-1的H2SO4溶液和0.075 mol·L-1的H2SO4溶液等体积混合,混合溶液的pH=
(4)常温下,pH=13的氢氧化钡溶液,c[Ba(OH)2]=
(5)当H2S浓度较低时常用纯碱溶液进行吸收。表为H2S、H2CO3 的电离平衡常数。
| 电离平衡常数 | Kal | Ka2 |
| H2S | 9.1×10-8 | 1.1×10-12 |
| H2CO3 | 4.3×10-7 | 5.61×10-11 |
您最近半年使用:0次



