名校
解题方法
1 .  不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方法再利用。其中甲烷干重整反应可以将两类重要的温室气体
不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方法再利用。其中甲烷干重整反应可以将两类重要的温室气体 和
和 进行重整,涉及主要反应如下:
进行重整,涉及主要反应如下:
反应I: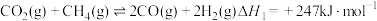
反应Ⅱ:
(1)若恒温、恒压的密闭容器中只发生反应I,下列能说明反应已达到化学平衡状态的是______。
(2)恒温刚性密闭容器中,按 投料,初始总压3MPa,达到平衡状态时测得
投料,初始总压3MPa,达到平衡状态时测得 和
和 转化率分别为60%、40%。计算该温度下反应I的压强平衡常数
转化率分别为60%、40%。计算该温度下反应I的压强平衡常数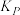 =
=______  (用各物质的分压代替物质的量浓度计算,分压=总压×物质的量分数)。
(用各物质的分压代替物质的量浓度计算,分压=总压×物质的量分数)。
(3)某研究小组为了评估甲烷干重整反应中不同催化剂的性能差异,在常压、催化剂作用下,按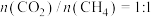 投料,不同温度下反应相同时间,测得
投料,不同温度下反应相同时间,测得 的转化率(柱形图)和产物
的转化率(柱形图)和产物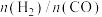 (
( )如图所示。请分析产物
)如图所示。请分析产物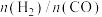 随温度变化的原因(不考虑催化剂失活)
随温度变化的原因(不考虑催化剂失活)______ 。 ;
;
(b) 。因此该小组借助X射线衍射(如图)定性评估催化剂的积碳情况。已知积碳会在
。因此该小组借助X射线衍射(如图)定性评估催化剂的积碳情况。已知积碳会在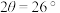 出现衍射峰,下列说法正确的是______。
出现衍射峰,下列说法正确的是______。
(5)该研究小组查阅资料发现还可利用电解还原 ,电解过程中常需要调控溶液pH以实现有效转化。现有1.0L
,电解过程中常需要调控溶液pH以实现有效转化。现有1.0L
 溶液,在298K下加入醋酸钾固体将
溶液,在298K下加入醋酸钾固体将 调至
调至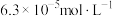 ,忽略溶液体积变化,所加醋酸钾固体的质量为
,忽略溶液体积变化,所加醋酸钾固体的质量为______ g。[已知:298K时, ]
]
 不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方法再利用。其中甲烷干重整反应可以将两类重要的温室气体
不仅是一种温室气体,也是一种来源广泛且廉价易得的碳资源,可通过热化学、电化学等方法再利用。其中甲烷干重整反应可以将两类重要的温室气体 和
和 进行重整,涉及主要反应如下:
进行重整,涉及主要反应如下:反应I:
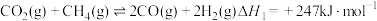
反应Ⅱ:

(1)若恒温、恒压的密闭容器中只发生反应I,下列能说明反应已达到化学平衡状态的是______。
| A.容器内气体密度不再发生变化 |
B. 和CO的物质的量之和不变 和CO的物质的量之和不变 |
C.化学反应速率 |
D.断裂4mol 键的同时生成2mol 键的同时生成2mol 键 键 |
(2)恒温刚性密闭容器中,按
 投料,初始总压3MPa,达到平衡状态时测得
投料,初始总压3MPa,达到平衡状态时测得 和
和 转化率分别为60%、40%。计算该温度下反应I的压强平衡常数
转化率分别为60%、40%。计算该温度下反应I的压强平衡常数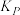 =
= (用各物质的分压代替物质的量浓度计算,分压=总压×物质的量分数)。
(用各物质的分压代替物质的量浓度计算,分压=总压×物质的量分数)。(3)某研究小组为了评估甲烷干重整反应中不同催化剂的性能差异,在常压、催化剂作用下,按
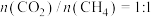 投料,不同温度下反应相同时间,测得
投料,不同温度下反应相同时间,测得 的转化率(柱形图)和产物
的转化率(柱形图)和产物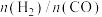 (
( )如图所示。请分析产物
)如图所示。请分析产物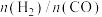 随温度变化的原因(不考虑催化剂失活)
随温度变化的原因(不考虑催化剂失活)
 ;
;(b)
 。因此该小组借助X射线衍射(如图)定性评估催化剂的积碳情况。已知积碳会在
。因此该小组借助X射线衍射(如图)定性评估催化剂的积碳情况。已知积碳会在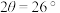 出现衍射峰,下列说法正确的是______。
出现衍射峰,下列说法正确的是______。
| A.碳附着在催化剂表面,使得活性位点与反应物之间的接触受阻,所以催化活性受到抑制 |
| B.一般甲烷干重整的反应温度都很高,因此副反应a很可能是实际过程中产生积碳的主要原因 |
| C.对比三种催化剂的X射线衍射结果可发现Ir型催化剂没有明显积碳,能在甲烷干重整过程中保持高稳定性 |
| D.该小组进一步评估新型金属复合催化剂(H型和M型)的积碳情况,将反应后的催化剂加热至恒重后,发现H型和M型催化剂的重量损失分别为16.7%和10.2%,这表明H型催化剂能在甲烷干重整过程中保持更高的稳定性 |
(5)该研究小组查阅资料发现还可利用电解还原
 ,电解过程中常需要调控溶液pH以实现有效转化。现有1.0L
,电解过程中常需要调控溶液pH以实现有效转化。现有1.0L
 溶液,在298K下加入醋酸钾固体将
溶液,在298K下加入醋酸钾固体将 调至
调至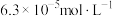 ,忽略溶液体积变化,所加醋酸钾固体的质量为
,忽略溶液体积变化,所加醋酸钾固体的质量为 ]
]
您最近一年使用:0次
2 . 常温下,将0.1 mol/L NaOH溶液分别滴入20 mL0.1 mol/L HX溶液与20 mL 0.1mol/L HCl溶液中,溶液pH随滴入NaOH溶液体积变化的图像如下图所示。下列说法错误的是
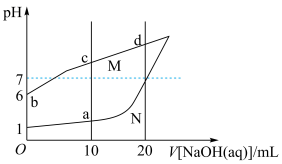
| A.N曲线代表HCl溶液 |
B.水的电离程度: |
C.HX的电离常数 为 为 |
| D.a、d点溶液混合后呈酸性 |
您最近一年使用:0次
3 . 室温下,向 柠檬酸钠
柠檬酸钠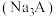 溶液中通入
溶液中通入 气体(忽略溶液体积变化),溶液中
气体(忽略溶液体积变化),溶液中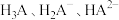 和
和 的分布系数
的分布系数 (某种含A微粒浓度与所有含A微粒浓度之和的比值)随
(某种含A微粒浓度与所有含A微粒浓度之和的比值)随 变化曲线如图所示.下列说法错误的是
变化曲线如图所示.下列说法错误的是
 柠檬酸钠
柠檬酸钠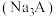 溶液中通入
溶液中通入 气体(忽略溶液体积变化),溶液中
气体(忽略溶液体积变化),溶液中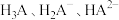 和
和 的分布系数
的分布系数 (某种含A微粒浓度与所有含A微粒浓度之和的比值)随
(某种含A微粒浓度与所有含A微粒浓度之和的比值)随 变化曲线如图所示.下列说法错误的是
变化曲线如图所示.下列说法错误的是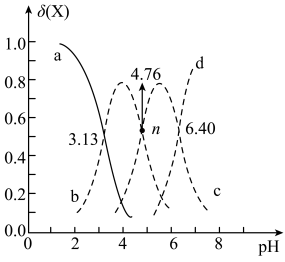
A.曲线c表示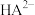 | B. 的水解平衡常数 的水解平衡常数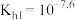 |
C.n点: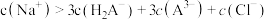 | D. 约为5时,通入 约为5时,通入 发生的反应为 发生的反应为 |
您最近一年使用:0次
7日内更新
|
91次组卷
|
2卷引用:安徽省县中联盟2023-2024学年高三下学期(三模)联考化学试题
4 . 饱和 溶液中,
溶液中,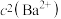 随
随 而变化,在
而变化,在 温度下,
温度下,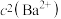 与
与 关系如右图所示。下列说法错误的是
关系如右图所示。下列说法错误的是
 溶液中,
溶液中,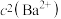 随
随 而变化,在
而变化,在 温度下,
温度下,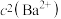 与
与 关系如右图所示。下列说法错误的是
关系如右图所示。下列说法错误的是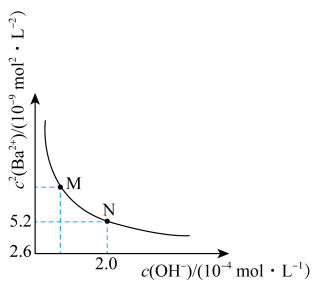
A. 的溶度积 的溶度积 |
B.若忽略 的第二步水解, 的第二步水解,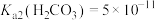 |
C.饱和 溶液中 溶液中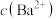 随 随 增大而减小 增大而减小 |
D. 点溶液中: 点溶液中: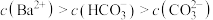 |
您最近一年使用:0次
7日内更新
|
69次组卷
|
2卷引用:河北省邯郸市部分示范性高中2024届高三下学期模拟考试(三模)化学试题
解题方法
5 . 常温常压下,H2S气体在水中的饱和浓度约为 ,已知:
,已知: ,
,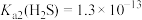 ;
;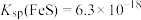 。下列说法
。下列说法不正确 的是
 ,已知:
,已知: ,
,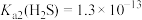 ;
;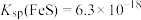 。下列说法
。下列说法A.饱和H2S溶液中存在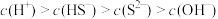 |
B.向 溶液中加几滴浓盐酸,使其浓度达到 溶液中加几滴浓盐酸,使其浓度达到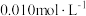 ,此时溶液中 ,此时溶液中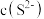 约为 约为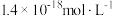 |
C.向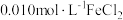 溶液中通入H2S气体直至饱和,溶液中有FeS沉淀生成 溶液中通入H2S气体直至饱和,溶液中有FeS沉淀生成 |
D.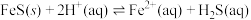 的平衡常数为 的平衡常数为 |
您最近一年使用:0次
7日内更新
|
81次组卷
|
2卷引用:2024届浙江省金华市义乌市高三下学期三模化学试题
名校
6 .  时,用氨水分别滴定浓度均为
时,用氨水分别滴定浓度均为 的
的 、
、 、
、 三种溶液,
三种溶液,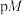 随
随 的变化关系如图所示[
的变化关系如图所示[ 表示负对数,
表示负对数, 表示
表示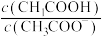 、
、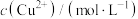 、
、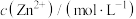 等],已知
等],已知 ,溶液中离子浓度小于
,溶液中离子浓度小于 可以认为已经除去。下列有关分析错误的是
可以认为已经除去。下列有关分析错误的是
 时,用氨水分别滴定浓度均为
时,用氨水分别滴定浓度均为 的
的 、
、 、
、 三种溶液,
三种溶液,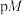 随
随 的变化关系如图所示[
的变化关系如图所示[ 表示负对数,
表示负对数, 表示
表示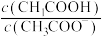 、
、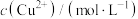 、
、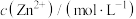 等],已知
等],已知 ,溶液中离子浓度小于
,溶液中离子浓度小于 可以认为已经除去。下列有关分析错误的是
可以认为已经除去。下列有关分析错误的是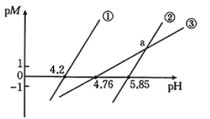
A. 时, 时, |
B. 点对应的 点对应的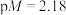 |
C.可通过调节 的方法除尽 的方法除尽 溶液(浓度为 溶液(浓度为 )中含有的 )中含有的 |
D.氨水过量时,均可形成 ( ( 表示 表示 或 或 ) ) |
您最近一年使用:0次
7日内更新
|
122次组卷
|
2卷引用:河北省保定市九校2024届高三下学期二模化学试题
名校
7 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.标准状况下 溶于足量水,所得溶液中 溶于足量水,所得溶液中 、 、 、 、 和 和 微粒总数为 微粒总数为 |
B.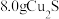 和 和 的混合物中含有的铜原子数为 的混合物中含有的铜原子数为 |
C.常温常压下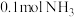 与 与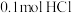 充分反应后所得到产物中含有分子数仍为 充分反应后所得到产物中含有分子数仍为 |
D.室温下向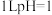 的醋酸溶液中加水,所得溶液中 的醋酸溶液中加水,所得溶液中 数目小于 数目小于 |
您最近一年使用:0次
8 . 298K时,用NaOH溶液分别滴定等物质的量浓度的HR、 、
、 三种溶液。pM[p表示负对数,M表示
三种溶液。pM[p表示负对数,M表示 、
、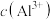 .
. ]随溶液pH变化的关系如图所示。已知:常温下,
]随溶液pH变化的关系如图所示。已知:常温下,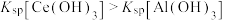 ,当离子浓度
,当离子浓度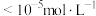 时,该离子完全沉淀。下列推断正确的是
时,该离子完全沉淀。下列推断正确的是
 、
、 三种溶液。pM[p表示负对数,M表示
三种溶液。pM[p表示负对数,M表示 、
、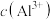 .
. ]随溶液pH变化的关系如图所示。已知:常温下,
]随溶液pH变化的关系如图所示。已知:常温下,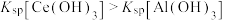 ,当离子浓度
,当离子浓度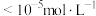 时,该离子完全沉淀。下列推断正确的是
时,该离子完全沉淀。下列推断正确的是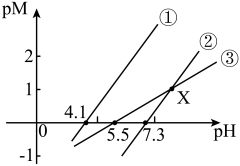
A.①代表滴定 溶液的变化关系 溶液的变化关系 |
B.调节pH=5时,溶液中 完全沉淀 完全沉淀 |
C.滴定HR溶液至X点时,溶液中: |
D.经计算, 不能完全溶于HR溶液 不能完全溶于HR溶液 |
您最近一年使用:0次
9 . 电位滴定是利用溶液电位突变指示终点的滴定法。常温下,某研究小组利用电位滴定法研究盐酸滴定亚磷酸钠 溶液过程中的化学变化,得到滴定过程中溶液电位E与
溶液过程中的化学变化,得到滴定过程中溶液电位E与 的关系如图所示。已知:亚磷酸是二元弱酸,常温下其电离常数分别是:
的关系如图所示。已知:亚磷酸是二元弱酸,常温下其电离常数分别是: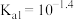 ,
,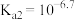 ,下列说法正确的是
,下列说法正确的是
 溶液过程中的化学变化,得到滴定过程中溶液电位E与
溶液过程中的化学变化,得到滴定过程中溶液电位E与 的关系如图所示。已知:亚磷酸是二元弱酸,常温下其电离常数分别是:
的关系如图所示。已知:亚磷酸是二元弱酸,常温下其电离常数分别是: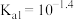 ,
,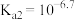 ,下列说法正确的是
,下列说法正确的是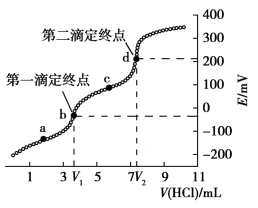
A.水的电离程度: |
B.b点对应溶液的 |
C.第二滴定终点时发生反应的平衡常数为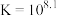 |
D.c点对应溶液中一定存在: |
您最近一年使用:0次
10 . 下列物质属于强电解质的是
| A.镁 | B. | C.HF | D.硬脂酸钠 |
您最近一年使用:0次



