常温下,将0.1 mol/L NaOH溶液分别滴入20 mL0.1 mol/L HX溶液与20 mL 0.1mol/L HCl溶液中,溶液pH随滴入NaOH溶液体积变化的图像如下图所示。下列说法错误的是
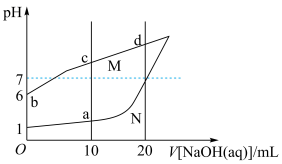
| A.N曲线代表HCl溶液 |
B.水的电离程度: |
C.HX的电离常数 为 为 |
| D.a、d点溶液混合后呈酸性 |
更新时间:2024-06-03 09:42:52
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下,在新制氯水中滴加NaOH溶液,溶液中水电离出的c(H+)与NaOH溶液的体积之间的关系如图所示,下列推断正确的是
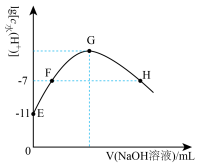

| A.可用pH试纸测定E点对应溶液,其pH=3 |
| B.H、F点的导电能力一定相同 |
| C.H、F点对应溶液中都存在:c (Na+)=c(Cl-)+c(ClO-) |
| D.G点对应溶液中:c(Na+)>c(Cl-)>c(ClO-)>c(OH- )>c(H+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,下列溶液中水的电离程度最大的是
| A.pH=5的硫酸 | B.pH=9的NaOH溶液 |
| C.pH=5的NaHSO3溶液 | D.pH=8的NaHCO3溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列事实不能用勒夏特列原理解释的是
| A.100℃时,纯水的pH≈6 |
| B.实验室常用排饱和食盐水的方法收集氯气 |
| C.实验室用过氧化氢制取氧气时,常常加入MnO2固体 |
| D.工业上采用高压条件合成氨气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】用甲醛法可间接测定尿素含量。称取 尿素
尿素 样品处理转化为铵盐,
样品处理转化为铵盐, 与甲醛发生反应[
与甲醛发生反应[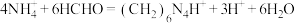 ,
,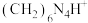 可看做一元酸],经转化后得到
可看做一元酸],经转化后得到 溶液,量取
溶液,量取 放入锥形瓶中,滴加2滴酚酞,用
放入锥形瓶中,滴加2滴酚酞,用 标准溶液滴定,滴定至终点时,消耗碱液体积
标准溶液滴定,滴定至终点时,消耗碱液体积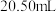 。下列说法正确的是
。下列说法正确的是
 尿素
尿素 样品处理转化为铵盐,
样品处理转化为铵盐, 与甲醛发生反应[
与甲醛发生反应[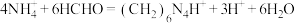 ,
,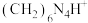 可看做一元酸],经转化后得到
可看做一元酸],经转化后得到 溶液,量取
溶液,量取 放入锥形瓶中,滴加2滴酚酞,用
放入锥形瓶中,滴加2滴酚酞,用 标准溶液滴定,滴定至终点时,消耗碱液体积
标准溶液滴定,滴定至终点时,消耗碱液体积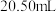 。下列说法正确的是
。下列说法正确的是| A.尿素转化为铵盐过程中N元素化合价降低 |
| B.当滴入最后半滴NaOH标准溶液时溶液恰好由无色变浅红色即为滴定终点 |
| C.若滴定前仰视读数,滴定终点时俯视读数,则测的结果偏高 |
| D.上述过程测得尿素质量分数为82.00% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列图示与叙述不相符的是
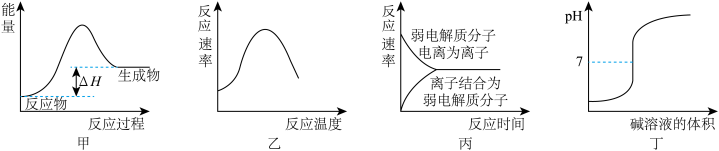

| A.图甲可表示生石灰和水反应的能量变化 |
| B.图乙可表示酶催化反应的反应速率随反应温度的变化 |
| C.图丙可表示乙酸在水中建立电离平衡的过程 |
| D.图丁可表示氢氧化钡溶液滴定硫酸溶液的滴定曲线 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】氯化亚砜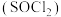 是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用
是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用 和
和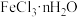 制备无水
制备无水 。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。
。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。
①称取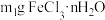 于试管中,加入足量
于试管中,加入足量 ,充分反应后固体质量为
,充分反应后固体质量为 。反应后的固体加入稀硫酸溶解,并分成两等份。
。反应后的固体加入稀硫酸溶解,并分成两等份。
②向其中一份溶液中滴加试剂X,验证实验过程中发生了副反应。
③向另一份溶液中加入适量还原剂将 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,用新配制的
酸化后,用新配制的 标准溶液滴定
标准溶液滴定 ,达终点时消耗标准溶液
,达终点时消耗标准溶液 (滴定过程中
(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。
步骤②中试剂X的化学式可为
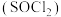 是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用
是一种无色或淡黄色发烟液体,遇水剧烈反应生成两种酸性气体,可用 和
和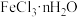 制备无水
制备无水 。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。
。由于该实验过程中可能会发生副反应使产品不纯,为测定n值,设计如下实验方案。①称取
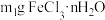 于试管中,加入足量
于试管中,加入足量 ,充分反应后固体质量为
,充分反应后固体质量为 。反应后的固体加入稀硫酸溶解,并分成两等份。
。反应后的固体加入稀硫酸溶解,并分成两等份。②向其中一份溶液中滴加试剂X,验证实验过程中发生了副反应。
③向另一份溶液中加入适量还原剂将
 完全还原为
完全还原为 ,加入稀
,加入稀 酸化后,用新配制的
酸化后,用新配制的 标准溶液滴定
标准溶液滴定 ,达终点时消耗标准溶液
,达终点时消耗标准溶液 (滴定过程中
(滴定过程中 转化为
转化为 ,
, 不反应)。
不反应)。步骤②中试剂X的化学式可为
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】液氨与纯水类似,也存在微弱的电离: ,T℃时,液氨的离子积常数
,T℃时,液氨的离子积常数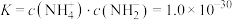 ,若用定义pH的方式来规定
,若用定义pH的方式来规定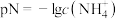 ,则下列叙述正确的是
,则下列叙述正确的是
 ,T℃时,液氨的离子积常数
,T℃时,液氨的离子积常数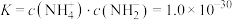 ,若用定义pH的方式来规定
,若用定义pH的方式来规定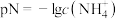 ,则下列叙述正确的是
,则下列叙述正确的是| A.其他条件不变,增加液氨的量,电离平衡正向移动 |
B.液氨达到电离平衡时 |
| C.T℃时1L溶解有0.001molNH4Cl的液氨溶液,其pN=3 |
| D.一定温度下,向液氨中加入氯化铵固体,电离平衡逆向移动,K值减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,用0.100mol·L-1的NaOH溶液分别滴定同浓度、体积均为20.00mL的盐酸和醋酸溶液(用HA表示酸),得到2条滴定曲线,如图所示。

下列说法正确的是

下列说法正确的是
| A.滴定醋酸的曲线是图1 |
| B.由图分析可得b>a=20 |
| C.D点对应的溶液中:c(Na+)=c(A-) |
| D.根据E点可计算得K(HA)=[0.05+(10-6-10-8)]×10-8/(10-6-10-8) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】25 ℃时,相同体帜和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如右图所示。下列说法正确的是
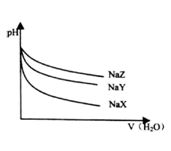

| A.在上述三种盐的原溶液中,水的电离度大小是NaX>NaY>NaZ |
| B.在等物质的量浓度的NaX、NaY、NaZ混合溶液中,离子浓度的大小关系是c(Z- )<c(Y- )<c(X- ) |
| C.在等物质的量浓度的NaX和NaY的混合液中存在c(HX)/c(X- )=c(HY)/c(Y -) |
D.浓度均为0. 1mol·L-1的NaX、NaY、NaZ的混合溶液中:c(OH- )=  +c(HX)+c(HY)+c(HZ) +c(HX)+c(HY)+c(HZ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如表,下列叙述正确的是
酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
电离平衡常数 |
|
|
|
|
A.将 的醋酸加水不断稀释,所有离子浓度均减小 的醋酸加水不断稀释,所有离子浓度均减小 |
B.少量 通入NaClO溶液中反应的离子方程式为 通入NaClO溶液中反应的离子方程式为 |
C.少量的 通入 通入 溶液中反应的离子方程式为 溶液中反应的离子方程式为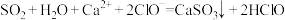 |
D.酸性由强到弱排序: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】25 °C时,0.1 mol·L-1R2SO4溶液加水稀释,混合溶液中lg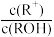 与lgc(OH-)的关系如图所示。下列说法错误的是
与lgc(OH-)的关系如图所示。下列说法错误的是

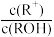 与lgc(OH-)的关系如图所示。下列说法错误的是
与lgc(OH-)的关系如图所示。下列说法错误的是
| A.Kb(ROH)的数量级为10 -6) |
B.P、Q点对应溶液中 的值:P<Q 的值:P<Q |
C.若将溶液无限稀释,溶液中:c(R+ ) ≈2c( ) ) |
| D.相同条件下,若c(R2SO4)=0.2 mol·L-1,则P点将移向W点 |
您最近一年使用:0次


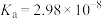

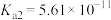
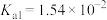

 表示,
表示, 时,用
时,用 ,溶液中含各种微粒的分布系数
,溶液中含各种微粒的分布系数 与
与 的分布系数:
的分布系数: ],下列叙述正确的是
],下列叙述正确的是
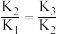
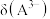 ,曲线4代表
,曲线4代表
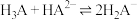 的
的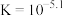
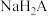 溶液、
溶液、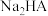 溶液都显酸性
溶液都显酸性

