名校
1 . 一种芳香族化合物 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为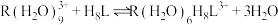 。分配比
。分配比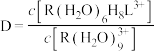 ,水相初始浓度
,水相初始浓度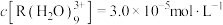 ,萃取平衡时
,萃取平衡时 关系如图。下列说法正确的是
关系如图。下列说法正确的是
 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为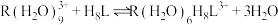 。分配比
。分配比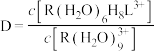 ,水相初始浓度
,水相初始浓度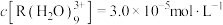 ,萃取平衡时
,萃取平衡时 关系如图。下列说法正确的是
关系如图。下列说法正确的是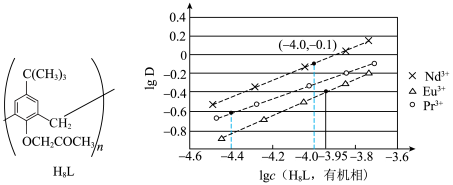
A. 对 对 萃取效果最好 萃取效果最好 |
B. 可通过缩聚反应制得 可通过缩聚反应制得 |
C.达平衡时水相中 |
D.萃取平衡时,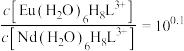 |
您最近一年使用:0次
2 . 常温下,将一定浓度的氨水逐滴加入25mL0.12mol⋅L
 溶液中,该过程中溶液
溶液中,该过程中溶液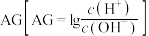 与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的
与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的 与
与 均约为
均约为 mol⋅L
mol⋅L 。下列叙述正确的是
。下列叙述正确的是

 溶液中,该过程中溶液
溶液中,该过程中溶液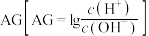 与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的
与加入氨水体积V的关系如图所示,已知e点对应的溶液迅速由浑浊变澄清,且此时溶液中的 与
与 均约为
均约为 mol⋅L
mol⋅L 。下列叙述正确的是
。下列叙述正确的是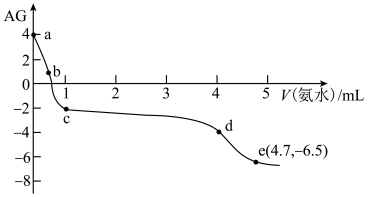
| A.最好选择d~e段溶液与葡萄糖等含有醛基的有机物发生银镜反应 |
B.a点对应溶液中由水电离出的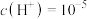 mol⋅L mol⋅L |
C.b点对应溶液中: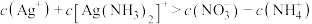 |
D.由e点可知,反应 的平衡常数约为 的平衡常数约为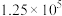 |
您最近一年使用:0次
名校
3 . 有下列几种物质:① 晶体;②
晶体;② ;③
;③ 溶液;④
溶液;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ (酒精);⑦
(酒精);⑦ ;⑧氨水;⑨饱和
;⑧氨水;⑨饱和 溶液。根据要求回答下列问题:
溶液。根据要求回答下列问题:
1.上述各物质属于强电解质的是___________ (填物质编号,下同);属于非电解质的是___________ 。
2.写出少量④通入⑤中反应的离子方程式:___________ ;③和⑧在水溶液中反应的离子方程式:___________ 。
3.将⑨加入到沸水中,继续加热溶液呈红褐色,制得 胶体,该反应的离子方程式:
胶体,该反应的离子方程式:___________ 。
4.向③中加入⑤至溶液中恰好呈中性,写出该反应的离子方程式:___________ 。
 晶体;②
晶体;② ;③
;③ 溶液;④
溶液;④ ;⑤
;⑤ 溶液;⑥
溶液;⑥ (酒精);⑦
(酒精);⑦ ;⑧氨水;⑨饱和
;⑧氨水;⑨饱和 溶液。根据要求回答下列问题:
溶液。根据要求回答下列问题:1.上述各物质属于强电解质的是
2.写出少量④通入⑤中反应的离子方程式:
3.将⑨加入到沸水中,继续加热溶液呈红褐色,制得
 胶体,该反应的离子方程式:
胶体,该反应的离子方程式:4.向③中加入⑤至溶液中恰好呈中性,写出该反应的离子方程式:
您最近一年使用:0次
名校
解题方法
4 . 亚砷酸C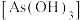 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数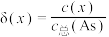 。下列说法错误的是
。下列说法错误的是
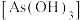 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数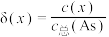 。下列说法错误的是
。下列说法错误的是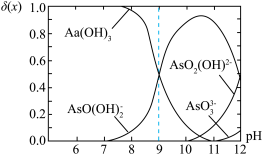
A. |
B. 时,水电离的 时,水电离的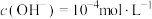 |
C.等物质的量浓度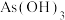 和 和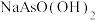 混合溶液中 混合溶液中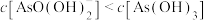 |
D.当溶液 后,体系中 后,体系中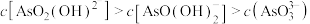 |
您最近一年使用:0次
昨日更新
|
43次组卷
|
2卷引用:2024届陕西省部分学校高三下学期5月份高考适应性考试理科综合试题-高中化学
5 . 研究弱电解质的电离及盐的水解,有重要的实际意义。
(1)醋酸的电离方程式为_______ 。
(2)下列事实不能说明CH3COOH是弱电解质的是_______(填标号)。
(3)某些弱酸在25℃时的电离常数(Ka)如表:
①同浓度的 CH3COOH、H2CO3、HClO 溶液的 pH 最大的是_______ 。
②常温下 0.1mol/L的 CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是_______ (填字母序号,下同)。
A.c(H⁺) B.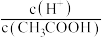 C.
C.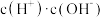 D.
D. E.
E. 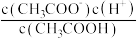
③若该溶液升高温度,上述5种表达式的数据减小的是_______ 。
④下列反应可以发生的是_______ (填标号)。
A. CH3COOH+ Na2CO3=NaHCO3 +CH3COONa
B. CH3COOH+NaCN=CH3COONa+HCN
C. CO2+H2O+2NaClO=Na2CO3+2HClO
D. NaHCO3+HCN=NaCN+H2O+CO2↑
(4)肼(N2H4)是一种二元弱碱,在水中的电离方式与NH3相似,写出第一步电离的离子方程式_______ 。
(5)已知 。
。 属于
属于_______ (填“一”“二”或“三”)元酸, 属于
属于_______ (填“正盐”或“酸式盐”)。
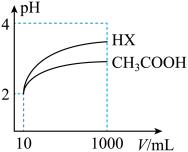
(6)体积为 10mL pH=2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至1000mL, 稀释过程pH变化如图:则HX的电离平衡常数_______ (填“大于”、“等于”或“小于”)醋酸的平衡常数。 稀释后,HX 溶液中有水电离出来的c(H⁺)_______ (填“大于”、“等于”或“小于”)醋酸的溶液中有水电离出来的c(H⁺),理由是_______ 。
(1)醋酸的电离方程式为
(2)下列事实不能说明CH3COOH是弱电解质的是_______(填标号)。
| A.相同温度下,浓度均为1mol/L的盐酸和醋酸的导电性对比:盐酸明显大于醋酸 |
| B.1mol/LCH3COONa溶液能使紫色石蕊试液变蓝 |
| C.25℃时,1 mol/LCH3COOH溶液的pH约为2 |
| D.10 mL1mol/L的CH3COOH溶液恰好与10 mL 1 mol/LNaOH溶液完全反应 |
(3)某些弱酸在25℃时的电离常数(Ka)如表:
| 化学式 | CH3COOH | HCN | HClO | H2CO3 |
| 电离常数(Ka) | 1.8×10-5 | 4.9×10 -10 | 3.0×10-8 | Ka1=4.4×10-7,Ka2=4.7×10-11 |
②常温下 0.1mol/L的 CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是
A.c(H⁺) B.
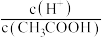 C.
C.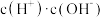 D.
D. E.
E. 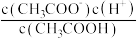
③若该溶液升高温度,上述5种表达式的数据减小的是
④下列反应可以发生的是
A. CH3COOH+ Na2CO3=NaHCO3 +CH3COONa
B. CH3COOH+NaCN=CH3COONa+HCN
C. CO2+H2O+2NaClO=Na2CO3+2HClO
D. NaHCO3+HCN=NaCN+H2O+CO2↑
(4)肼(N2H4)是一种二元弱碱,在水中的电离方式与NH3相似,写出第一步电离的离子方程式
(5)已知
 。
。 属于
属于 属于
属于(6)体积为 10mL pH=2 的醋酸溶液与一元酸 HX 溶液分别加水稀释至1000mL, 稀释过程pH变化如图:则HX的电离平衡常数
您最近一年使用:0次
解题方法
6 . 下列物质的水溶液呈酸性且为弱电解质的是
A. | B. | C. | D. |
您最近一年使用:0次
7 . 某废水处理过程中始终保持 饱和,即
饱和,即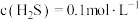 ,通过调节
,通过调节 使
使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与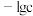 关系如图所示,c为
关系如图所示,c为 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知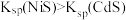 ,下列说法正确的是
,下列说法正确的是
 饱和,即
饱和,即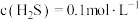 ,通过调节
,通过调节 使
使 和
和 形成硫化物而分离,体系中
形成硫化物而分离,体系中 与
与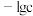 关系如图所示,c为
关系如图所示,c为 、
、 、
、 和
和 的浓度,单位为
的浓度,单位为 。已知
。已知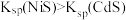 ,下列说法正确的是
,下列说法正确的是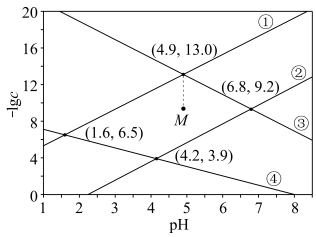
A.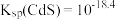 |
B.M点条件下能生成 沉淀,不能生成 沉淀,不能生成 沉淀 沉淀 |
C.③为 与 与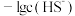 的关系曲线 的关系曲线 |
D.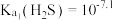 |
您最近一年使用:0次
名校
8 . 琥珀酸(丁二酸,简记为 )为二元弱酸。常温下,在含
)为二元弱酸。常温下,在含 和
和 的混合液中滴加
的混合液中滴加 溶液,溶液
溶液,溶液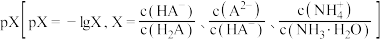 与
与 的关系如图所示。
的关系如图所示。
 )为二元弱酸。常温下,在含
)为二元弱酸。常温下,在含 和
和 的混合液中滴加
的混合液中滴加 溶液,溶液
溶液,溶液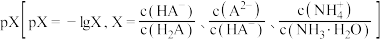 与
与 的关系如图所示。
的关系如图所示。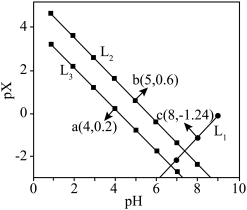
A.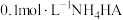 溶液中: 溶液中: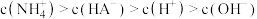 |
B.当 时, 时,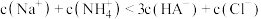 |
C.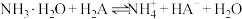 的平衡常数K小于 的平衡常数K小于 |
D. 和 和 直线交点坐标为(7.42,-1.82) 直线交点坐标为(7.42,-1.82) |
您最近一年使用:0次
9 . 利用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 (起始浓度为
(起始浓度为 )体系中的可能产物。
)体系中的可能产物。
已知:
ⅰ.图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ.图2表示不同pH下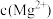 的变化。
的变化。
 在不同pH的
在不同pH的 (起始浓度为
(起始浓度为 )体系中的可能产物。
)体系中的可能产物。已知:
ⅰ.图1中曲线表示
 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。ⅱ.图2表示不同pH下
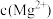 的变化。
的变化。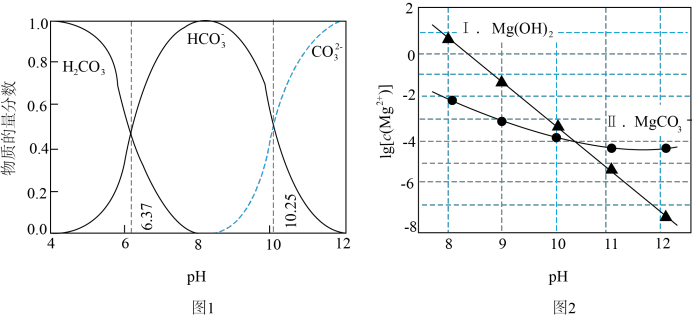
A.由图1,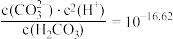 |
B.在 时,一定存在 时,一定存在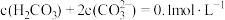 |
C.由图2,初始状态 、 、 ,无沉淀生成 ,无沉淀生成 |
D.由图1和图2,初始状态 、 、 ,主要发生反应: ,主要发生反应: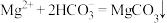  |
您最近一年使用:0次
10 . 用0.1 NaOH标准溶液滴定20mL等浓度的三元酸
NaOH标准溶液滴定20mL等浓度的三元酸 ,得到pH与
,得到pH与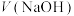 、
、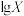 [
[ 或
或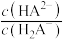 或
或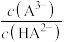 ]的关系分别如图1、图2所示。
]的关系分别如图1、图2所示。
 NaOH标准溶液滴定20mL等浓度的三元酸
NaOH标准溶液滴定20mL等浓度的三元酸 ,得到pH与
,得到pH与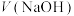 、
、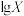 [
[ 或
或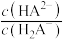 或
或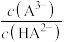 ]的关系分别如图1、图2所示。
]的关系分别如图1、图2所示。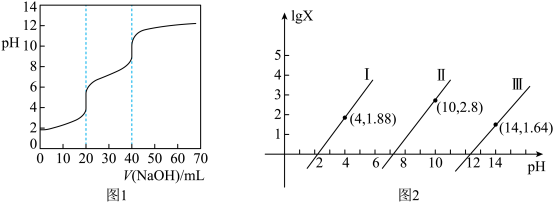
A.当加入20mL NaOH溶液时,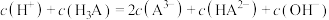 |
B.当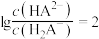 时,水电离出的 时,水电离出的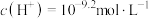 |
C.当加入40mL NaOH溶液时, |
D.当pH=11时,溶液中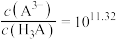 |
您最近一年使用:0次
7日内更新
|
345次组卷
|
3卷引用:山东省潍坊市2024届高三下学期二模化学试题



