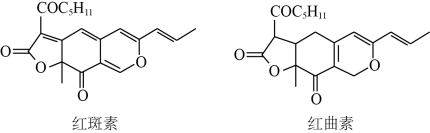
一种芳香族化合物 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为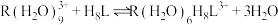 。分配比
。分配比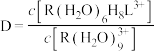 ,水相初始浓度
,水相初始浓度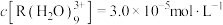 ,萃取平衡时
,萃取平衡时 关系如图。下列说法正确的是
关系如图。下列说法正确的是
 结构如图。
结构如图。 萃取稀土离子
萃取稀土离子 的原理为
的原理为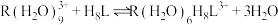 。分配比
。分配比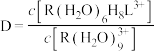 ,水相初始浓度
,水相初始浓度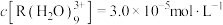 ,萃取平衡时
,萃取平衡时 关系如图。下列说法正确的是
关系如图。下列说法正确的是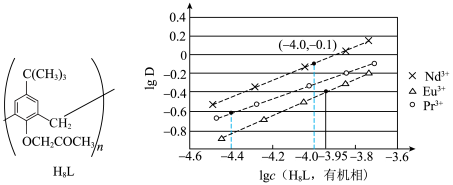
A. 对 对 萃取效果最好 萃取效果最好 |
B. 可通过缩聚反应制得 可通过缩聚反应制得 |
C.达平衡时水相中 |
D.萃取平衡时,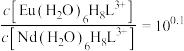 |
更新时间:2024-05-27 09:17:24
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】一定温度下,下列溶液的离子浓度关系式正确的是
A.0.1mol•L-1NaHCO3溶液中:c(Na+)+c(H+)=c(HCO )+c(CO )+c(CO )+c(OH-) )+c(OH-) |
| B.Na2CO3溶液中:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C.Na2S溶液中:2c(Na+)=C(S2-)+C(HS-)+c(H2S) |
| D.pH相同的①CH3COONa、②NaOH、③NaClO三种溶液的c(Na+):③>①>② |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25°C时,以甲基橙为指示剂用0.1000 mol·L-1的NaOH溶液滴定二元酸H2X溶液。溶液的pH及溶液中H2X、 HX-及X2-的物质的量液度变化如图所示,下列说法错误的是
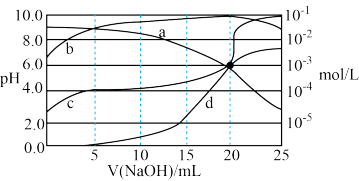

| A.a曲线表示c(H2X) ,d曲线表示c(X2-) |
| B.H2X的电离平衡常数Ka1 =1×10-4 |
C.V (NaOH) =5mL时,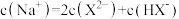 |
| D.滴定终点时:2c(H2X) +c(H+)= c(OH-)-c(HX-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】化合物丙是合成药物盐酸沙格雷酯的重要中间体,其合成路线中的前两步反应如下。下列说法不正确的是

A.甲中C原子的杂化类型皆为 | B.甲分子和甲醛在一定条件下能发生缩聚反应 |
C.乙与足量 加成产物中有3个手性碳原子 加成产物中有3个手性碳原子 | D.丙分子能使酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下图所示的某聚酰胺树脂是飞机材料中的一种,具有较好的耐热性、耐水性。则下列说法不正确的是


| A.该树脂材料可通过缩聚反应合成 |
| B.该树脂能使溴水褪色 |
| C.该树脂中所有碳原子不可能在同一平面上 |
D.合成该树脂单体可以是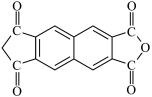 和 和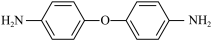 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】人体血液存在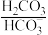 、
、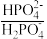 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值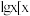 表示
表示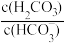 或
或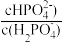 与pH的关系如图所示,已知碳酸
与pH的关系如图所示,已知碳酸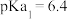 、磷酸
、磷酸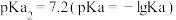 ,则下列说法正确的是
,则下列说法正确的是

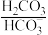 、
、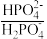 等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值
等缓冲对。常温下,水溶液中各缓冲对的微粒浓度之比的对数值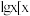 表示
表示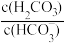 或
或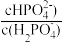 与pH的关系如图所示,已知碳酸
与pH的关系如图所示,已知碳酸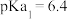 、磷酸
、磷酸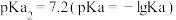 ,则下列说法正确的是
,则下列说法正确的是
A.曲线Ⅱ表示 与pH的变化关系 与pH的变化关系 |
B.当 时, 时,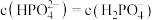 |
C.当pH增大时,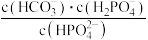 逐渐减小 逐渐减小 |
D. 的过程中,水的电离程度逐渐减小 的过程中,水的电离程度逐渐减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】天然溶洞的形成与水体中含碳物种的浓度有密切关系。已知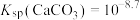 ,某溶洞水体中
,某溶洞水体中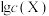 (X为
(X为 、
、 或
或 )与
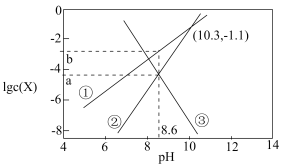
)与 变化的关系如下图所示。下列说法正确的是
变化的关系如下图所示。下列说法正确的是
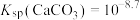 ,某溶洞水体中
,某溶洞水体中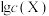 (X为
(X为 、
、 或
或 )与
)与 变化的关系如下图所示。下列说法正确的是
变化的关系如下图所示。下列说法正确的是
A.曲线②代表 |
B.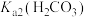 的数量级为 的数量级为 |
C. , , |
D. 时, 时,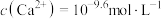 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】25℃时,向Na2CO3溶液中逐滴滴入稀盐酸,所得混合溶液的pH与离子浓度变化关系如图所示。下列叙述正确的是
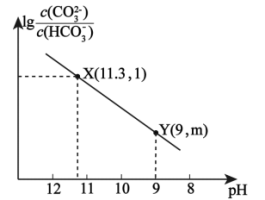

A.图中 |
B. 的水解常数 的水解常数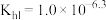 |
| C.随pH的逐渐减小,水的电离程度逐渐增大 |
D.X点溶液中: |
您最近一年使用:0次