在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是___________ 。
(3)若三者pH相同时,物质的量浓度由大到小的顺序是___________ 。
(4)将pH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是___________ 。
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH 的能力由大到小的顺序是
(3)若三者pH相同时,物质的量浓度由大到小的顺序是
(4)将pH相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
(5)将pH相同的三种酸均加水稀释至原来的100倍后,pH由大到小的顺序是
更新时间:2024-05-15 21:23:44
|
【知识点】 一元强酸与一元弱酸的比较解读
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有H+浓度均为0.1mol/L的醋酸甲和盐酸乙:
(1)请写出醋酸的电离常数的表达式:_____ 。
(2)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡__________ (填“向左”、“向右”或“不”)移动,若加入少量的冰醋酸,醋酸的电离平衡________ (填“向左”、“向右”或“不”)移动,若加入少量无水醋酸钠固体,待固体溶解后,溶液中c(H+)/c(CH3COOH)的值将________ (填“增大”、“减小”或“无法确定”)。
(3)相同条件下,取等体积的甲、乙两溶液,加入足量的金属镁,开始反应时的速率:甲___ 乙(填“大于”、“小于”或“等于”)。产生氢气的体积:甲___ 乙(填“大于”、“小于”或“等于”)。
(4)0.1mol/L的甲溶液和0.05mol/L的甲溶液中氢离子浓度:前者是后者的_____ 。
A.小于2倍 B. 大于2倍 C. 等于2倍
(1)请写出醋酸的电离常数的表达式:
(2)取10 mL的甲溶液,加入等体积的水,醋酸的电离平衡
(3)相同条件下,取等体积的甲、乙两溶液,加入足量的金属镁,开始反应时的速率:甲
(4)0.1mol/L的甲溶液和0.05mol/L的甲溶液中氢离子浓度:前者是后者的
A.小于2倍 B. 大于2倍 C. 等于2倍
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】醋酸是一种常见的弱酸,在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:(填“正向”、“逆向”或“不移动”, “增大”、“减小”或“不变”, 填“>”、“<”或“=”)
(1)向醋酸中加入醋酸钠固体,电离平衡向___________ 移动;pH __________
(2)向醋酸中加入碳酸钙固体,电离平衡向________ 移动;c(CH3COOH)_________ .
(3)向醋酸中加入大量的水,c(OH-)_________ .导电能力__________ .
(4)体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①_____ ②;与完全相同的镁条发生反应,开始时的反应速率:①______ ②;中和等量NaOH时消耗的体积:①______ ②;与足量的Zn反应生成H2的物质的量:①_______ ②。
(1)向醋酸中加入醋酸钠固体,电离平衡向
(2)向醋酸中加入碳酸钙固体,电离平衡向
(3)向醋酸中加入大量的水,c(OH-)
(4)体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】常温下,向100mL0.01mol·L-1MOH溶液中逐滴加入0.02mol·L-1HA溶液,滴加过程中混合溶液的pH随着HA溶液体积变化如图所示(体积变化忽略不计)。
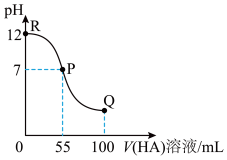
(1)由图中信息可知HA为___________ 酸(填“强”或 “弱”),理由是___________ 。
(2)R点时由水电离出的c(OH-)=___________ mol·L-1。
(3)常温下一定浓度的MA稀溶液中所有离子的浓度由大到小的顺序为:___________ 。
(4)Q点时所得溶液中,c(A-)+c(HA)___________ 2c(M+),c(M+)___________ c(HA)(填“>”、“<”或“=”)。

(1)由图中信息可知HA为
(2)R点时由水电离出的c(OH-)=
(3)常温下一定浓度的MA稀溶液中所有离子的浓度由大到小的顺序为:
(4)Q点时所得溶液中,c(A-)+c(HA)
您最近一年使用:0次



