醋酸是一种常见的弱酸,在0.1mol·L﹣1醋酸中加入下列物质,醋酸的电离平衡及平衡时物质的浓度的变化:(填“正向”、“逆向”或“不移动”, “增大”、“减小”或“不变”, 填“>”、“<”或“=”)
(1)向醋酸中加入醋酸钠固体,电离平衡向___________ 移动;pH __________
(2)向醋酸中加入碳酸钙固体,电离平衡向________ 移动;c(CH3COOH)_________ .
(3)向醋酸中加入大量的水,c(OH-)_________ .导电能力__________ .
(4)体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①_____ ②;与完全相同的镁条发生反应,开始时的反应速率:①______ ②;中和等量NaOH时消耗的体积:①______ ②;与足量的Zn反应生成H2的物质的量:①_______ ②。
(1)向醋酸中加入醋酸钠固体,电离平衡向
(2)向醋酸中加入碳酸钙固体,电离平衡向
(3)向醋酸中加入大量的水,c(OH-)
(4)体积相同、物质的量浓度均为0.1 mol·L-1的①盐酸、②醋酸两种溶液,pH:①
更新时间:2018-10-31 11:44:45
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】常温下,部分酸的电离平衡常数如下:
(1)c (H+)相同的三种酸,其酸的浓度从大到小为____________________ 。
(2)若HCN酸的起始浓度为0.0lmol/L,平衡时c(H+)约为____________ mol/L。若使此溶液中HCN的电离程度增大且c(H+)也增大的方法是____________ 。
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为aL、bL,则a______ b (填“大于”、“小于”或“等于”)。中和等浓度、等体积的氢氟酸和硫酸需要NaOH的物质的量为n1、n2,则n1_________ n2 (填“大于”、“小于”或“等于”)
(4)向NaCN中通入少量的CO2,发生的离子方程式为____________________ 。
| 化学式 | HF | HCN | H2CO3 |
| 电离常数 | Ka=3.5×10-4 | Ka=5.0×10-10 | Ka1=4.3×10-7,Ka2=5.6×10-11 |
(1)c (H+)相同的三种酸,其酸的浓度从大到小为
(2)若HCN酸的起始浓度为0.0lmol/L,平衡时c(H+)约为
(3)中和等量的NaOH,消耗等pH的氢氟酸和硫酸的体积分别为aL、bL,则a
(4)向NaCN中通入少量的CO2,发生的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有25 ℃时0.1 mol/L的氨水。请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 c(OH-) / c(NH3·H2O)________ (填“增大”“减小”或“不变”);
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:
_____________________________________________________________________ ;
所得溶液的pH________ 7(填“>”“<”或“=”),用离子方程式表示其原因:
_____________________________________________________________________ 。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol/L,则c(SO42-)=________ ;
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的关系是______________________________________ 。
(1)若向氨水中加入少量硫酸铵固体,此时溶液中 c(OH-) / c(NH3·H2O)
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:
所得溶液的pH
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH4+)=a mol/L,则c(SO42-)=
(4)若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1∶1,则所得溶液中各离子物质的量浓度由大到小的关系是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】弱电解质的研究是重要课题。
(1)①25℃时,已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不正确的是______ (填字母)。

a.pH=8时,溶液中含碳元素的微粒主要是HCO
b.A点溶液中H2CO3和HCO 浓度相同
浓度相同
c.当c(HCO )=c(CO
)=c(CO )时,c(H+)>c(OH-)
)时,c(H+)>c(OH-)
②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是______ 。
(2)H2CO3以及其他部分弱酸的电离平衡常数如表:
①H2S、H2CO3、HClO的酸性由强到弱的顺序为______ 。
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:______ 。
(3)常温下,已知0.1mol/L一元酸HCOOH(甲酸)溶液中 =1×10-8。
=1×10-8。
①0.1mol/LHCOOH溶液的pH=______ 。
②取10mL0.1mol/L的HCOOH溶液稀释至100倍,下列有关说法正确的是______ (填字母)。
A.所有离子的浓度在稀释过程中都会减小 B.稀释后溶液的pH=5
C.稀释后甲酸的电离度会增大 D.与稀释前比较,稀释后水的电离程度增大
(4)现有0.1mol•L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是______ 。
①电离程度增大 ②c(NH3•H2O)增大 ③NH 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥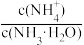 增大 ⑦
增大 ⑦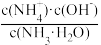 减小
减小
(1)①25℃时,已知不同pH条件下,水溶液中碳元素的存在形态如图所示。下列说法不正确的是

a.pH=8时,溶液中含碳元素的微粒主要是HCO

b.A点溶液中H2CO3和HCO
 浓度相同
浓度相同c.当c(HCO
 )=c(CO
)=c(CO )时,c(H+)>c(OH-)
)时,c(H+)>c(OH-)②向上述pH=8.4的水溶液中加入NaOH溶液时发生反应的离子方程式是
(2)H2CO3以及其他部分弱酸的电离平衡常数如表:
| 弱酸 | H2S | H2CO3 | HClO |
| 电离平衡常数(25℃) | Ka1=1.1×10-7 Ka2=1.3×10-13 | Ka1=4.5×10-7 Ka2=4.7×10-11 | Ka=4.8×10-8 |
②将少量CO2气体通入NaClO溶液中,写出该反应的离子方程式:
(3)常温下,已知0.1mol/L一元酸HCOOH(甲酸)溶液中
 =1×10-8。
=1×10-8。①0.1mol/LHCOOH溶液的pH=
②取10mL0.1mol/L的HCOOH溶液稀释至100倍,下列有关说法正确的是
A.所有离子的浓度在稀释过程中都会减小 B.稀释后溶液的pH=5
C.稀释后甲酸的电离度会增大 D.与稀释前比较,稀释后水的电离程度增大
(4)现有0.1mol•L-1氨水10mL,加蒸馏水稀释到1L后,下列变化中正确的是
①电离程度增大 ②c(NH3•H2O)增大 ③NH
 数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥
数目增多 ④c(OH-)增大 ⑤导电性增强 ⑥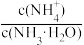 增大 ⑦
增大 ⑦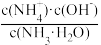 减小
减小| A.①②③ | B.①③⑤ | C.①③⑥ | D.②④⑥ |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】I、如图表示元素周期表中部分元素的某种性质(X值)随原子序数变化的关系示意图。

(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是_______ (填元素符号)。
(2)预测S元素与 元素x值的大小关系为
元素x值的大小关系为_______ ,x值最小的元素在元素周期表中的位置是_______ (放射性元素除外)。
(3)下列关于元素性质的说法正确的是_______ (填标号)。
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
II、今有① 、②HCl、③
、②HCl、③ 三种溶液,根据要求回答下列问题:
三种溶液,根据要求回答下列问题:
(4)pH相同的三种酸溶液各lmL,加水稀释相同倍数后,溶液中水电离出来的 的关系为
的关系为_______ 。(用序号填空,下同)
(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为_______ 。
(6)中和等体积相同浓度的烧碱溶液,需同浓度的三种溶液的体积分别为 、
、 、
、 ,则
,则 、
、 、
、 的关系为
的关系为_______ (用等式表示)。
III.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(7)实验室在保存FeCl3溶液时,常在溶液中加少量的_______ ,以抑制其水解;把 溶液蒸干并灼烧,最后得到的固体主要产物是
溶液蒸干并灼烧,最后得到的固体主要产物是_______ 。
(8)在日常生活中经常用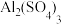 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:_______ 。

(1)短周期中原子核外p能级上电子总数与s能级上电子总数相等的元素是
(2)预测S元素与
 元素x值的大小关系为
元素x值的大小关系为(3)下列关于元素性质的说法正确的是
a.X值可反映元素最高正化合价的变化规律
b.X值可反映元素在化合物中吸引电子的能力
c.X值的大小可用来判断元素金属性和非金属性的强弱
II、今有①
 、②HCl、③
、②HCl、③ 三种溶液,根据要求回答下列问题:
三种溶液,根据要求回答下列问题:(4)pH相同的三种酸溶液各lmL,加水稀释相同倍数后,溶液中水电离出来的
 的关系为
的关系为(5)当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为
(6)中和等体积相同浓度的烧碱溶液,需同浓度的三种溶液的体积分别为
 、
、 、
、 ,则
,则 、
、 、
、 的关系为
的关系为III.平衡思想是化学研究的一个重要观念,在水溶液中存在多种平衡体系。
(7)实验室在保存FeCl3溶液时,常在溶液中加少量的
 溶液蒸干并灼烧,最后得到的固体主要产物是
溶液蒸干并灼烧,最后得到的固体主要产物是(8)在日常生活中经常用
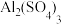 和
和 混合溶液作灭火剂,请用离子方程式表示其灭火原理:
混合溶液作灭火剂,请用离子方程式表示其灭火原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有常温下的4种溶液:①
 溶液;②
溶液;② HCl溶液;③
HCl溶液;③ 的氨水:④
的氨水:④ 的NaOH溶液。回答下列问题:
的NaOH溶液。回答下列问题:
(1)在25℃时,若用④滴定未知浓度的 应选用
应选用___________ 作指示剂。
(2)将4种溶液同等程度稀释10倍后,溶液pH由大到小的顺序是___________ 。
(3)若将①④混合后所得溶液中的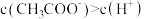 ,则下列说法正确的是___________(填序号)
,则下列说法正确的是___________(填序号)
(4)若将②③混合后所得溶液的 ,则消耗溶液的体积:②
,则消耗溶液的体积:②___________ ③(填“>”“<”或“=”)。
(5)若将②④混合后所得溶液的 ,则消耗②和④溶液的体积比:
,则消耗②和④溶液的体积比:
___________ 。
(6)在25℃时,将bmol/L的KCN溶液与②等体积混合,反应达到平衡时,测得溶液 ,则KCN溶液的物质的量浓度b
,则KCN溶液的物质的量浓度b___________ 0.01 mol/L(填“>”、“<”或“=”);用含b的代数式表示HCN的电离常数
___________ 。

 溶液;②
溶液;② HCl溶液;③
HCl溶液;③ 的氨水:④
的氨水:④ 的NaOH溶液。回答下列问题:
的NaOH溶液。回答下列问题:(1)在25℃时,若用④滴定未知浓度的
 应选用
应选用(2)将4种溶液同等程度稀释10倍后,溶液pH由大到小的顺序是
(3)若将①④混合后所得溶液中的
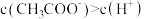 ,则下列说法正确的是___________(填序号)
,则下列说法正确的是___________(填序号)| A.溶液一定呈酸性 | B.溶液一定呈碱性 |
| C.溶液一定呈中性 | D.溶液可能呈酸性、中性或碱性 |
 ,则消耗溶液的体积:②
,则消耗溶液的体积:②(5)若将②④混合后所得溶液的
 ,则消耗②和④溶液的体积比:
,则消耗②和④溶液的体积比:
(6)在25℃时,将bmol/L的KCN溶液与②等体积混合,反应达到平衡时,测得溶液
 ,则KCN溶液的物质的量浓度b
,则KCN溶液的物质的量浓度b
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】国家标准规定,酿造的食醋中醋酸的含量不得低于3.5g/100mL。选择酚酞作指示剂,用标准NaOH溶液测定白醋中醋酸的浓度,以检测白醋是否符合国家标准。测定过程如图所示:

(1)①滴定达到终点时的现象是滴入半滴标准NaOH溶液后_______ 。
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则消耗NaOH溶液的体积为_______ mL。

③下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是_______ (填编号)。
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后用白醋稀溶液润洗
D.滴定过程中摇动锥形瓶时有液滴溅出
E.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
F.碱式滴定管在滴定前有气泡,滴定后气泡消失
(2)若用0.1 NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1
NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1 的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。
的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。

①滴定醋酸的曲线是_______ (填“Ⅰ”或“Ⅱ”)。
②滴定醋酸时,M点时微粒浓度大小关系是_______ ( 除外)。
除外)。
③滴定醋酸过程中,下列关系正确的是_______ 。
A.M点时溶液中有: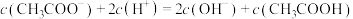
B.醋酸恰好反应完全时,溶液中有:
C.滴定过程中,曲线上任何一点,溶液中都有:
D.滴定过程中可能出现: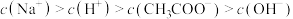
E.v=20mL时,溶液中有:
④若25℃时,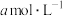 的醋酸与0.01
的醋酸与0.01 的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为_______ (用含a的代数式表示)。

(1)①滴定达到终点时的现象是滴入半滴标准NaOH溶液后
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则消耗NaOH溶液的体积为

③下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后用白醋稀溶液润洗
D.滴定过程中摇动锥形瓶时有液滴溅出
E.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
F.碱式滴定管在滴定前有气泡,滴定后气泡消失
(2)若用0.1
 NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1
NaOH溶液分别滴定体积均为20.00mL、浓度均为0.1 的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。
的盐酸和醋酸溶液,得到滴定过程中pH随加入NaOH溶液体积而变化的两条滴定曲线如图所示。
①滴定醋酸的曲线是
②滴定醋酸时,M点时微粒浓度大小关系是
 除外)。
除外)。③滴定醋酸过程中,下列关系正确的是
A.M点时溶液中有:
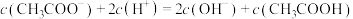
B.醋酸恰好反应完全时,溶液中有:

C.滴定过程中,曲线上任何一点,溶液中都有:

D.滴定过程中可能出现:
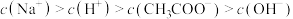
E.v=20mL时,溶液中有:

④若25℃时,
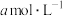 的醋酸与0.01
的醋酸与0.01 的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
的氢氧化钠溶液等体积混合显中性,则醋酸的电离常数为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据所学知识回答问题
Ⅰ、现有①硫酸铜、②碳酸钙、③磷酸、④硫化氢、⑤三氧化硫、⑥金属镁、⑦石墨、⑧苛性钾、⑨氨水、⑩熟石灰,其中
(1)属于强电解质的是___________ (填序号,下同)。
(2)属于弱电解质的是___________ 。
(3)属于非电解质的是___________ 。
(4)既不是电解质,又不是非电解质的是___________ 。
(5)能导电的是___________ 。
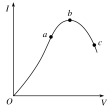
Ⅱ、在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:
(6)O点导电能力为0的理由是___________ 。
(7)a、b、c三点溶液中氢离子浓度由小到大的顺序为___________ 。
(8)a、b、c三点处,电离程度最大的是___________ 。
(9)500 mL 0.1 mol/L 醋酸溶液a和500 mL 0.1 mol/L盐酸溶液b与足量Zn粉反应,初始速率a___________ b;生成H2的量a___________ b;完全中和这两种酸,消耗NaOH的量a___________ b.(填“>”“<”或“=”)
Ⅰ、现有①硫酸铜、②碳酸钙、③磷酸、④硫化氢、⑤三氧化硫、⑥金属镁、⑦石墨、⑧苛性钾、⑨氨水、⑩熟石灰,其中
(1)属于强电解质的是
(2)属于弱电解质的是
(3)属于非电解质的是
(4)既不是电解质,又不是非电解质的是
(5)能导电的是
Ⅱ、在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力I随加入水的体积V变化的曲线如图所示。请回答下列问题:

(6)O点导电能力为0的理由是
(7)a、b、c三点溶液中氢离子浓度由小到大的顺序为
(8)a、b、c三点处,电离程度最大的是
(9)500 mL 0.1 mol/L 醋酸溶液a和500 mL 0.1 mol/L盐酸溶液b与足量Zn粉反应,初始速率a
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】25℃时,用0.10mol·L-1的氨水滴定 10.00mL0.05 mol·L-1的二元酸 H2Y的溶液,滴定过程中加入氨水的体积(V)与溶液中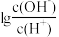 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
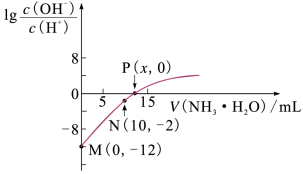
(1)写出H2Y的电离方程式_______
(2)滴定过程中,M、N、P三点对应水电离出的H+浓度由大到小的顺序为_______
(3)用x表示的NH3·H2O电离平衡常数值Kb=_______
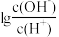 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是
(1)写出H2Y的电离方程式
(2)滴定过程中,M、N、P三点对应水电离出的H+浓度由大到小的顺序为
(3)用x表示的NH3·H2O电离平衡常数值Kb=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】分布系数的概念在分析化学中非常重要。在酸碱平衡中,分布系数指酸碱以各种形式存在的平衡浓度与其分析浓度的比值。
(1)请以H3A为例,推导出分布系数公式

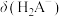
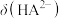
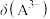
 、
、 、
、 、
、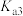 的式子表示,写出表达式即可]。
的式子表示,写出表达式即可]。(2)请用分布系数公式与电荷守恒公式,分别计算出
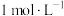 和
和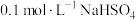 中
中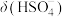 的精确值
的精确值 能否拆为H+和
能否拆为H+和
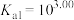 、
、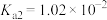 。写出计算过程)
。写出计算过程)
您最近一年使用:0次



