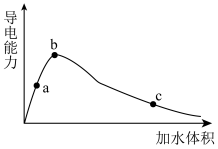
25℃时,将一定量的冰醋酸(即无水乙酸)加水稀释,稀释过程中溶液的导电性变化如图所示。则下列说法不正确的是
A.醋酸的电离程度: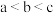 |
B.溶液中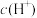 : : |
C.溶液中 : : |
D.从b点到c点,溶液中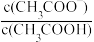 的比值增大 的比值增大 |
更新时间:2024-05-08 15:33:03
|
【知识点】 弱电解质在水溶液中的电离平衡解读
相似题推荐
单选题
|
容易
(0.94)
【推荐1】人体血液的正常pH范围是7.35~7.45.血浆“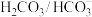 ”缓冲体系对稳定体系酸碱度有重要作用
”缓冲体系对稳定体系酸碱度有重要作用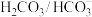 的缓冲作用可用下列平衡表示:
的缓冲作用可用下列平衡表示: 。下列说法错误的是
。下列说法错误的是
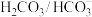 ”缓冲体系对稳定体系酸碱度有重要作用
”缓冲体系对稳定体系酸碱度有重要作用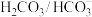 的缓冲作用可用下列平衡表示:
的缓冲作用可用下列平衡表示: 。下列说法错误的是
。下列说法错误的是A.人体血浆中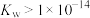 |
B.运动后血液中的 增加,血液的pH降低 增加,血液的pH降低 |
C.当人体血液中pH升高时,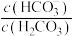 的值减小 的值减小 |
D.人体血浆中的 可以消耗无氧呼吸产生的乳酸 可以消耗无氧呼吸产生的乳酸 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】下列符号表征或说法错误的是
A. 的电离: 的电离: |
B.基态Fe原子的价层电子排布式: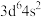 |
C. 的结构示意图: 的结构示意图: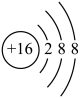 |
D. 分子的空间结构:三角锥形 分子的空间结构:三角锥形 |
您最近一年使用:0次



