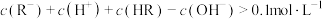常温下向 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是
 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是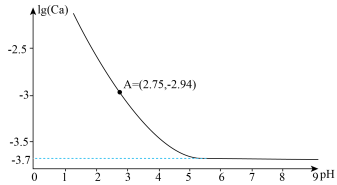
A.溶液中始终存在: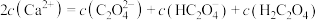 |
B.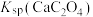 的数量级为 的数量级为 |
C.pH=7时,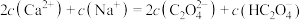 |
D.A点时,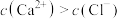 |
更新时间:2024-05-17 21:32:29
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】常温下,向5mL一定浓度的硫酸铜溶液中逐滴滴入 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中pc{
络离子(假定溶液混合后体积不变)。滴加过程中pc{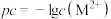 ,
, 为
为 或
或 }与氨水体积的关系如图所示。下列说法错误的是
}与氨水体积的关系如图所示。下列说法错误的是
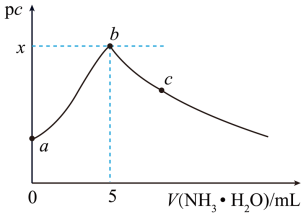
 的氨水,首先析出浅蓝色的
的氨水,首先析出浅蓝色的 沉淀,氨水过量时此沉淀溶解,形成
沉淀,氨水过量时此沉淀溶解,形成 络离子(假定溶液混合后体积不变)。滴加过程中pc{
络离子(假定溶液混合后体积不变)。滴加过程中pc{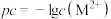 ,
, 为
为 或
或 }与氨水体积的关系如图所示。下列说法错误的是
}与氨水体积的关系如图所示。下列说法错误的是
A.硫酸铜溶液的浓度为 |
| B.常温下,b点溶液中水的电离程度低于纯水的 |
C.c点溶液中存在 |
D.常温下,忽略 的影响,可得 的影响,可得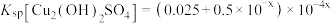 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】亚氯酸钠是一种高效氧化剂漂白剂,主要用于 棉纺、亚麻、纸浆等漂白亚氯酸钠(NaClO2)在溶液中可生成ClO2、HClO2、ClO2-、Cl- 等,其中HClO2和ClO2都具有漂白作用,但ClO2是有毒气体。经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析不正确的是
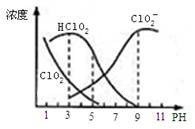

| A.亚氯酸钠在碱性条件下较稳定 |
| B.25℃时,HClO2的电离平衡常数的数值Ka=10-6 |
| C.使用该漂白剂的最佳pH为3 |
| D.25℃时,同浓度的HClO2溶液和NaClO2溶液等体积混合,混合溶液中有则c(HClO2)+ 2c(H+)=c(ClO2-)+ 2c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,下列溶液中各粒子的物质的量浓度关系正确的是
| A.0.1 mol·L-1的氨水中,c(NH4+)=c(OH-)=0.1 mol·L-1 |
| B.NH4Cl溶液中,若溶液的pH=6,则c(Cl-)-c(NH4+)=9.9×10-7 mol·L-1 |
| C.0.1 mol·L-1的Na2SO4溶液中,c(SO42-)>c(Na+)>c(OH-)=c(H+) |
| D.0.1 mol·L-1的Na2SO3溶液中,c(Na+)=2 c(SO32-)+c(HCO3-)+c(H2SO3) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
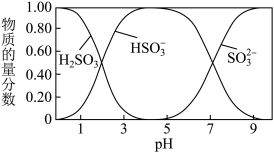
【推荐1】25℃时,起始浓度为0.1mol.L-1的亚硫酸溶液中,H2SO3、HSO 、SO
、SO 三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
 、SO
、SO 三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
三种微粒的物质的量分数(即微粒本身物质的量与三种粒子总物质的量之比)随pH变化的关系如图所示。下列说法正确的是
| A.读取图中数据计算可得到常温下亚硫酸溶液的Ka2≈10-7 |
B.向该体系中加入一定量的NaOH固体,HSO 的物质的量分数一定增大 的物质的量分数一定增大 |
C.在pH=1.0溶液中:c(H2SO3)>c(HSO )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
D.在该体系中的任意一点都存在:c2(H+)=c(H+)·c(HSO )+2c(H+)∙c(SO )+2c(H+)∙c(SO )+Kw )+Kw |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】乙二胺(H2NCH2CH2NH2),无色液体,电离类似于氨:NH3+H2O
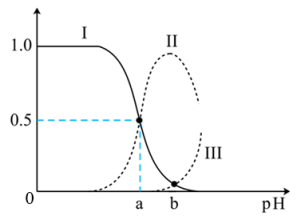
 +OH-,25℃时,Kb1=10-4.07,Kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是( )
+OH-,25℃时,Kb1=10-4.07,Kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是( )

 +OH-,25℃时,Kb1=10-4.07,Kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是( )
+OH-,25℃时,Kb1=10-4.07,Kb2=10-7.15;乙二胺溶液中含氮微粒的物质的量浓度分数随溶液pH的变化如图。下列说法不正确的是( )
A.曲线Ⅱ代表的微粒符号为H2NCH2CH2NH |
| B.曲线Ⅰ与曲线Ⅱ相交点对应pH=6.85 |
C.0.1 mol·L-1 H2NCH2CH2NH3Cl溶液中各离子浓度大小关系为c(Cl-)>c(H2NCH2CH2NH )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
D.乙二胺在水溶液中第二步电离的方程式:H2NCH2CH2NH +H2O +H2O [H3NCH2CH2NH3]2++OH- [H3NCH2CH2NH3]2++OH- |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】室温下,通过下列实验探究 、
、 溶液的性质。
溶液的性质。
实验1:用 试纸测量
试纸测量 溶液的
溶液的 ,测得
,测得 约为8
约为8
实验2:将 溶液与
溶液与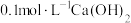 溶液等体积混合,产生白色沉淀
溶液等体积混合,产生白色沉淀
实验3:饱和 溶液中通入
溶液中通入 产生白色沉淀,溶液
产生白色沉淀,溶液 从12下降到约为9
从12下降到约为9
实验4:向 溶液中滴加几滴酚酞,加水稀释,溶液红色变浅
溶液中滴加几滴酚酞,加水稀释,溶液红色变浅
下列说法正确的是
 、
、 溶液的性质。
溶液的性质。实验1:用
 试纸测量
试纸测量 溶液的
溶液的 ,测得
,测得 约为8
约为8实验2:将
 溶液与
溶液与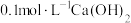 溶液等体积混合,产生白色沉淀
溶液等体积混合,产生白色沉淀实验3:饱和
 溶液中通入
溶液中通入 产生白色沉淀,溶液
产生白色沉淀,溶液 从12下降到约为9
从12下降到约为9实验4:向
 溶液中滴加几滴酚酞,加水稀释,溶液红色变浅
溶液中滴加几滴酚酞,加水稀释,溶液红色变浅下列说法正确的是
A.由实验1可得出: |
B.由实验2可推测: |
C.实验3中发生反应的离子方程式为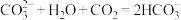 |
D.实验4中加水稀释后,溶液中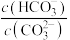 的值增大 的值增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
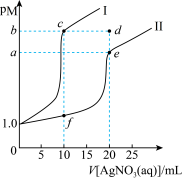
【推荐2】常温下,分别向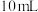 浓度均为
浓度均为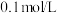 的NaX溶液、
的NaX溶液、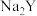 溶液滴加
溶液滴加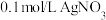 溶液,pM与
溶液,pM与 溶液体积的关系如图所示[
溶液体积的关系如图所示[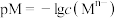 ,
,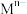 代表
代表 、
、 ],下列说法正确的是
],下列说法正确的是
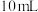 浓度均为
浓度均为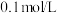 的NaX溶液、
的NaX溶液、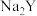 溶液滴加
溶液滴加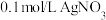 溶液,pM与
溶液,pM与 溶液体积的关系如图所示[
溶液体积的关系如图所示[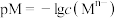 ,
,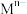 代表
代表 、
、 ],下列说法正确的是
],下列说法正确的是
A.曲线Ⅱ表示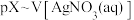 的关系图 的关系图 |
B.常温下,饱和溶液的物质的量浓度: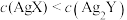 |
C.若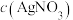 变为 变为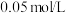 ,则c点向e点移动 ,则c点向e点移动 |
D.d点是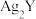 的饱和溶液 的饱和溶液 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】常温下,向500mL一定物质的量浓度KAl(SO4)2溶液中逐滴加入0.1mol·L-1Ba(OH)2溶液,加入Ba(OH)2溶液的体积和所得沉淀的质量关系如图,(忽略混合时溶液体积的变化),已知:Ksp(BaSO4)=1.1×10-10。下列说法正确的是


A.ab段发生离子反应有:SO +Ba2+=BaSO4↓、Al3++3OH-=Al(OH)3↓ +Ba2+=BaSO4↓、Al3++3OH-=Al(OH)3↓ |
| B.a点、b点、c点三点所对应的溶液的水的电离程度:a>b>c |
C.若V2=1;V3=1.5时,c点溶液中c(SO )=4.4×10-9mol·L-1 )=4.4×10-9mol·L-1 |
| D.若V2=1时,m2=27.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
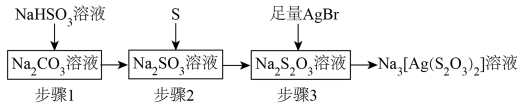
【推荐1】硫代硫酸钠( )的制备和应用相关流程如图所示。
)的制备和应用相关流程如图所示。
已知:25℃时, 的
的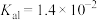 ,
, ;
; 的
的 ,
,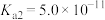
下列说法正确的是
 )的制备和应用相关流程如图所示。
)的制备和应用相关流程如图所示。
已知:25℃时,
 的
的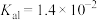 ,
, ;
; 的
的 ,
,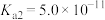
下列说法正确的是
A.步骤1所得的溶液中: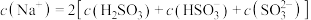 |
B.步骤1过程中pH=8时,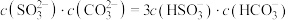 |
C.步骤3所得的清液中: |
D.步骤3的离子方程式为: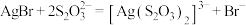 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知 ,25℃时,
,25℃时, 的
的 ,
,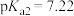 。用
。用 溶液滴定
溶液滴定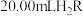 溶液,溶液中
溶液,溶液中 、
、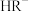 、
、 的分布分数
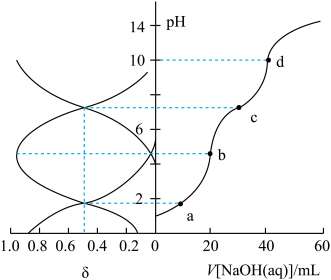
的分布分数 随pH变化曲线及滴定曲线如下图(忽略滴定过程中温度的变化)。下列说法错误的是[如
随pH变化曲线及滴定曲线如下图(忽略滴定过程中温度的变化)。下列说法错误的是[如 分布分数:
分布分数: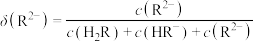 ]
]
 ,25℃时,
,25℃时, 的
的 ,
,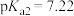 。用
。用 溶液滴定
溶液滴定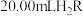 溶液,溶液中
溶液,溶液中 、
、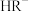 、
、 的分布分数
的分布分数 随pH变化曲线及滴定曲线如下图(忽略滴定过程中温度的变化)。下列说法错误的是[如
随pH变化曲线及滴定曲线如下图(忽略滴定过程中温度的变化)。下列说法错误的是[如 分布分数:
分布分数: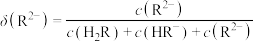 ]
]
| A.两次突变,应选用不同的指示剂 |
B.pH=8时: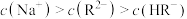 |
| C.b点溶液的pH约为4.54 |
D.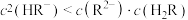 |
您最近一年使用:0次

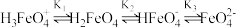 。常温下,
。常温下, 的高铁酸盐溶液中,含铁粒子的物质的量分数
的高铁酸盐溶液中,含铁粒子的物质的量分数 随
随 的变化如图所示
的变化如图所示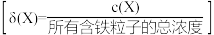 。下列说法错误的是
。下列说法错误的是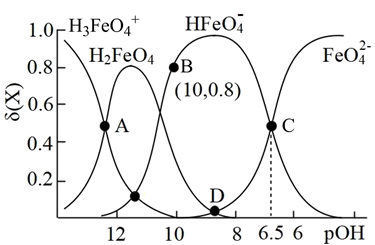
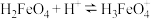 的平衡常数
的平衡常数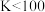
 时,
时,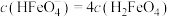
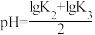
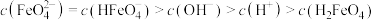
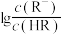 与溶液pH的关系如图所示(已知
与溶液pH的关系如图所示(已知 )。下列说法正确的是
)。下列说法正确的是
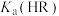 的数量级是
的数量级是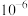
 的分布分数
的分布分数 等于
等于 时,溶液的pH=4.1
时,溶液的pH=4.1