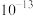常温下,向某浓度的HA溶液中加入NaOH固体,保持溶液的体积和温度不变,测得pH与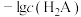 、
、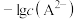 、
、 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
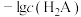 、
、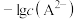 、
、 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
A.常温下, 的电离平衡常数 的电离平衡常数 为 为 |
B.a点时, |
| C.a点→b点过程中,水的电离程度增大 |
D.NaHA溶液中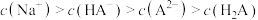 |
更新时间:2024-05-06 19:47:12
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,向体积均为V0、浓度均为0.10 mol·L-1的MOH和ROH溶液中分别加水稀释至体积为V,溶液pH随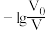 的变化如图所示,
的变化如图所示,
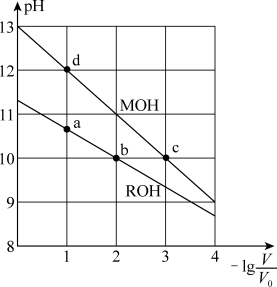
下列叙述正确的是
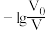 的变化如图所示,
的变化如图所示,
下列叙述正确的是
A.b、c两点的溶液中: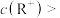 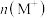 |
| B.MOH的电离程度:c点小于d点 |
| C.溶液中水的的电离程度:b>c>a>d |
D.当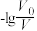 =2时,若两溶液同时升高温度,则 =2时,若两溶液同时升高温度,则 增大 增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列叙述正确 的是
A.用水稀释0.1 mol/L的氨水,则溶液中 增大 增大 |
| B.pH=3的盐酸和醋酸分别升高相同的温度,pH均不变 |
| C.在等体积等pH 的盐酸和醋酸两溶液中分别加入等质量的相同锌粒,若只有一种溶液中的锌粒有剩余,则该溶液一定是盐酸; |
| D.两种氨水溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c2=10 c1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知: 是一元弱酸。常温下,向
是一元弱酸。常温下,向 的
的 溶液滴加
溶液滴加 盐酸,测得溶液
盐酸,测得溶液 [
[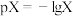 ,
, 为
为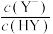 ]和
]和 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
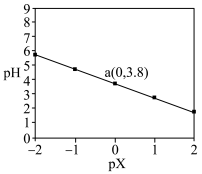
 是一元弱酸。常温下,向
是一元弱酸。常温下,向 的
的 溶液滴加
溶液滴加 盐酸,测得溶液
盐酸,测得溶液 [
[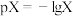 ,
, 为
为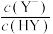 ]和
]和 的关系如图所示。下列叙述正确的是
的关系如图所示。下列叙述正确的是
A.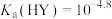 |
B. 点代表加入盐酸体积为 点代表加入盐酸体积为 |
C.加水稀释 溶液,所有离子浓度均减小 溶液,所有离子浓度均减小 |
D.浓度均为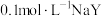 和 和 的混合溶液中存在: 的混合溶液中存在: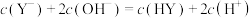 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】已知: 常温下,(1) Ka1(H2CO3)=4.3×10-7, Ka2(H2CO3)=5.6×10-11;(2)H2R及其钠盐的溶液中,H2R、HR-、R2-分别在三者中所占的物质的量分数(α)随溶液pH变化关系如图所示,下列叙述错误的是


| A.在pH=4.3的溶液中:3c(R2-)=c(Na+)+c(H+)-c(OH-) |
| B.等体积等浓度的NaOH溶液与H2R溶液混合后,溶液中水的电离程度比纯水大 |
| C.在pH=3的溶液中存在c(R2−)×c(H2R)/c2(HR−)=10-3 |
D.向Na2CO3溶液中加入少量H2R溶液,发生反应:2 +H2R=2HCO3-+R2- +H2R=2HCO3-+R2- |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】常温下,用0.10 mol·L-1 KOH溶液滴定10.00 mL 0.10 mol·L-1 H2C2O4(二元弱酸)溶液所得滴定曲线如图(混合溶液的体积可看成两者溶液的体积之和),下列说法正确的是( )
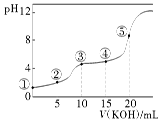
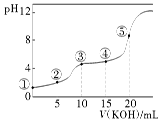
| A.点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) |
| B.点③所示溶液中:c(K+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-) |
| C.点④所示溶液中:c(K+)+c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.10 mol·L-1 |
| D.点⑤所示溶液中:c(OH-)= c(H+)+ c(HC2O4-)+ c(C2O42-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列溶液中各微粒的浓度关系或说法正确的是
| A.0.1mol•L-1pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) |
B.物质的量浓度相同的下列溶液①(NH4)2CO3②(NH4)2SO4③NH4HCO3④NH4HSO4⑤NH4Cl⑥NH3·H2O;按c(NH )由大到小的排列顺序:②>①>④>⑤>⑥>③ )由大到小的排列顺序:②>①>④>⑤>⑥>③ |
| C.向有AgCl固体的饱和溶液中加少许水,c(Ag+)和Ksp(AgCl)都不变 |
| D.0.1mol·L-1的氨水的pH=a,0.01mol·L-1的氨水的pH=b,则a=b+1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】NH4Al(SO4)2(俗名铵明矾)是食品加工中最为快捷的食品添加剂,常用于焙烤食品中;NH4Al(SO4)2在分析试剂、医药、电子工业中用途广泛。下列有关叙述不正确的是
| A.NH4Al(SO4)2可做净水剂,其理由是Al3+水解生成的Al(OH)3胶体具有吸附性 |
B.相同条件下,0.1mol·L-1NH4Al(SO4)2中c(NH )小于0.1mol·L-1NH4HSO4中c(N )小于0.1mol·L-1NH4HSO4中c(N ) ) |
| C.NH4Al(SO4)2溶液中加入盐酸抑制水解,酸性减弱 |
D.20℃时0.1mol·L-1NH4Al(SO4)2溶液的pH为3,则溶液中2c(SO )-c(NH )-c(NH )-3c(Al3+)≈10-3mol·L-1 )-3c(Al3+)≈10-3mol·L-1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】向 二元弱酸溶液中逐滴滴加
二元弱酸溶液中逐滴滴加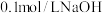 溶液,混合溶液中
溶液,混合溶液中 、
、 和
和 的物质的量分数
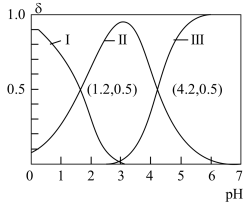
的物质的量分数 随pH变化的关系如图所示。下列叙述正确的是。
随pH变化的关系如图所示。下列叙述正确的是。
 二元弱酸溶液中逐滴滴加
二元弱酸溶液中逐滴滴加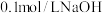 溶液,混合溶液中
溶液,混合溶液中 、
、 和
和 的物质的量分数
的物质的量分数 随pH变化的关系如图所示。下列叙述正确的是。
随pH变化的关系如图所示。下列叙述正确的是。
A.曲线II代表的微粒是 |
B. 的数量级为 的数量级为 |
C.向 的溶液中持续滴加NaOH溶液,水的电离程度持续变大 的溶液中持续滴加NaOH溶液,水的电离程度持续变大 |
D.滴加NaOH溶液的过程中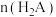 、 、 、 、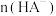 之和不变 之和不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】饱和 溶液中,
溶液中,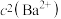 随
随 而变化,在
而变化,在 温度下,
温度下,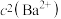 与
与 关系如右图所示。下列说法错误的是
关系如右图所示。下列说法错误的是
 溶液中,
溶液中,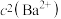 随
随 而变化,在
而变化,在 温度下,
温度下,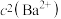 与
与 关系如右图所示。下列说法错误的是
关系如右图所示。下列说法错误的是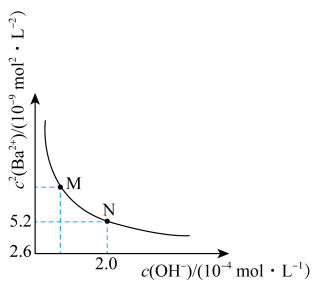
A. 的溶度积 的溶度积 |
B.若忽略 的第二步水解, 的第二步水解,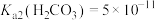 |
C.饱和 溶液中 溶液中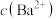 随 随 增大而减小 增大而减小 |
D. 点溶液中: 点溶液中: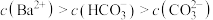 |
您最近一年使用:0次

 的值增大
的值增大 和
和 溶液混合:
溶液混合: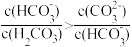
 ]与pH关系如图所示。已知:
]与pH关系如图所示。已知: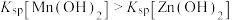 。下列叙述错误的是
。下列叙述错误的是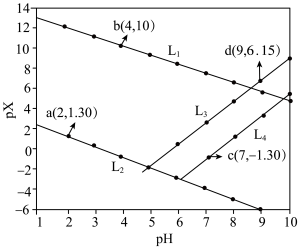
 ,L3代表Zn2+
,L3代表Zn2+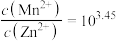
 的平衡常数
的平衡常数
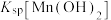 的数量级为
的数量级为