1 . 25℃时,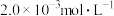 氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到
氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到 、
、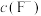 与溶液pH的变化关系,如下图所示:
与溶液pH的变化关系,如下图所示: 形式;②
形式;② 。
。
下列说法不正确的是
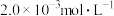 氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到
氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到 、
、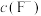 与溶液pH的变化关系,如下图所示:
与溶液pH的变化关系,如下图所示:
 形式;②
形式;② 。
。下列说法不正确的是
| A.常温下NaF溶液呈碱性 |
B.固态氟化氢中存在 ,其链状结构可表示为: ,其链状结构可表示为: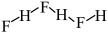 |
C.HF的电离平衡常数的值为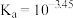 |
D.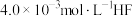 溶液与 溶液与 溶液等体积混合,调节混合液pH为3.45(忽略调节混合液体积的变化),无 溶液等体积混合,调节混合液pH为3.45(忽略调节混合液体积的变化),无 沉淀产生 沉淀产生 |
您最近一年使用:0次
名校
2 . 已知:25℃时, 的电离平衡常数
的电离平衡常数 、
、 。某小组同学用
。某小组同学用 溶液吸收
溶液吸收 得到吸收液w。
得到吸收液w。
1.请根据上述数据判断 溶液呈
溶液呈___________ (填“酸性”、“碱性”、“中性”),理由是:___________ 。
2.当吸收液w呈中性时,溶液中
___________  。
。
A. B.
B. C.
C.
 的电离平衡常数
的电离平衡常数 、
、 。某小组同学用
。某小组同学用 溶液吸收
溶液吸收 得到吸收液w。
得到吸收液w。1.请根据上述数据判断
 溶液呈
溶液呈2.当吸收液w呈中性时,溶液中

 。
。A.
 B.
B. C.
C.
您最近一年使用:0次
3 .  代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是
 代表阿伏加德罗常数的值。下列说法正确的是
代表阿伏加德罗常数的值。下列说法正确的是A.11.2L  含π键数目为 含π键数目为 |
B.NaCl和 的混合物中含1mol 的混合物中含1mol  ,则混合物中质子数为28 ,则混合物中质子数为28 |
C.电解熔融 ,阴极增重6.4g,外电路中通过电子的数目为0.1 ,阴极增重6.4g,外电路中通过电子的数目为0.1 |
D.1.7g  完全溶于1L 完全溶于1L  所得的溶液中, 所得的溶液中, 微粒的数目为0.1 微粒的数目为0.1 |
您最近一年使用:0次
名校
4 . 一定温度下,向 、
、 均为0.01 mol/L的混合溶液中持续通入CO2,始终保持CO2分压固定,体系中
均为0.01 mol/L的混合溶液中持续通入CO2,始终保持CO2分压固定,体系中 关系如图所示。其中,c表示
关系如图所示。其中,c表示 、
、 、
、 、
、 、
、 的浓度。已知
的浓度。已知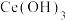 的
的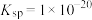 。下列说法正确的是
。下列说法正确的是
 、
、 均为0.01 mol/L的混合溶液中持续通入CO2,始终保持CO2分压固定,体系中
均为0.01 mol/L的混合溶液中持续通入CO2,始终保持CO2分压固定,体系中 关系如图所示。其中,c表示
关系如图所示。其中,c表示 、
、 、
、 、
、 、
、 的浓度。已知
的浓度。已知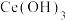 的
的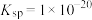 。下列说法正确的是
。下列说法正确的是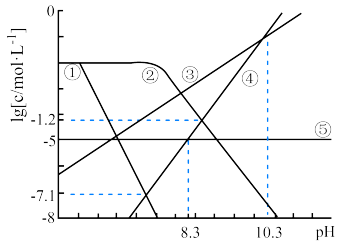
A.③代表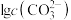 与pH的关系曲线 与pH的关系曲线 |
B.pH逐渐增大时,溶液中优先析出的沉淀为 |
C.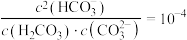 |
D.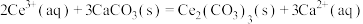 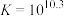 |
您最近一年使用:0次
2024-05-16更新
|
139次组卷
|
2卷引用:2024届山东省日照市五莲县第一中学高三下学期模拟预测化学试题
名校
5 . 磷烷( )是集成电路、太阳能电池等电子工业生产的原材料。工业上制备
)是集成电路、太阳能电池等电子工业生产的原材料。工业上制备 的反应原理为:
的反应原理为: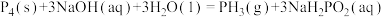 。
。 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 )是集成电路、太阳能电池等电子工业生产的原材料。工业上制备
)是集成电路、太阳能电池等电子工业生产的原材料。工业上制备 的反应原理为:
的反应原理为: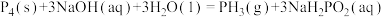 。
。 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.常温下 的NaOH溶液中水电离出的 的NaOH溶液中水电离出的 |
B.3.1g白磷( )中共价键的数目为 )中共价键的数目为 |
C.每转移3个电子,生成 磷烷 磷烷 |
D. 的 的 溶液中 溶液中 的数目小于 的数目小于 |
您最近一年使用:0次
名校
6 . 焦亚硫酸钠 是一种常用的还原剂,溶于水即生成
是一种常用的还原剂,溶于水即生成 ,用
,用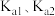 分别表示
分别表示 的一级与二级电离平衡常数。
的一级与二级电离平衡常数。 时,
时, 溶液中含硫微粒分布系数随
溶液中含硫微粒分布系数随 变化如图所示,已知
变化如图所示,已知 ,下列说法不正确的是
,下列说法不正确的是
 是一种常用的还原剂,溶于水即生成
是一种常用的还原剂,溶于水即生成 ,用
,用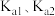 分别表示
分别表示 的一级与二级电离平衡常数。
的一级与二级电离平衡常数。 时,
时, 溶液中含硫微粒分布系数随
溶液中含硫微粒分布系数随 变化如图所示,已知
变化如图所示,已知 ,下列说法不正确的是
,下列说法不正确的是
A. 时, 时,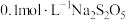 水溶液中 水溶液中 |
B.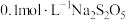 水溶液中 水溶液中 |
C.利用 氧化 氧化 回收单质硫,溶液中存在反应: 回收单质硫,溶液中存在反应: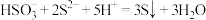 |
D.向 溶液中滴加 溶液中滴加 溶液,发生反应: 溶液,发生反应: ,其平衡常数 ,其平衡常数 |
您最近一年使用:0次
7 . 下列由实验操作及现象所得的结论正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向0.5mL溴乙烷中加入约2mL2%AgNO3溶液,振荡 | 溶液分层,上层出现浑浊 | 溴乙烷是电解质,能电离出Br- |
| B | 向苯酚钠溶液中通入足量CO2气体 | 溶液变浑浊 | 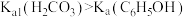 |
| C | 光洁的铜丝灼烧后,趁热插入2mL乙醇中 | 铜丝由黑色变为红色 | 乙醇具有氧化性 |
| D | 向CH3COOH溶液中加入CH3CCONH4固体,测量溶液pH变化 | pH变大 | CH3COONH4溶液呈碱性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 25℃时,向含有1 mol甘氨酸盐酸盐(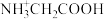 )的溶液中加入NaOH固体,溶液pH及体系中
)的溶液中加入NaOH固体,溶液pH及体系中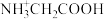 ,
, ,
,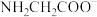 三种粒子的分布系数变化如图所示。
三种粒子的分布系数变化如图所示。 中
中 的分布系数:
的分布系数: ]
]
下列说法正确的是
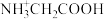 )的溶液中加入NaOH固体,溶液pH及体系中
)的溶液中加入NaOH固体,溶液pH及体系中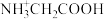 ,
, ,
,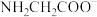 三种粒子的分布系数变化如图所示。
三种粒子的分布系数变化如图所示。
 中
中 的分布系数:
的分布系数: ]
]下列说法正确的是
A.a代表 |
| B.m点:pH小于2.35 |
C.n点溶液中 |
D.曲线上任意点溶液均存在: |
您最近一年使用:0次
9 . 室温下,某 溶液体系中满足
溶液体系中满足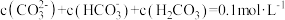 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合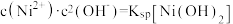 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合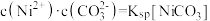 ,不同pH下
,不同pH下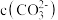 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
 溶液体系中满足
溶液体系中满足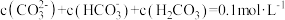 ,现利用平衡移动原理,研究
,现利用平衡移动原理,研究 在不同pH的
在不同pH的 体系中的可能产物。图1中曲线表示
体系中的可能产物。图1中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合
体系中各含碳粒子的物质的量分数与pH的关系;图2为沉淀溶解平衡曲线,曲线Ⅰ的离子浓度关系符合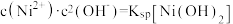 ,曲线Ⅱ的离子浓度关系符合
,曲线Ⅱ的离子浓度关系符合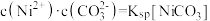 ,不同pH下
,不同pH下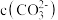 由图1得到。下列说法错误的是
由图1得到。下列说法错误的是
A.由图1, 的水解平衡常数的数量级是 的水解平衡常数的数量级是 |
B.图2中M点,溶液中存在 |
C.图2中P点,存在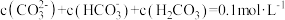 |
D.沉淀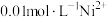 制备 制备 时,选用 时,选用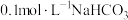 溶液比 溶液比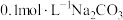 溶液效果好 溶液效果好 |
您最近一年使用:0次
2024-05-16更新
|
354次组卷
|
3卷引用:内蒙古呼和浩特市高三下学期第二次质量数据监测理科综合试题-高中化学
名校
10 . 某研究小组为研究水溶液中粒子浓度随pH的变化关系,25℃时,用NaOH调节 溶液的pH,且保持体系中
溶液的pH,且保持体系中 ,完成了一系列实验。粒子浓度的对数值(
,完成了一系列实验。粒子浓度的对数值( )、反应物初始物质的量之比
)、反应物初始物质的量之比 与pH的关系如图所示。下列说法错误的是
与pH的关系如图所示。下列说法错误的是
 溶液的pH,且保持体系中
溶液的pH,且保持体系中 ,完成了一系列实验。粒子浓度的对数值(
,完成了一系列实验。粒子浓度的对数值( )、反应物初始物质的量之比
)、反应物初始物质的量之比 与pH的关系如图所示。下列说法错误的是
与pH的关系如图所示。下列说法错误的是
A. 对应的溶液中: 对应的溶液中: |
B. 对应的溶液中: 对应的溶液中: |
C. 对应的溶液中: 对应的溶液中: |
D.水的电离程度: |
您最近一年使用:0次



