某研究小组为研究水溶液中粒子浓度随pH的变化关系,25℃时,用NaOH调节 溶液的pH,且保持体系中
溶液的pH,且保持体系中 ,完成了一系列实验。粒子浓度的对数值(
,完成了一系列实验。粒子浓度的对数值( )、反应物初始物质的量之比
)、反应物初始物质的量之比 与pH的关系如图所示。下列说法错误的是
与pH的关系如图所示。下列说法错误的是
 溶液的pH,且保持体系中
溶液的pH,且保持体系中 ,完成了一系列实验。粒子浓度的对数值(
,完成了一系列实验。粒子浓度的对数值( )、反应物初始物质的量之比
)、反应物初始物质的量之比 与pH的关系如图所示。下列说法错误的是
与pH的关系如图所示。下列说法错误的是
A. 对应的溶液中: 对应的溶液中: |
B. 对应的溶液中: 对应的溶液中: |
C. 对应的溶液中: 对应的溶液中: |
D.水的电离程度: |
2024·河北承德·二模 查看更多[2]
更新时间:2024-05-16 08:26:47
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】25℃,在 溶液中,由水电离出的
溶液中,由水电离出的 是
是
 溶液中,由水电离出的
溶液中,由水电离出的 是
是A.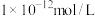 | B. | C.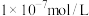 | D.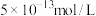 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列大小顺序排列完全正确的组合是
①气态氢化物的稳定性:HF>NH3>PH3
②熔点:Na>C3H8>CH3OH
③离子半径:K+>Ca2+>S2—
④相同温度、相同浓度的溶液中水的电离程度:NH4Cl>CH3COOH>HCl
①气态氢化物的稳定性:HF>NH3>PH3
②熔点:Na>C3H8>CH3OH
③离子半径:K+>Ca2+>S2—
④相同温度、相同浓度的溶液中水的电离程度:NH4Cl>CH3COOH>HCl
| A.①④ | B.①② | C.②③ | D.③④ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】室温下,向某Na2CO3和NaHCO3的混合溶液中逐滴加入BaCl2溶液,溶液中lgc(Ba2+)与lg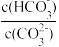 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是

(已知:H2CO3的Ka1、Ka2分别为4.2×10-7、5.6×10-11)
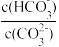 的变化关系如图所示。下列说法不正确的是
的变化关系如图所示。下列说法不正确的是
(已知:H2CO3的Ka1、Ka2分别为4.2×10-7、5.6×10-11)
| A.a对应溶液的pH大于b |
| B.b对应溶液的c(H+) = 5.6×10-9mol·L-1 |
C.a→b对应的溶液中 不变 不变 |
D.a 对应的溶液中一定存在:c(Na+)+c(H+) = 3c(HCO )+c(Cl-)+c(OH-) )+c(Cl-)+c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据下列图示所得出的结论正确的是
A.图甲表示密闭容器中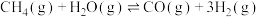 到达平衡时, 到达平衡时, 的转化率与压强、温度的变化关系曲线,说明 的转化率与压强、温度的变化关系曲线,说明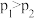 |
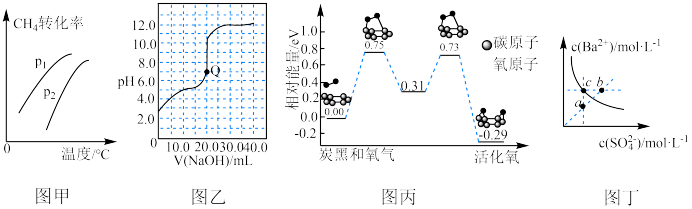
B.图乙是室温下用 NaOH溶液滴定20.00mL NaOH溶液滴定20.00mL 某一元酸HX的滴定曲线,说明HX是一元弱酸,Q点( 某一元酸HX的滴定曲线,说明HX是一元弱酸,Q点( ): ):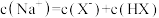 |
C.图丙表示炭黑作用下 生成活化氧过程中能量变化情况,说明活化氧分子时释放能量 生成活化氧过程中能量变化情况,说明活化氧分子时释放能量 |
D.图丁是室温下 在水中的沉淀溶解平衡曲线,若向a点加入 在水中的沉淀溶解平衡曲线,若向a点加入 固体,则溶液组成可实现b点状态 固体,则溶液组成可实现b点状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知25℃时,Ka1(H2C2O4)=5.9×10−2,Ka2(H2C2O4)=6.4×10−5。为探究Na2C2O4溶液的性质,进行如下实验:
①测定0.1000mol·L−1Na2C2O4溶液pH为8.4;
②向0.2000mol·L−1Na2C2O4溶液中滴加等浓度等体积盐酸,无明显现象;
③向0.1000mol·L−1Na2C2O4溶液中,滴加等浓度的盐酸至溶液pH=7;
④向0.1000mol·L−1Na2C2O4溶液中滴加几滴酸性KMnO4溶液,振荡,溶液仍为无色。
下列说法正确的是
①测定0.1000mol·L−1Na2C2O4溶液pH为8.4;
②向0.2000mol·L−1Na2C2O4溶液中滴加等浓度等体积盐酸,无明显现象;
③向0.1000mol·L−1Na2C2O4溶液中,滴加等浓度的盐酸至溶液pH=7;
④向0.1000mol·L−1Na2C2O4溶液中滴加几滴酸性KMnO4溶液,振荡,溶液仍为无色。
下列说法正确的是
A.实验①溶液中存在:c(Na)+>c(HC2O )>c((C2O )>c((C2O )>c(H+) )>c(H+) |
B.实验②所得溶液中:c(C2O )>c(H2C2O4) )>c(H2C2O4) |
C.实验③所得溶液中存在:c(Na+)=c(HC2O )+2c(C2O )+2c(C2O ) ) |
D.实验④中MnO 被还原成Mn2+,则反应的离子方程式为C2O 被还原成Mn2+,则反应的离子方程式为C2O +4MnO +4MnO +14H+=2CO2↑+4Mn2++7H2O +14H+=2CO2↑+4Mn2++7H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知某温度下 的
的 溶液呈酸性,下列关系
溶液呈酸性,下列关系不正确 的是
 的
的 溶液呈酸性,下列关系
溶液呈酸性,下列关系A. |
B.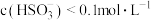 |
C. |
D.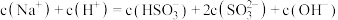 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知25℃时, ,
,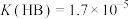 ,下列说法不正确的是
,下列说法不正确的是
 ,
,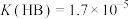 ,下列说法不正确的是
,下列说法不正确的是| A.25℃时,等浓度的NaA 和 NaB两溶液,水的电离程度:前者<后者 |
| B.25℃时,等浓度的NaA 和 NaB两溶液,c(A-)>c(B-) |
| C.25℃时,等浓度的 HA 和 HB两溶液加水稀释10倍后,电离度α(HA)<α(HB) |
| D.25℃时,c(A-)和c(B-)相等的两种酸溶液pH相等,混合后pH不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】常温下,向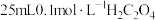 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中 、
、 、
、 的分布系数
的分布系数 随
随 的变化如图所示(忽略反应过程中温度变化)。已知:
的变化如图所示(忽略反应过程中温度变化)。已知: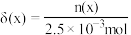 常温下,
常温下,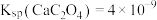 。下列说法错误的是
。下列说法错误的是
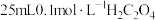 溶液中滴加
溶液中滴加 溶液,溶液中
溶液,溶液中 、
、 、
、 的分布系数
的分布系数 随
随 的变化如图所示(忽略反应过程中温度变化)。已知:
的变化如图所示(忽略反应过程中温度变化)。已知: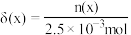 常温下,
常温下,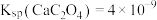 。下列说法错误的是
。下列说法错误的是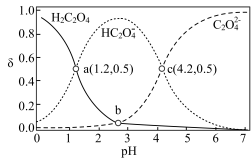
A.常温下,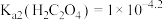 |
B.b、c点对应的溶液中均存在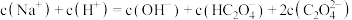 |
C. 时, 时,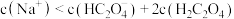 |
D.若等浓度、等体积的 溶液与 溶液与 溶液混合后产生沉淀,则上层清液中 溶液混合后产生沉淀,则上层清液中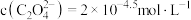 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知常温下三种酸的电离平衡常数,下列说法不正确的是
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 |
| 电离平衡常数 | 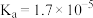 | 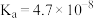 | 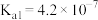 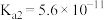 |
A.三种酸的酸性由强到弱的顺序是: |
B. 和 和 的混合溶液中: 的混合溶液中: |
C.相同温度,浓度相等的 和 和 两种溶液: 两种溶液: |
D. 溶液中通入少量 溶液中通入少量 的离子反应为: 的离子反应为: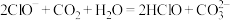 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】最新研究表明,在多孔炭材料上搭载活性组分催化氧化硫化氢,脱硫效果明显优于传统的吸附法。其反应机理如图所示,H2S在某温度下浓度为0.1mol•L-1。下列有关说法正确的是
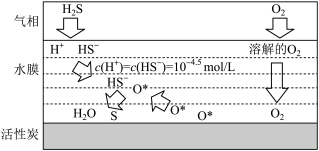

| A.该温度下,H2S一级电离常数数量级为10-8 |
| B.提高水膜的酸性,有利于增强脱硫效果 |
| C.温度越高,反应速率越快,脱硫效果越好 |
| D.多孔炭材料上搭载活性组分,主要的目的是吸附O2 |
您最近一年使用:0次

 的溶液:H+、NH
的溶液:H+、NH 、I-、SO
、I-、SO =10-12的溶液:K+、AlO
=10-12的溶液:K+、AlO 、CO
、CO 、Na+
、Na+ 为二元弱碱,在水中的电离与
为二元弱碱,在水中的电离与 相似。下列说法正确的是
相似。下列说法正确的是 会增大
会增大
 的电子式为
的电子式为


