22. 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率,请回答下列问题。
(1)①工业合成氨反应:N
2+3H
2
2NH
3是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知1molN
2完全反应生成NH
3可放出92kJ热量。如果将10molN
2和足量H
2混合,使其充分反应,放出的热量
_______(填“大于”、“小于”或“等于”)920kJ。
②已知拆开1 mol H-H键、1 mol N-H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N
2与H
2反应生成NH
3的热化学方程式为
_______。
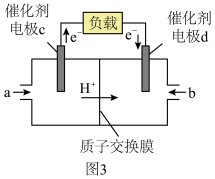
(2)某实验小组同学进行如图1所示实验,以检验化学反应中的能量变化。请根据你掌握的反应原理判断,②中的温度
_______(填“升高”或“降低”)。反应过程
_______(填“①”或“②”)的能量变化可用图2表示。
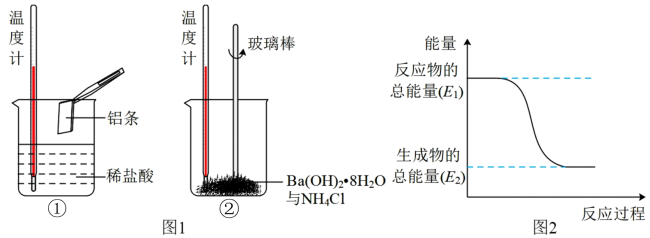
(3)用CH
3OH和O
2组合形成的质子交换膜燃料电池的结构如图3所示,则d电极是
_______(填“正极”或“负极”),d电极的电极反应式为
_______。