18. ICl(氯化碘)是红棕色液体,熔点为13.9°C,沸点为974°C,易水解,接触空气时能形成五氧化二碘,能与许多单质发生作用,溶于乙醇、乙醚等。某校研究性学习小组的同学拟用下列仪器制备氯化碘。回答下列问题:

(1)检查A装置气密性的方法为
___________。
(2)上述装置,按气流方向连接的顺序为
___________。(装置可重复使用)。
(3)C装置的作用是
___________。
(4)E装置中的物质反应时需放在水中,控制温度大约40°C,其目的是
______________________。
(5)按上述连接好的装置进行实验,实验步骤如下:
①检查装置气密性后,装入药品②打开分液漏斗活塞③关闭分液漏斗活塞④停止加热E,充分冷却⑤水浴加热E
请按正确的顺序填入上述步骤的序号
___________。
(6)ICl和水反应的化学方程式为
___________。
(7)自来水厂用ClO
2处理后的水,可用碘量法可以检测水中ClO
2的浓度,步骤如下:
I、取定体积的水样,加入过量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝。(已知:2ClO
2+2I
-=2
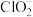
+I
2)
II、Na
2S
2O
3溶液滴定到终点。(已知:2

+I
2=

+2I
-)
问题:①滴定终点时的现象:
___________②若水样的体积为1.0L,在操作II时消耗了1.0×10
-3mol·L
-1的Na
2S
2O
3溶液15mL,则水样中ClO
2的浓度是
___________mol·L
-1。
(8)将0.64gCu全部溶于一定量的浓硝酸中,测得生成气体0.009mol(含NO、NO
2和N
2O
4),共消耗硝酸0.032mol。将生成的气体与空气混合,再通入NaOH溶液中,氮氧化物被完全吸收,产物只有NaNO
3和H
2O。计算空气中参加反应的O
2在标准状况下的体积为
___________mL。